
Утворення аморфних матеріалів
Нанокристалічна тверда фаза відповідає граничному стану метастабільного твердого тіла і може бути отримана різними способами, включаючи тверднення з рідкої або газоподібної фази, хімічне осадження з розчину, опромінювання кристалічного матеріалу високоенергетичними іонами або нейтронами. Некристалічне тверде тіло, отримане безперервним охолоджуванням з рідини, називають склом або аморфним твердим тілом. Аморфізація розплаву вимагає, щоб розплав був охолоджений з достатньо великою швидкістю, з метою придушення процесів кристалізації і отримання розупорядочного розташування атомів.
Процеси кристалізації легко пригнічуються у ряді неметалічних матеріалів (силікати, органічні полімери). У цих матеріалів, за рахунок природи міжатомних зв'язків, розплав може перейти в скло при достатньо малих швидкостях охолоджування (<102 К/с).
У металевих розплавах немає направлених зв'язків і атомні перебудови протікають дуже швидко навіть при великих ступенях охолоджування нижче рівноважної температури твердіння. Проте, дуже високі швидкості охолоджування (>106 К/с) дозволяють отримувати аморфний стан сплаву, а в багатокомпонентних системах аморфні металеві фази можуть бути отримані при нижчих швидкостях охолоджування.
1.3 Експериментальна частина
1.3.1 Обладнання:
- біологічний мікроскоп;
- проектор;
- предметне скло;
- піч для нагріву;
- електропіч;
- тиглі;
- зразки сплавів Pb- Sn за різним складом;
- термопари.
1.3.2 Порядок виконання роботи
Невелику навіску солі Na2S2O2 розплавляю у пробірці. Краплину розплаву солі поміщаю на предметне скло нормальної температури і попередньо нагріваю. За допомогою проектору і біологічного мікроскопу спостерігаю процес кристалізації, звертаю увагу на залежність розмірів кристалів від температури переохолодження.
Зразки сплавів перегріваю на 50°С вище за температуру плавлення. За допомогою термопари фіксую зниження температури кожні 10 сек.
За отриманими даними будую криву охолодження в координатах "температура-час". За перегинам на кривої охолодження визначте критичні крапки ліквідус і солідус. Користуючись діаграмою стану, визначаю склад досліджуваного сплаву та досліджую його мікроструктуру.
Процес кристалізації починається в місці найбільшого переохолодження або там, де е скупчення кристалів.
Контролюючим параметром є різниця температури розплаву і температура кристалізації( t).
Якщо значення t велике то процес кристалізації відбувається швидше та утворюється значна кількість центрів кристалізації, структура дрібнозерниста.
Якщо значення t мале то утворюється крупнозерниста структура з кристалами – дендритами.
Механізм процесу кристалізації – це зародження центрів кристалів та ріст кристалів.

Рисунок 1.4 – Схема процесу кристалізації
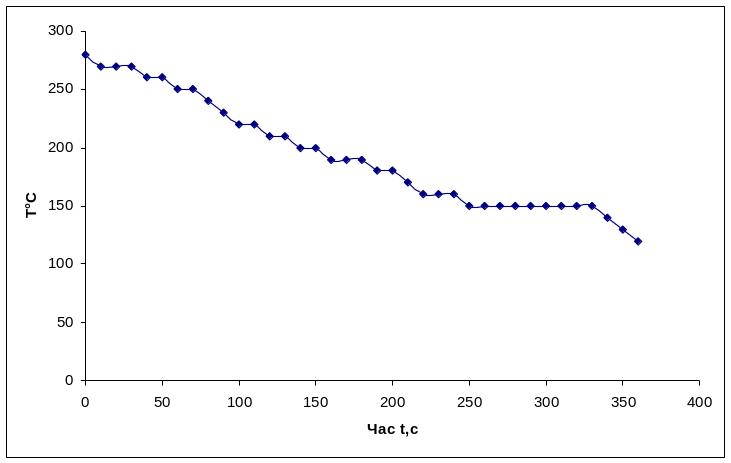
Рисунок 1.5 – Крива охолодження чистого металу
Висновок: процес кристалізації відбувається від країв до центра краплини, бо температура переохолодження з країв краплини більша, тому кристалізація починається звідти, а завершується процес в центрі краплини оскільки там більше речовини і тому витрачається більше для кристалізації часу. Якщо температура переохолодження більша тим процес кристалізації протікає швидше і тому кристалізація утворюється менше.
