
- •Общие понятия и термины.
- •3О2↔2о3 (λ – ультрафиолетовые лучи)
- •Классификация химико-технологических процессов.
- •Материальный и Энергетический Баланс.
- •Классификация химических реакций.
- •Равновесие в технологических процессах.
- •Сдвиг равновесия под влиянием концентрации реагирующих веществ.
- •Кинетика химико-технологических процессов.
- •Реактор идеального смешения непрерывный (рис-н)
- •Каскад реакторов
- •Реакторы полунепрерывные
- •Снижение энергии активации под действием катализатора
- •Устройство реакторов.
- •Трубчатый реактор непрерывного действия. Рив
- •Барботажные реакторы
- •Сырье химической промышленности.
- •Очистка воды
- •Энергия
3О2↔2о3 (λ – ультрафиолетовые лучи)
Ультрафиолетовое излучение затрачивается в этом обратимом процессе. Все живое не предохраняется от разрушительного воздействия ультрафиолетового излучения. Галогены: фрионы, окислы азота попадая в озоновый слой разрушают его. Эта проблема озоновой дыры. Загрязнение атмосферы оксидом углерода СО2 нарушает соотношение оксида углерода к кислороду (СО2 : О2), необходимое для фотосинтеза и живого организма. Загрязнение водоемов углеводородами приводит к расходу кислорода в воде, которое ведет к кислородному голоданию живых организмов.
Главными задачами технического процесса в химической технологии являются повышение производительности труда, улучшение качества продукции, снижение себестоимости продукции и снижение вредного воздействия на окружающую среду.
Развитие химической промышленности должно быть направлено на:
1) увеличение масштабов производства; мощностей химико-технологических систем (ХТС) и химико-технологических процессов (ХТП).
2) Интенсификация работы аппаратов.
3) Снижение энергозатрат и максимальное использование теплоты химических реакций.
4) Уменьшение количества стадий производства и переход к замкнутым циклам.
5) Замена периодических процессов непрерывными процессами.
6) Механизация трудоемких операций и автоматизация производства.
7) Создание малоотходных и безотходных производств.
Основные технологические понятия и определения.
Общая химическая технология изучает теоретические основы химических процессов, протекающих в реакторах, а также способы оформления химико-технологических процессов.
Реактор – аппарат в котором протекает химическая реакция.
Технологическая схема процесса получения продуктов
по
реакции
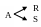 может быть изображена следующим
образом:
может быть изображена следующим
образом:
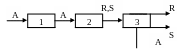
1
А
2 – химическое превращение (реакторный узел)
3 – выделение целевого продукта (разделение продуктов реакции).
В 1-й стадии протекают только физические процессы и реагент А химически неизмененным переходит во 2-ю стадию, где происходит химическая реакция и образуется продукты R и S. Обычно реакция не идет до конца и часть реагента А остается без изменений. В 3-й стадии происходит разделение продуктов: на R – целевой продукт и S – побочный продукт и оставшийся реагент А который может быть возращен в начальную стадию процесса. В 3-й стадии химических превращений нет
1стадия – относится к физическим процессам,
2стадия – к химическим процессам,
3стадия – к физико-химическим процессам.
Показателем эффективности работы аппарата, цеха, производства, завода в целом служит производительность.
Производительность – количество выработанного продукта или переработанного сырья в единицу времени. Обозначается буквой П.
П=G/, или П=VB/τ
где G ( или VB ) – кол-во продукта,
- время.
Единицы измерения [кг/ч; т/ч; т/сутки)]
Максимально возможная производительность называется мощностью. Для сравнения эффективности работы различных аппаратов, в которых протекают одни и те же химические процессы, вводят понятие интенсивности.
Интенсивность – производительность, отнесенная к какой-либо величине, характеризующей размеры аппарата (к его объему или площади сечения, длине аппарата).
И=П/Vp=G/Vp - интенсивность.
Где Vp – объем реактора,
G – количество продукта,
П – производительность.
Интенсивность может измеряется количеством продукта, получаемого в течение единицы времени с единицы объема аппарата [кг/часм3, т/сут.м2]. Расход сырья, воды, энергии и различных реагентов отнесенный к единице целевого продукта называются расходным коэффициентом.
= Q/G [т/т]
– расходный коэффициент,
Q – расход сырья,
G – кол-во продукта.
Единица измерения [м3/кг, кВт ч/кг]
Степень превращения – отношение количества реагента вступившего в реакцию, к его исходному количеству.
Пример: Для простой необратимой реакции типа АR степень превращения выражается

![]()
ХА – степень превращения реагента А.
NA,O, NA – количество исходного реагента А в начале и в конце процесса.
Иногда степень превращения ХА выражается в %
∙100%
Если реакция протекает без изменения объема, то степень превращения выражается через концентрацию:
![]()
![]()
СА,О, СА – концентрация исходного реагента А в конце и начале процесса.
Выход продукта – отношение количества полученного целевого продукта к его количеству, которое должно быть получено по стехиометрическому уравнению.
![]() или
Х =
или
Х =
![]()
Это отношение количества фактически полученного продукта Gф и максимального Gmax , которое могло бы получиться из данного исходного продукта и обозначается X
или Х =
где NR − количество продукта R в конце процесса
Селективностью – называется отношение количества целевого продукта к общему количеству получаемых продуктов. Это понятие вводится для сложных реакций, т.е. когда протекают параллельные и последовательные реакции с получением нескольких продуктов.
Пусть для реакции , целевым продуктом будет R, тогда
селективность
![]()
NR – количество продукта R
NS – количество продукта S
Нетрудно установить, что выход целевого продукта (Х) равен степени превращения (ХА) умноженного на селективность:
Х=ХА
