- •Предмет общей энергетики. Некоторые показатели мировой энергетики
- •Основные физические свойства жидкостей и газов
- •Основные положения гидростатики
- •Предмет термодинамики. Ее основные понятия и определения.
- •Термодинамические параметры состояний
- •Теплоемкость
- •8. Термодинамический процесс
- •9. Основные термодинамические процессы
- •10. Внутренняя энергия и энтальпия
- •11. Работа расширения и сжатия рабочего тела
- •Первый закон термодинамики
- •Теплосиловые установки с магнитогидродинамическим генератором
- •Закон Кирхгофа
- •Химический состав топлива
- •Марки мазута
- •Пылеугольные топки
- •Подготовка твердого топлива к сжиганию. Пылеугольные мельницы
- •Классификация паровых турбин
- •Физические основы атомной энергетики
- •Реакторные установки аэс
- •Современное состояние атомной энергетики
- •Работа водяного потока схема концентрации напора
- •Гидравлические турбины
- •Малая гидроэнергетика
- •Гидроаккумулирующие электростанции
- •Приливные электростанции
Теплоемкость
Теплоемкость физического (материального) тела - равна количеству теплоты, которую нужно подвести к телу, чтобы нагреть его на 10.
Удельная теплоемкость – теплоемкость единицы количества вещества.
В зависимости от того, в чем выражается количество, различают удельные теплоемкости:
1.массовую
 массовая
массовая
2.объемную
 объемная
объемная
3.молярную
 молярная
молярная
Величина теплоемкости газа зависит от условий нагрева.
Важное
значение имеет изобарная теплоемкость,
процесс идет при постоянном давлении

Изохорная
теплоемкость, процесс идет при постоянном
объеме


Уравнение
Майера:

Физический смысл газовой постоянной: газовая постоянная равна работе, которую совершает 1 кг газа, при нагреве на 10 в изобарном процессе.
Различают истинную и среднюю теплоемкости:
Истинная теплоемкость определяется на бесконечно малом интервале температуры, представляет собой производную подведенной теплоты по температуре.

Средняя теплоемкость находится для конечного интервала температур равная отношению подведенной теплоты к разности температур в начале и конце процесса:



Теплоемкость сложной системы равна сумме теплоемкостей компонентов.
8. Термодинамический процесс
Термодинамический процесс - процесс перехода термодинамической системы из одного состояния в другое.


 Газ
в цилиндре:
Газ
в цилиндре:

 … …
…
… …
…
… ..

Равновесным называется процесс, когда значения одноименных параметров во всех точках системы одинаковы в любой фиксированный момент времени.
В природе разновесных процессов не существует.
Термодинамический процесс:
1

 p
p

 2
2


v
Обратным называется термодинамический процесс, когда в прямом и обратном направлении система проходит через одинаковые состояния в обратной последовательности, и после возвращения системы в исходное состояние в точку 1, окружающая среда так же вернется в исходное состояние, иначе процесс необратим.
Все реальные процессы необратимы.
9. Основные термодинамические процессы
Закон
Шарля:
График изохорного процесса: 

р

v |
Закон
Гей-Люссака: 
р


v |
Закон
Бойля-Мариотта:
p теплоемкость
v |
(расширение газа в двигателе)
V
|
Значение показателей политропны в основных термодинамических процессах:
|
|



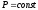







 ;
;
 ;
;

 показатель
адиабаты.
показатель
адиабаты.

 p
p 
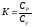





 (постоянная
теплоемкость)
(постоянная
теплоемкость)
 ,
, показатель
адиабаты
показатель
адиабаты