
- •Міністерство освіти і науки, молоді та спорту україни
- •Одеської національної академії харчових технологій
- •Міністерство освіти і науки, молоді та спорту україни одеський технічний коледж одеської національної академії харчових технологій
- •Методичні вказівки та завдання до самостійних робіт з предмету “Аналітична хімія” для студентів іі курсу
- •Самостійна робота № 1.
- •Стислі теоретичні відомості
- •Періодичний закон і періодична система елементів ді Менделєєва та її значення в аналітичній хімії Якісний аналіз.
- •Теорія електролітичної дисоціації
- •3. Хімічна рівновага в гомогенних та гетерогенних системах Добуток розчинності
- •4. Іонне добування води Водневий показник.
- •Завдання для виконання самостійної роботи
- •Самостійна робота № 2.
- •Стислі теоретичні відомості
- •1. Кількісний аналіз. Гравіметричний метод. Задачі. Особливості методу.
- •3. Типи вагових визначень.
- •4. Операції гравіметричного методу. Відокремлення осаду.
- •Переведення осаду у вагову форму.
- •5. Обчислення у гравіметричному аналізі.
- •Завдання для виконання самостійної роботи
- •Самостійна робота № 3.
- •Стислі теоретичні відомості
- •1. Сутність титриметричного аналізу.
- •2. Розчини у титриметричному аналізі.
- •3. Приготування стандартних розчинів.
- •4. Приготування стандартизованих розчинів.
- •Завдання для виконання самостійної роботи
- •Самостійна робота № 4.
- •Стислі теоретичні відомості
- •Сутність метода кислотно-основного титрування
- •Порядок титрування.
- •Кількість додавання індикатору.
- •Завдання для виконання самостійної роботи
- •Самостійна робота № 5.
- •Стислі теоретичні відомості
- •1. Методи окисно-відновного титрування. В оксидиметричному методі аналізу зустрічаються з трьома видами титрування: прямим, зворотнім та титруванням по заміщенню.
- •Завдання для виконання самостійної роботи
- •Самостійна робота № 6.
- •1. Перманганатометрія.
- •2. Йодометрія.
- •Стислі теоретичні відомості
- •Перманганатометрія.
- •У нейтральному, слабокислому або слаболужному середовищі іон МnО4- приймає три електрони, при цьому утворюється осад МnО2 або МnО(он)2 бурого кольору:
- •Йодометрія.
- •3. Характеристика розчинів, які використовують у йодометрії.
- •Завдання для виконання самостійної роботи
- •Самостійна робота № 7.
- •Стислі теоретичні відомості
- •1. Комплексонометричне титрування.
- •2. Класифікація прийомів комплексонометричного титрування.
- •Завдання для виконання самостійної роботи
- •Самостійна робота № 8.
- •2.1. Емісійний спектральний аналіз.
- •Стислі теоретичні відомості
- •1. Сутність фізико-хімічних методів аналізу.
- •2.Оптичні методи аналізу.
- •2.1. Емісійний спектральний аналіз.
- •2.2. Походження емісійних спектрів.
- •2.3. Абсорбціоний аналіз.
- •2.4. Атомно - абсорбціоний аналіз.
- •2.5. Молекулярно - абсорбціоний аналіз.
- •Завдання для виконання самостійної роботи
- •Самостійна робота № 9.
- •Стислі теоретичні відомості
- •1. Сутність рефрактометричного методу аналізу.
- •2. Показник преломлення.
- •3. Мольна та питома рефракція.
- •2. Будова і принцип роботи рефрактометра рпл-3.
- •Завдання для виконання самостійної роботи
- •Самостійна робота № 10.
- •Стислі теоретичні відомості
- •1. Сутність поляриметричного методу аналізу.
- •2. Будова та принцип роботи поляриметру.
- •3. Визначення кута обертання площини поляризації.
- •Завдання для виконання самостійної роботи
- •Самостійна робота № 11.
- •Стислі теоретичні відомості
- •2. Будова та принцип роботи флуориметру.
- •Завдання для виконання самостійної роботи
- •Самостійна робота № 12.
- •2. Сутність потенціонометричного аналізу.
- •Стислі теоретичні відомості
- •1. Сутність електрохімічних методів аналізу
- •2. Сутність потенціонометричного аналізу.
- •3. Сутність кулонометричного аналізу.
- •Методи кулонометрії
- •4. Сутність кондуктометричного аналізу .
- •5. Сутність полярографічного аналізу.
- •6. Сутність діелектрометричного аналізу .
- •Завдання для виконання самостійної роботи
- •Самостійна робота № 13.
- •Стислі теоретичні відомості
- •1. Сутність хроматографічного методу аналізу Мета і задачі.
- •2. Іонообміна хроматографія
- •3. Розподільна хроматографія.
- •4. Паперова хроматографія.
- •5. Тонкошарова хроматографія.
- •6. Газова хроматографія
- •Завдання для виконання самостійної роботи
- •Рекомендована література.
3. Розподільна хроматографія.
Вид хроматаграфічного аналізу, оснований на розподіленні компонентів хроматографіної суміші між рухомим та нерухомим розчинниками називають розподільною хроматографією. Для того, щоб використовувати систему із двух рідких фаз (рухомий та нерухомий розчинники), необхідно, щоб одні із фаз переміщалися відносно другої, а для цього необхідно закріпити одну із фаз. Така закріплена рідка фаза називається нерухомою. Інша фаза повинна повільно передвигатися вдоль поверхності розподілу з первою і вона називається рухомою.
В якості носія, який втримує нерухомий розчинник (або фазу), використовують селікагель, крохмаль, целюлозу (гідрофільні носителі) та кизельгур, скляний порошок, поліетилен (гідрофобні носителі).
Методом розподільної хроматографії можна розділяти: жирні кислоти, амінокислоти, металоорганічні сполуки, хелати, спирти, вуглеводні, пестициди, гормони, антибіотики, алкалоіди.
4. Паперова хроматографія.
Вперше паперову хроматографію в 1944 р. Використав Мартин та Синдж для анализу сумішів амінокислот. Ідентифікацію компонентів хроматографіруємої суміші проводять на смугах фільтровальнго паперу. Ефективність паперової хроматографії залкжить від трьох факторів: типу паперу; складу рухомої фази; виборочності та чутливості реагентів, які використовують для прояви компонентів.
Сорт паперу розрізняють по пористості і ступені гідротації. Ці властивості визначають швидкість фаз.
На отриманій хроматограмі можливо якісно визначити суміш речовин і дати їх кількісну характеристику. Ідентифікація компонентів суміші продиться за допомогою величини Rf, яка представляє з себе відношення відстані від центра пятна - Х, пройденого речовиною, до відстані Хf, пройденому розчинником:
Rf
=
![]()
Чим більше різниця в значеннях Rf, тим краще можна розділити речовину. Но, при дуже великих значеннях Rf речовини не встигають поділитися. На величину Rf впливають: умови проведення експерименту (сорт паперу, склад розчинюючої системы, вологість та насиченість атмосфери камери).
5. Тонкошарова хроматографія.
В методі тонкошарової хроматографії (ТШХ) розподіл речовини відбувається у тонкому шарі стаціонарної фази, нанесеної на носитель. Вперше тонкошарову хроматографію для розділення фармацевтичних настойк використав Н.А. Ізмайлов в 1935 році.
Якісну оцінку хроматограми проводять по величені Rf, сопоставляючи значення Rf з еталонними.
Метод ТШХ використовують для розподілу стероідів, ефірів, холестерину, барвників, неорганічних іонів. Паперова та тонкошарова хроматографії мають наступні переваги: низьку вартість, простота, експресність та широке використання для анализу різних видів речовин і різних розмірів проб.
6. Газова хроматографія
Газовою хроматографією називають метод розподілення і ідентифікації компонентів газової суміші, в якій рухомою фазою використовують газ або пар. Вперше метод був предложений Макртином і Джеймсом у 1952 році.
Газову хроматографію класифікують:
По агрегатному стану нерухомих фаз: газорідка (нерухома фаза, рідина, розподілена тонким шаром по поверхні якого-нибуть твердого матеріалу); газо-тверда (нерухома фаза тверда речовина).
По механізму дії: розподільна хроматографія, (газорідка один із варіантів), адсорбціонна хроматографія, (газо-тверда – варіант).
По способу переміщення фаз: проявительна або елюєнтна, фронтальна, витесняюча.
Газова і газорідка хроматографія широко використовують у різних галузях науки, техніки і медицини.
Характеристика еволюційної кривої.
Вихідну криву називають еволюційною. Основними її характеристиками або параметрами є час утримання () і утримуючий об’єм. Ці параметри служать засобом вираження результатів хроматографічного розподілу суміші речовини. Час втримання характеризується відношенням відстані (мм) на хроматограмі від момента випуска проби речовини в колонку до досягнення визиваємих речовиною на виході із максимальної концентрації (Смакс.). Швидкість руху стрічки самописця (Uл мм/с).
Кст
=
![]() ,
ммоль/г
,
ммоль/г
n
=
![]() ,
ммоль
,
ммоль
де n - число еквівалентних масс речовини;
C(A)eq - еквівалентна концентрація розчину, моль/ л;
V – об’єм розчина, л;
K - об’ємна ємкість іоніта, ммоль/ г.
Масову частку речовин, близьких по властивостям, визначають співвідношенням:
і
=
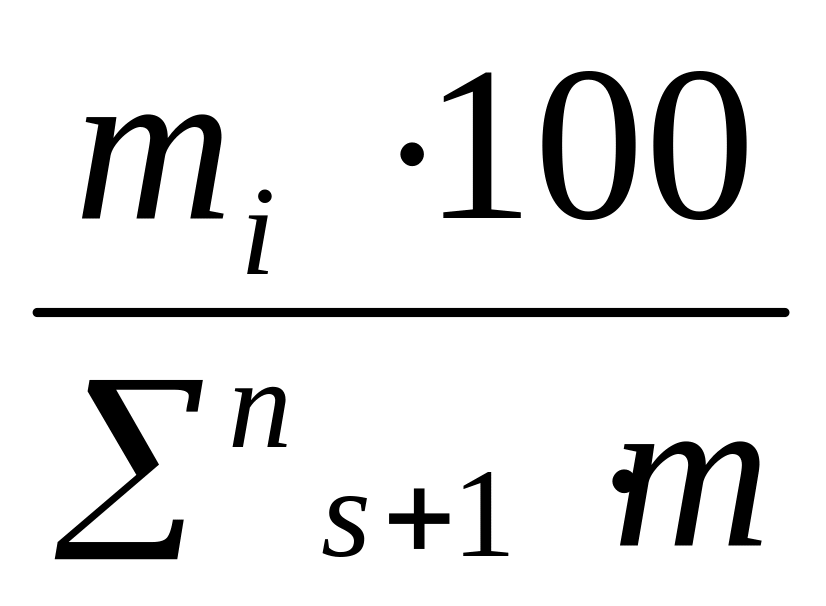 ,
%
,
%
де mi- маса паперу i-го хроматаграфічного піка;
n - число компонентів суміші.
