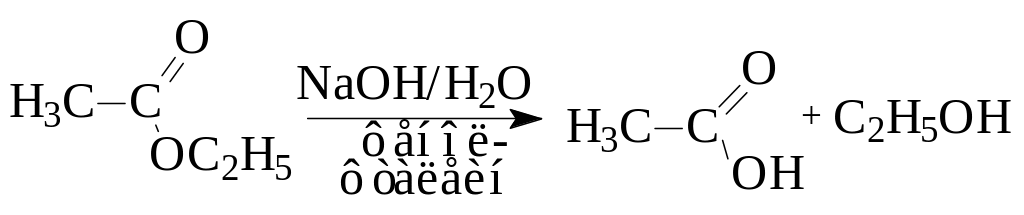- •Техника безопасности при работе в химической лаборатории
- •Физические константы органических веществ
- •Лабораторная работа Определение температуры кипения и показателя преломления неизвестного вещества
- •1. Порядок выполнения работы.
- •2. Образец оформления работы.
- •1) Определение температуры плавления с применением прибора Сиволобова.
- •Лабораторная работа Определение температуры плавления неизвестного вещества с применением прибора Сиволобова
- •1. Порядок выполнения работы.
- •2. Образец оформления работы.
- •1.1. Исследование физических свойств вещества
- •1.2. Проба на свечение пламени
- •1.3. Проба Бельштейна на галоген
- •1.4. Открытие кратной связи
- •1.5. Открытие бензольного кольца
- •1.6. Открытие боковой цепи в бензольном кольце
- •1.7. Открытие галогена в алифатической цепи
- •Аналитическая задача
- •Качественный анализ неизвестного вещества
- •Задача 1
- •1. Исследование физических свойств вещества
- •2. Качественные реакции
- •2.1.Открытие карбоксильной группы
- •2.2. Открытие фенолов.
- •2.3. Открытие карбонильной группы (открытие альдегидов и кетонов).
- •2.4. Открытие спиртов.
- •2.5. Открытие сложного эфира.
- •Идентификация индивидуальных веществ
- •1. Идентификация кислот
- •3. Идентификация альдегидов и кетонов.
- •4. Идентификация спиртов.
- •Аналитическая задача
- •Идентификация неизвестного вещества (образец)
- •Дата Подпись преподавателя Задача 2
- •1.1. Предварительные испытания
- •1.2. Качественные реакции
- •1.2.1. Открытие углеводов реакцией Молиша
- •1.2.2. Открытие моносахаридов реакцией с калий-гидроксидом
- •1.2.3. Открытие альдоз и кетоз реакцией Троммера
- •1.2.4. Открытие кетоз реакцией Селиванова
- •1.3. Идентификация моно- и дисахаридов
- •1.3.1. Фруктоза
- •1.3.2. Ксилоза
- •1.3.3. Глюкоза
- •1.3.4. Мальтоза (солодовый сахар)
- •1.3.5. Сахароза (свекловичный, тростниковый сахар)
- •1.4. Идентификация полисахаридов
- •1.4.1. Амилоза и амилопектин
- •1.4.2. Открытие целлюлозы
- •1.5. Идентификация производных сахаров
- •1.5.1. Сорбит
- •1.5.2. Глюкаровая кислота
- •Аналитическая задача по теме «Углеводы»
- •Дата Подпись преподавателя Задача 3
2.4. Открытие спиртов.
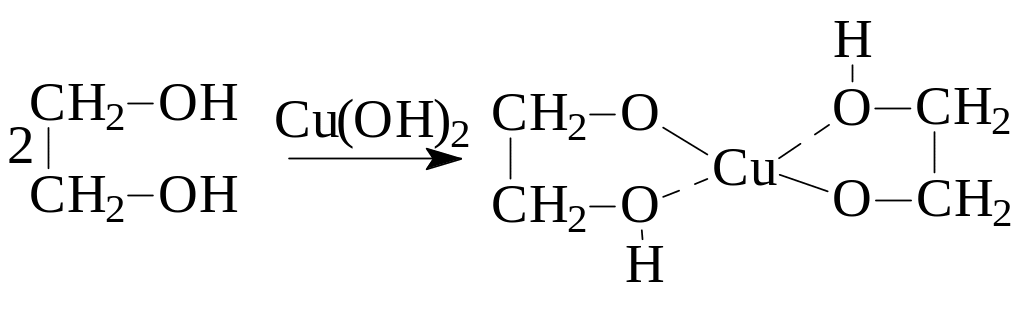
2.4.1. Открытие многоатомных вицинальных спиртов. Вицинальные спирты, содержащие две и более гидроксильных групп у соседних С-атомов открываются по их способности растворять в щелочной среде голубой осадок гидроксида меди (II) с образованием комплексных солей (гликолятов) меди темно-синего цвета.
К 3 каплям 5%-ного раствора СuSO4 (7) добавляют 4 капли 5%-ного раствора NаОН (6), при этом сразу выпадает голубой осадок гидроксида меди Cu(OH)2. Затем к смеси прибавляют 12 капли этиленгликоля (19) или неизвестного вещества, пробирку встряхивают.
При наличии многоатомного спирта голубой осадок гидроксида меди растворяется с образованием темно-синего окрашенного раствора. Записывают уравнение реакции, отмечают окраску раствора.
Если проба с неизвестным веществом положительна, то полученный раствор нагревают до кипения, наблюдая за возможными изменениями. Гликоляты устойчивы в щелочной среде и при нагревании не разлагаются. Если имеется альдегидная группа, то идет реакция Троммера (что наблюдается?).
2.4.2. Открытие одноатомных спиртов (реакция с металлическим натрием). Все гидроксилсодержащие соединения дают реакцию с металлическим натрием, внешний признак выделение пузырьков газа (какого?). Однако, одноатомные спирты не дают положительных проб с NaHCO3 (на СООН), c Cu(OH)2 (на виц. диол), c FeCl3 (на фенолы), поэтому, если эти реакции отрицательны, а проба с натрием положительна, то предполагают наличие одноатомного спирта.
Предварительно следует абсолютизировать спирт, то есть удалить примесь воды, которая обычно присутствует в спиртах, например, этиловый спирт всегда содержит около 4,5% воды. Для удаления воды в сухую пробирку вносят 10 капель этанола (20) или неизвестного вещества, добавляют 0,1 г безводного сульфата меди (43), встряхивают и дают отстояться. Безводный сульфат меди связывает воду за счет образования кристаллогидрата СuSO4·5Н2О, при этом цвет осадка изменяется с серого на голубой. Полученный обезвоженный спирт аккуратно без осадка переливают в другую сухую пробирку, куда затем бросают маленький очищенный кусочек натрия (42). При наличии ОН-группы наблюдается выделение водорода и растворение натрия. Записывают уравнение реакции, отмечают наблюдаемый результат.
![]()
В случае отрицательной пробы остатки натрия растворяют добавлением этанола (20).
2.5. Открытие сложного эфира.
Сложные эфиры не дают рассмотренных выше качественных реакций, их можно идентифицировать, проведя гидролиз в щелочной среде (реакцию омыления). В результате образуются спирт и кислота, последняя нейтрализует щелочь и открывается по обесцвечиванию малиновой окраски фенолфталеина.
К смеси 2 капель этилацетата (21) или неизвестного вещества, 5 капель воды, 3 капель фенолфталеина (49) добавляют 12 капли 5%-ного раствора NaOH (6) до возникновения красного окрашивания. Если неизвестное вещество нерастворимо в воде, то его (0,05 г) растворяют в небольшом количестве спирта (20). Пробирку нагревают при встряхивании. При наличии сложноэфирной группы наблюдается исчезновение красно-малиновой окраски индикатора. Для подтверждения результата опыт повторяют.
Записывают уравнение реакции.