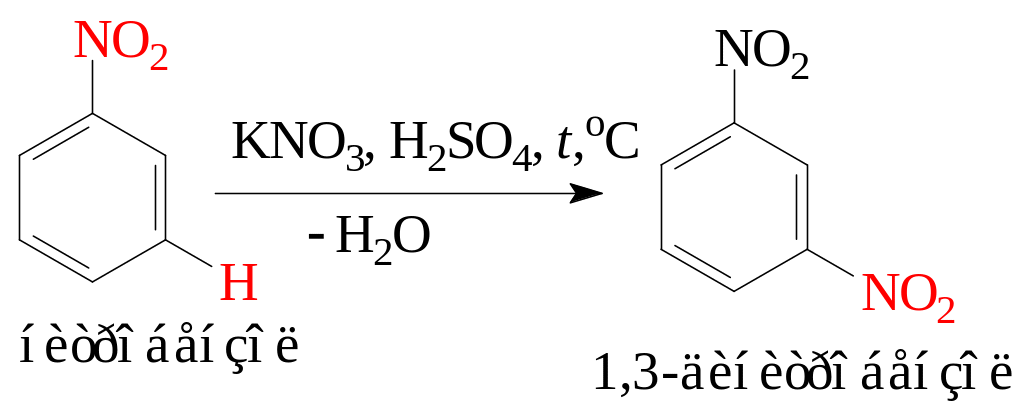- •Я. М. Каток, о. Я. Толкач органическая химия задачи и упражнения
- •Предисловие
- •1. Классификация и номенклатура органических соединений
- •Углеводороды и углеводородные радикалы (перечислены в порядке возрастания старшинства)
- •Примеры названий органических соединений
- •Примеры названий органических соединений
- •Индивидуальные задания Задача 1
- •Задача 2
- •2. Химическая связь
- •Индивидуальные задания Задача 3
- •Задача 4
- •3. Химическая реакция
- •Индивидуальные задания Задача 5
- •Задача 6
- •4. Алканы
- •Номенклатура
- •Примеры названий алканов по рациональной номенклатуре
- •Индивидуальные задания Задача 7
- •Задача 8
- •5. Непредельные углеводороды Номенклатура
- •Примеры названий непредельных соединений по рациональной номенклатуре
- •Примеры названий непредельных соединений
- •Индивидуальные задания Задача 9
- •Задача 10
- •Задача 11
- •Задача 12
- •Задача 13
- •Задача 14
- •Задача 15
- •Задача 16
- •6. Арены Номенклатура и изомерия замещенных бензола
- •Индивидуальные задания Задача 17
- •Задача 18
- •Задача 19
- •7. Галогенопроизводные углеводородов Номенклатура
- •Индивидуальные задания Задача 20
- •Задача 21
- •8. Спирты, фенолы, простые эфиры Классификация и номенклатура
- •Индивидуальные задания Задача 22
- •Задача 23
- •Задача 24
- •9. Альдегиды и кетоны Классификация и номенклатура
- •Индивидуальные задания Задача 25
- •Задача 26
- •10. Карбоновые кислоты и их производные Классификация и номенклатура
- •Примеры названий функциональных производных карбоновых кислот
- •Индивидуальные задания Задача 27
- •Задача 28
- •Задача 29
- •Задача 30
- •11. Углеводы
- •Номенклатура
- •Индивидуальные задания Задача 31
- •Задача 32
- •12. Нитросоединения Классификация и номенклатура
- •Индивидуальные задания Задача 33
- •13. Амины, аминокислоты и пептиды Классификация и номенклатура
- •Индивидуальные задания Задача 34
- •Задача 35
- •Задача 36
- •Задача 37
- •Задача 38
- •Литература
- •Оглавление
- •Органическая химия Задачи и упражнения
- •220006. Минск, Свердлова, 13а.
- •Пример решения задачи 1
- •Решение
- •Пример решения задачи 2
- •Решение
- •Пример решения задачи 3
- •Пример решения задачи 4
- •Решение
- •Пример решения задачи 5
- •Пример решения задачи 6
- •Пример решения задачи 7
- •Способы получения алканов
- •Решение
- •Пример решения задачи 8
- •Основные химические свойства алканов
- •Пример решения задачи 9
- •Способы получения алкенов
- •Решение
- •Пример решения задачи 10
- •Химические свойства алкенов
- •Решение
- •Пример решения задачи 11
- •Пример решения задачи 12
- •Химические свойства алкадиенов
- •Решение
- •Пример решения задачи 18
- •Способы получения аренов
- •Решение
- •Пример решения задачи 19
- •Пример решения задачи 20
- •Химические свойства галогенопроизводных углеводородов
- •Кислотно-основные свойства спиртов и фенолов
- •Реакции, иллюстрирующие кислотные свойства спиртов и фенолов
- •Решение
- •Пример решения задачи 23
- •Основные химические свойства спиртов, фенолов и простых эфиров
- •Решение
- •Пример решения задачи 24
- •Способы получения спиртов
- •Способы получения фенолов
- •Химические свойства карбонильных соединений
- •Решение
- •Пример решения задачи 26
- •Пример решения задачи 27
- •Решение
- •Пример решения задачи 28
- •Способы получения карбоновых кислот
- •Решение
- •Пример решения задачи 29
- •Пример решения задачи 30
- •Пример решения задачи 31
- •Моносахариды (монозы), классификация
- •Химические свойства моносахаридов
- •Решение
- •Пример решения задачи 32
- •Химические свойства дисахаридов
- •Решение
- •Пример решения задачи 34
- •Решение
- •Пример решения задачи 35 Основные химические свойства аминов
- •Химические свойства аминокислот
- •Качественные реакции на аминокислоты
- •Решение
- •Пример решения задачи 36 Решение
- •Пример решения задачи 37
- •Пример решения задачи 38
- •Решение
Пример решения задачи 32
I. Из двух моносахаридов, указанных в колонках А и Б (табл.), постройте восстанавливающий и невосстанавливающий дисахариды.
II. Приведите уравнения реакций:
– для невосстанавливающего дисахарида с (СH3)2CHI, Ag2O;
– восстанавливающего дисахарида с Cu(OH)2, t, С.
А |
Б |
|
|
Классификация, строение и номенклатура дисахаридов. Дисахариды природные вещества, которые при гидролизе распадаются на два моносахарида. Дисахариды образуются из двух молекул моносахаридов за счет отщепления молекулы Н2О. В образовании связи между моносахаридами принимают участие гликозидный гидроксил от одной молекулы, а от второй – гликозидный, или спиртовой (гликозный), гидроксилы.
Если в образовании дисахарида принимает участие гликозидный гидроксил одной монозы и спиртовой (гликозный) гидроксил второй, т. е. остатки моноз соединяются гликозил-гликозной (моногликозидной) связью, образуется восстанавливающий дисахарид. К таким дисахаридам относятся мальтоза, целлобиоза, лактоза. Например, мальтоза образуется из двух молекул α-глюкозы:
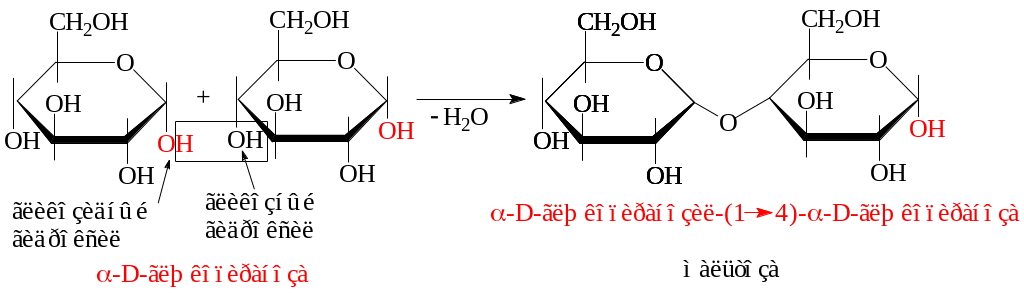
Целлобиоза из двух молекул β-глюкозы:
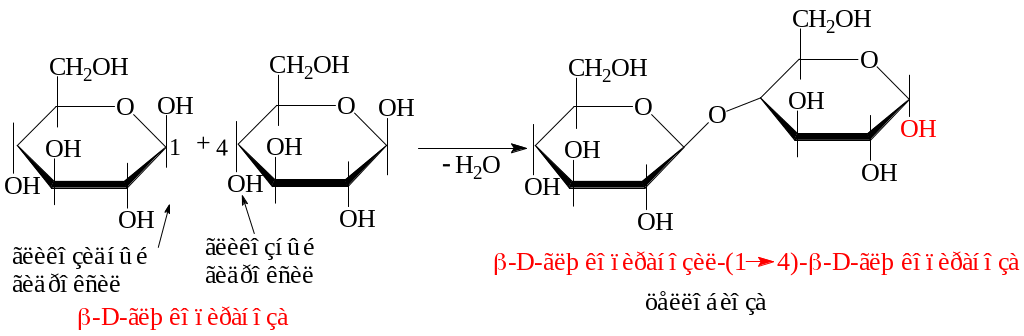
Лактоза образуется из b-галактозы и a-глюкозы.
Если в образовании дисахарида принимает участие гликозидный гидроксил одной монозы и гликозидный гидроксил второй, т. е. остатки моноз соединяются гликозил-гликозидной (дигликозидной) связью, образуется невосстанавливающий дисахарид. К таким дисахаридам относятся сахароза, трегалоза. Дисахарид сахароза образуется из α-глюкозы и β-фруктозы:
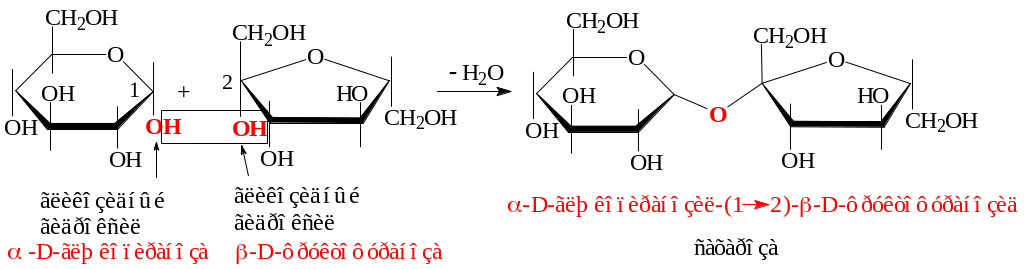
Дисахариды, как и моносахариды, называют в основном по тривиальной номенклатуре. Систематические названия дисахаридов образуют из названий моносахаридов: гликозил-гликозы (восстанавливающие) и гликозил-гликозиды (невосстанавливающие).
Химические свойства дисахаридов
Для дисахаридов характерны реакции с участием:
карбонильной группы;
спиртовых гидроксилов;
только полуацетального (гликозидного) гидроксила.
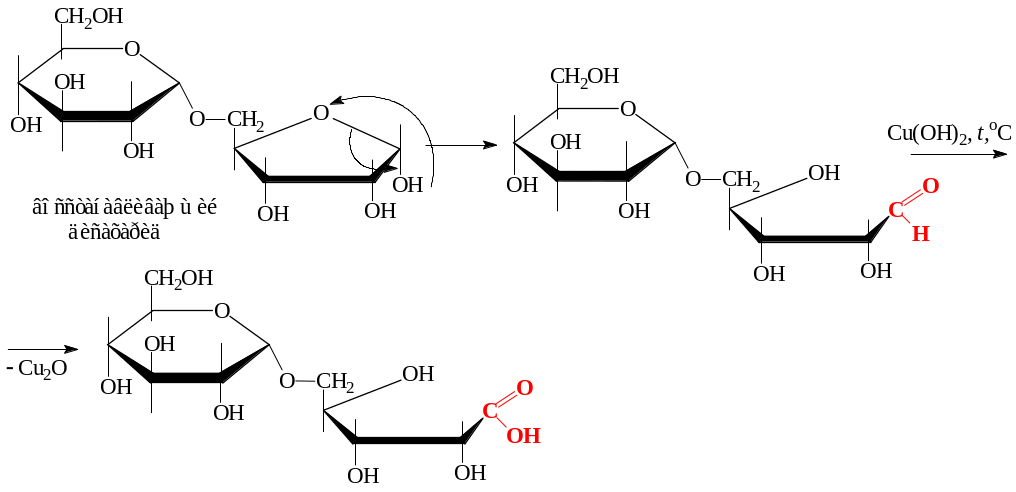
1. Реакции восстанавливающих дисахаридов. Восстанавливающие дисахариды содержат в молекуле полуацетальный (гликозидный) гидроксил OH, который позволяет циклической молекуле раскрываться с образованием альдегидной группы:
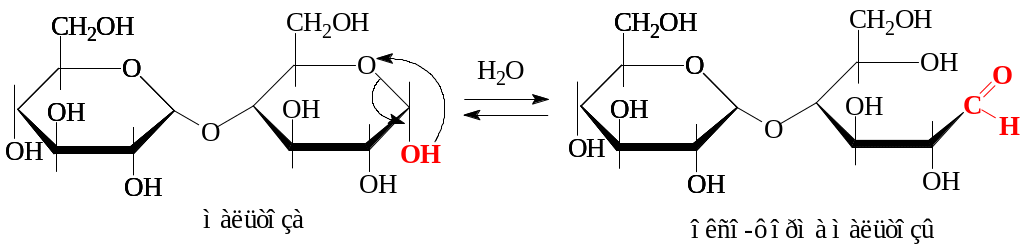
Для альдегидной группы дисахаридов, как и для моносахаридов, характерны следующие реакции:
а) восстановление меди и серебра из их оксидов:
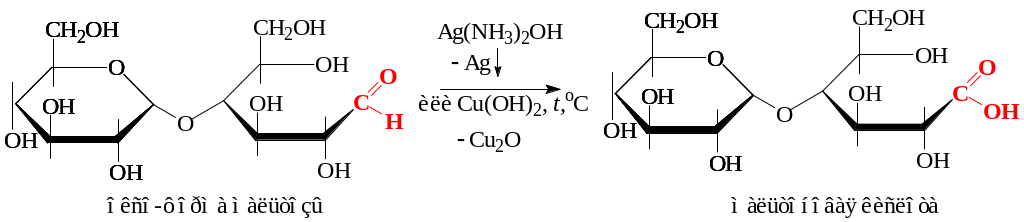
б) явление мутаротации:

в) с азотсодержащими нуклеофилами:
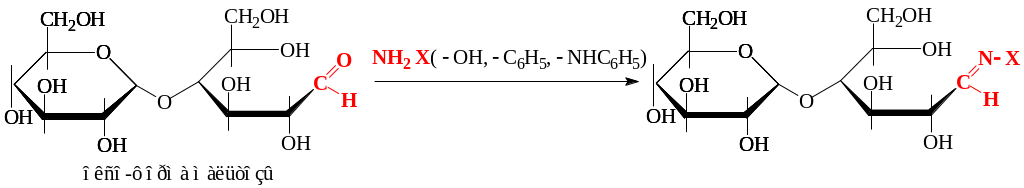
г) в реакциях алкилирования под действием спиртов (слабое алкилирующее средство) участвует только гликозидный гидроксил:
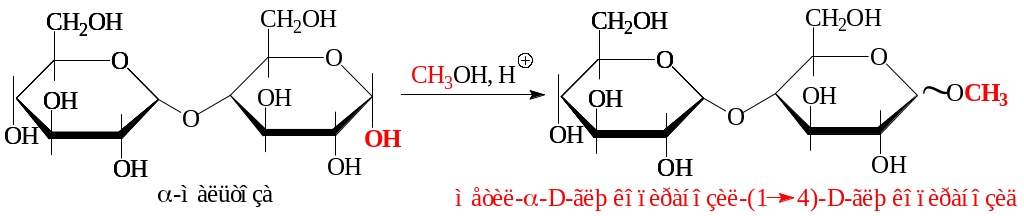
В реакциях алкилирования под действием галогеналканов (сильное алкилирующее средство) участвуют все гидроксилы:
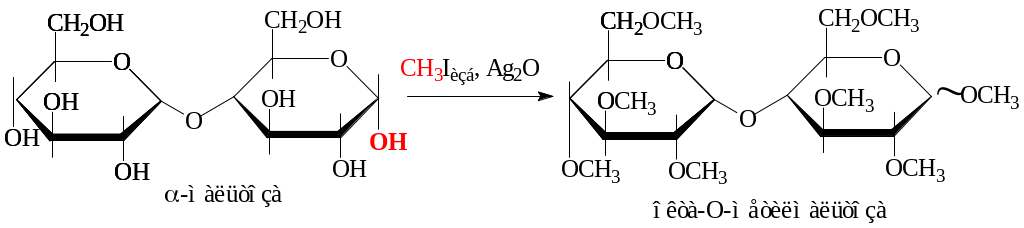
д) реакции ацилирования:
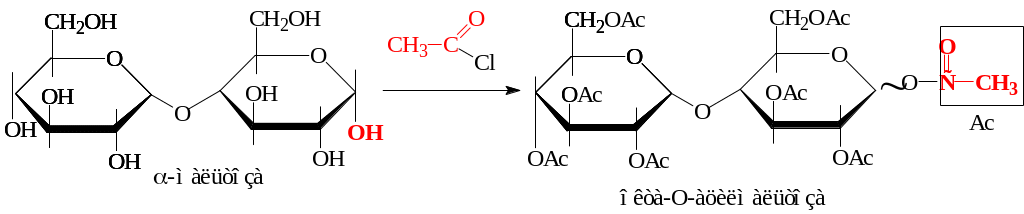
е) гидролиз до моносахаридов:
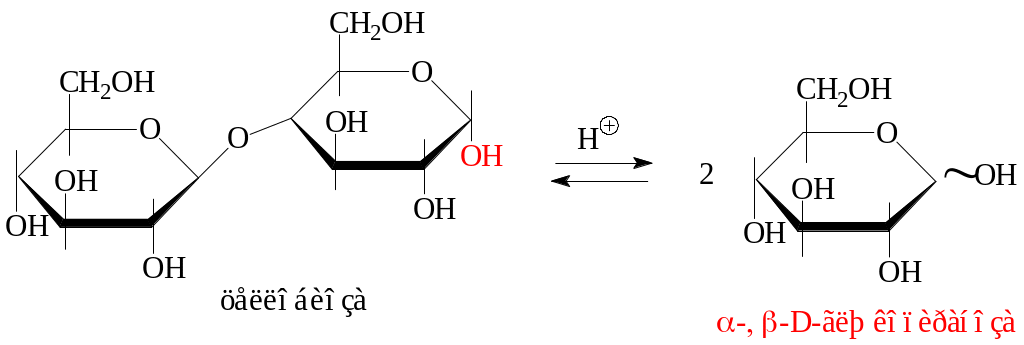
2. Реакции невосстанавливающих дисахаридов. Невосстанавливающие дисахариды не содержат в молекуле полуацетальный (гликозидный) гидроксил OH, поэтому не способны превращаться в оксо-форму с образованием альдегидной группы. Следовательно, для таких дисахаридов не характерны реакции по карбонильной группе: восстанавление меди и серебра из их оксидов; явление мутаротации; реакции с азотсодержащими нуклеофилами.
Такие углеводы реагируют по спиртовым группам OH с образованием простых и сложных эфиров:
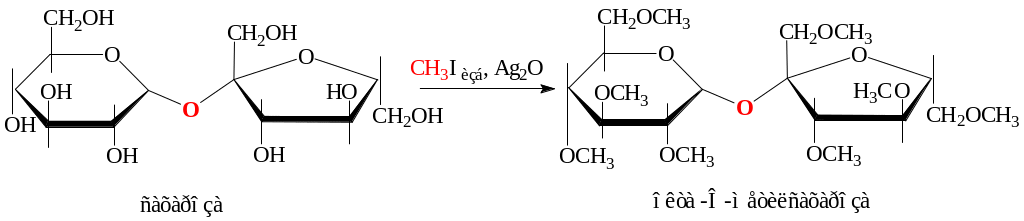

Решение
1. Из двух моносахаридов, указанных в колонках А и Б (табл.), строим восстанавливающий и невосстанавливающий дисахариды.
А |
Б |
|
|
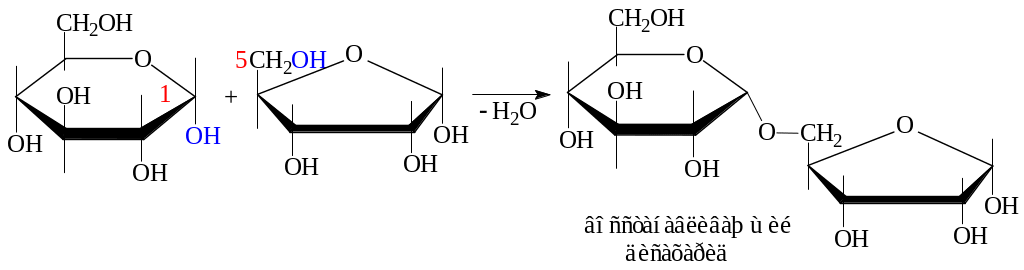

2. Приводим уравнения реакций:
а) для невосстанавливающего дисахарида с (СH3)2CHI, Ag2O;
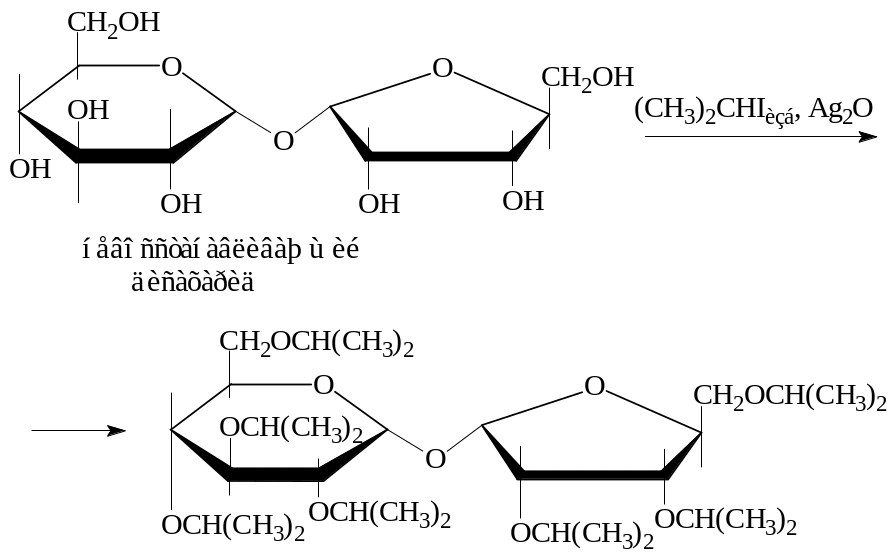
б) восстанавливающего дисахарида с Cu(OH)2, t, С.
Пример решения задачи 33
Приведите уравнение реакции получения бензилнитрометана из соответствующего углеводорода или галогенопроизводного углеводорода, укажите условия ее протекания. Напишите уравнения реакций данного соединения с реагентами NaOH, H2O; HNO2, назовите полученные продукты.
Нитросоединения
Нитросоединения производные углеводородов, в молекулах которых один или несколько атомов водорода замещены на нитрогруппу.
Способы получения нитросоединений
1. Нитрование алканов в условиях реакции Коновалова преимущественно идет по третичному или вторичному атому углерода с образованием продуктов мононитрования:
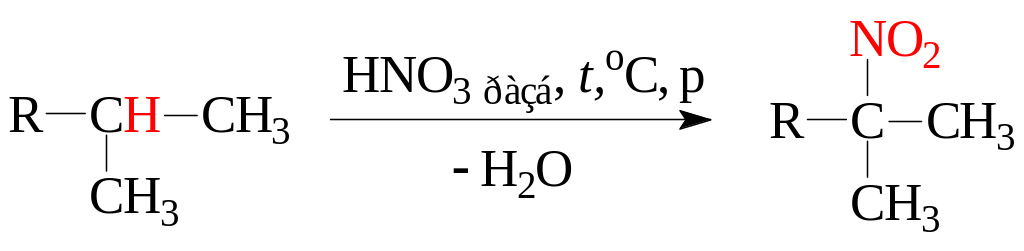
2. Нитрование аренов требует кислотного катализа:
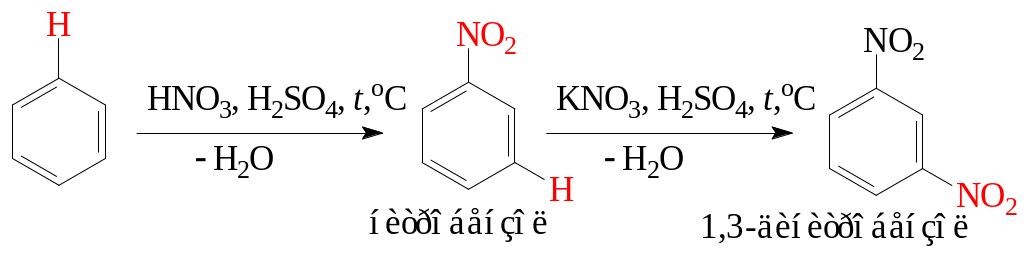
3. Нуклеофильное замещение галогена в галогенопроизводных углеводородов на нитрогруппу действием нитритов натрия или калия (алкилирование нитритов):

Химические свойства
1. Восстановление нитрогруппы.
Восстановление нитрогруппы в алифатических нитросоединениях приводит к образованию соответствующих аминов. В качестве восстановителей применяют гидриды металлов (LiAlH4, NaBH4); молекулярный водород (H2/Ni); водород, выделяющийся в реакции металлов (Fe, Zn, Sn) с кислотами:
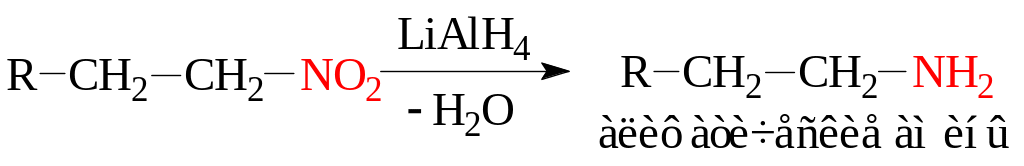
Восстановление нитрогруппы в ароматических нитросоединениях приводит к образованию ароматических аминов. В качестве восстановителей применяют каталитическое гидрирование водородом над катализаторами: H2, Ni(Pd, Pt); сульфид аммония (NH4)2S.
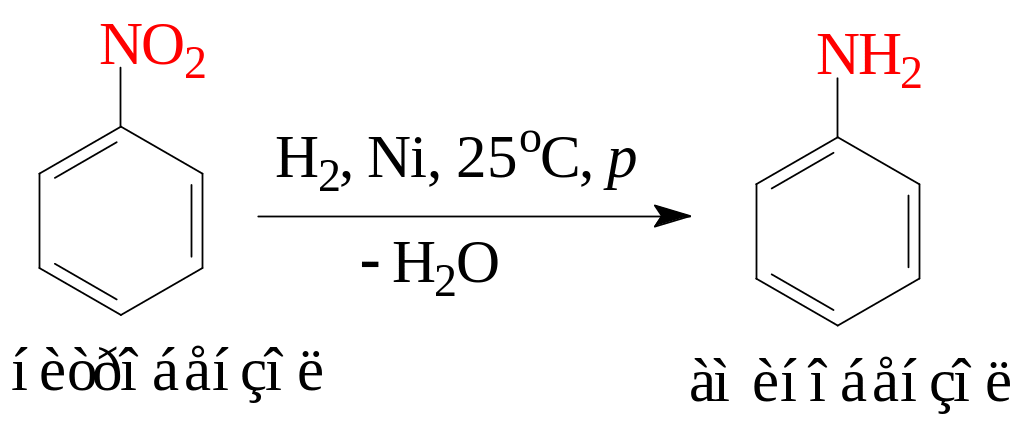
2. Реакции по α-углеродному атому:
а) реакции с основаниями. Первичные и вторичные алифатические нитросоединения характеризуются повышенной подвижностью водорода при α-углеродном атоме, связанном с нитрогрупой. Такая CH кислотность обусловлена высокой электроотрицательностью атома азота нитрогруппы. Под действием оснований происходит отщепление водорода и образование аци-нитроформы. Нитро- и аци-нитроформа являются изомерами - таутомерами, находящимися в состоянии динамического равновесия. Таким образом, первичные и вторичные нитросоединения медленно растворяются в щелочах с образованием солей аци-нитроформы.
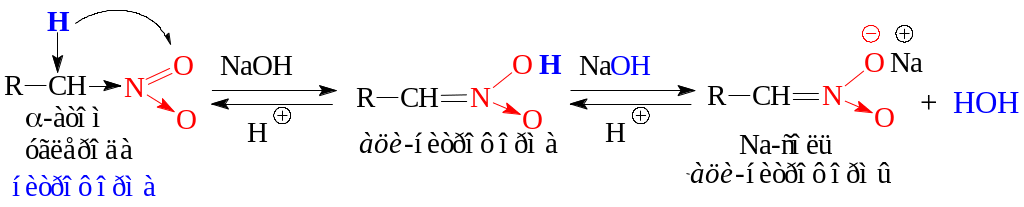
б) реакции с азотистой кислотой реакции нитрозирования. Первичные и вторичные алифатические нитросоединения реагируют с азотистой кислотой с образованием нитроловых кислот и псевдонитролов соответственно. В реакциях нитрозирования водород при α-углеродном атоме замещается на нитрозогруппу. Третичные нитросоединения в таких реакциях не участвуют, так как не содержат Н-атом у α-углеродного атома.
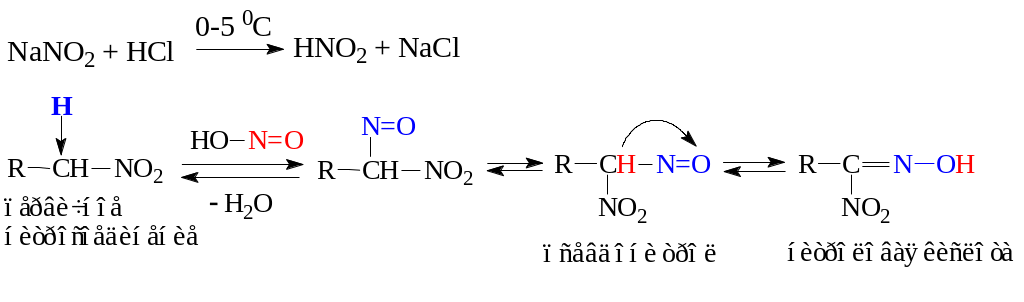

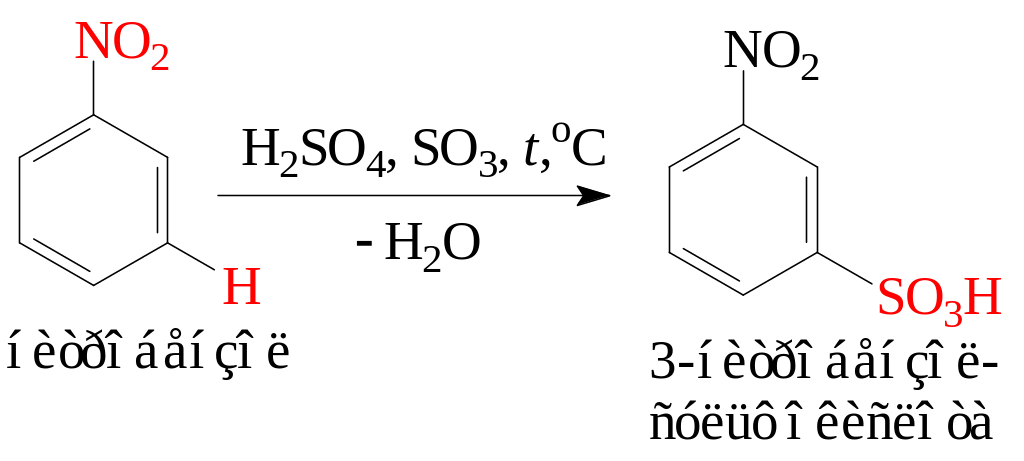
3. Реакции нитросоединений по ароматическому кольцу (реакции электрофильного замещения). Нитроарены в реакциях электрофильного замещения взаимодействуют только с сильными электрофильными реагентами при повышенных температурах. Нитрогруппа в аренах является заместителем II-рода, обладает электроноакцепторными свойствами и направляет замещение водорода на электрофил в мета-положение. Приводим реакции нитрования и сульфирования нитробензола: