- •Глава 8
- •8.1. Кристаллические и аморфные тела
- •8.2. Кристаллические структуры
- •8.3. Дефекты кристаллов
- •8.4. Механические свойства твердых тел
- •8.4.1. Деформация твердых тел
- •8.4.2. Прочность твердых тел
- •8.4.3. Распространение упругих волн в твердых телах
- •8.5. Тепловые свойства твердых тел
- •8.5.1. Тепловое расширение твердых тел
- •8.5.2. Теплоемкость твердых тел
- •8.6. Плавление и кристаллизация
- •8.7. Тройная точка. Полиморфные превращения
больше
разность
 и тем, следовательно, меньше критический
радиус зародыша, т.е. тем более мелкие
капли способны служить зародышами
жидкой фазы и тем, значит, скорее начнется
конденсация.
и тем, следовательно, меньше критический
радиус зародыша, т.е. тем более мелкие
капли способны служить зародышами
жидкой фазы и тем, значит, скорее начнется
конденсация.
Аналогично обстоит дело и в случае других фазовых переходов первого рода, например, в случае кипения жидкости; только теперь вместо капель жидкости необходимо рассматривать появление маленьких пузырьков газа в жидкости.
В заключение отметим, что фазовый переход первого рода и
механизм образования упорядоченных структур в открытых системах имеют много общего. Но если фазовый переход есть процесс равновесный, то образование диссипативных структур – неравновесный процесс. По этой причине образование диссипативных структур в неустойчивой открытой системе называют неравновесными (кинетическими) фазовыми переходами.
Глава 8
ТВЕРДЫЕ ТЕЛА
8.1. Кристаллические и аморфные тела
Твердыми телами обычно называют кристаллические тела или просто кристаллы. Кристаллы – это тела, обладающие упорядоченным периодически повторяющимся расположением образующих их частиц (атомов, молекул, ионов). Эти частицы называются структурными частицами. Структурной частицей, однако, может быть не просто одна частица, но и целая группа частиц (десятки, сотни и даже более). В этом случае кристалл называют молекулярным. В идеальном кристалле закономерное расположение частиц соблюдается не только вблизи каждой частицы, но и на сотнях тысяч или миллионах межатомных расстояний от нее. Поэтому говорят, что в кристаллах имеет место как ближний, так и дальний порядок в расположении частиц.
На рис. 8.1 представлена радиальная функция распределения
Рис. 8.1 |
Тела, сохраняющие порядок на больших расстояниях часто называют монокристаллами. Структура монокристалла представляет собой непрерывное повторение в трехмерном пространстве одинаковых структурных частиц. Реальные кристаллические тела обычно встречаются в виде поликристаллов. Поликристалл – это совокупность большого числа хаотически ориентированных мелких монокристаллов, называемых зернами или кристаллитами. Поликристаллами являются, например, все металлы.
К твердым телам иногда относят и аморфные тела. У аморфных тел, как и у жидкостей, отсутствует характерная для кристаллов
строгая упорядоченность в расположении частиц, периодически повторяющаяся во всех направлениях, т.е. у них отсутствует дальний порядок. Но у них, как и у жидкостей, существует определенная упорядоченность в расположении в пространстве соседних частиц, т.е. имеет место ближний порядок. С увеличением расстояния от данной частицы эта упорядоченность уменьшается и уже на расстоянии трех-четырех диаметров атома исчезает. Поэтому в аморфном теле вдоль различных направлений атомы в среднем располагаются с одинаковой плотностью, что и обусловливает для аморфных тел изотропию их физических свойств. Как видим, структура аморфных тел аналогична структуре жидкости. Поэтому их рассматривают как переохлажденные жидкости, вязкость которых такова, что вещество не является жидким в обычном смысле этого слова (не обладает текучестью).
Возможность
существования твердого кристаллического
состояния вещества обусловлена характером
сил взаимодействия между структурными
частицами. Зависимость cилы
f
взаимодействия между структурными
частицами твердого тела от расстояния
r
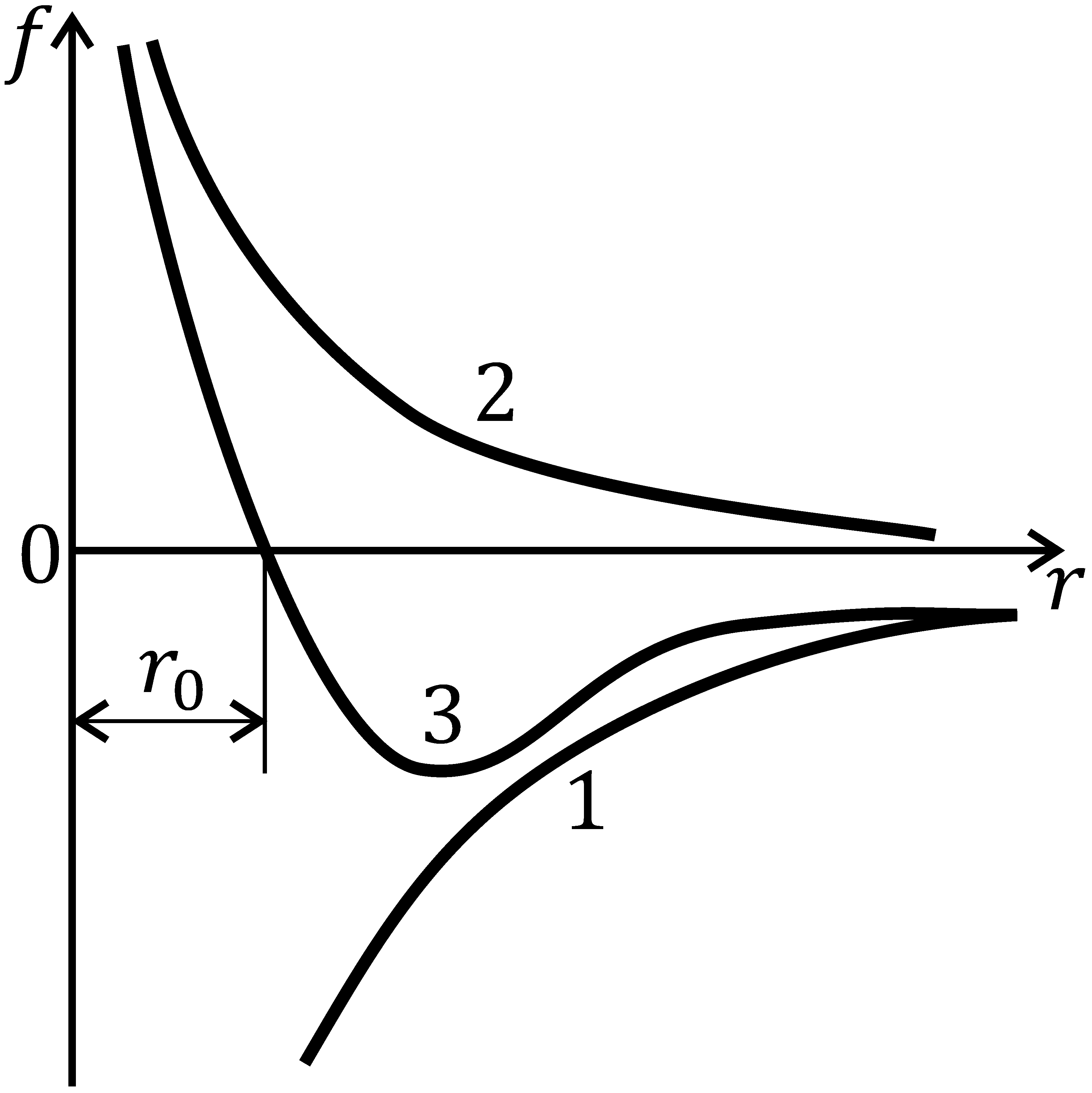
между ними показана на рис. 8.2. Зависимость
от расстояния r
энергии u
взаимодействия частиц. показана на рис.
8.3. Силы взаимодействия на относительно
больших (порядка двух-трех диаметров
частиц) расстояниях проявляют себя как
силы притяжения (кривая 1 на рис. 8.2), а
на малых (не более диаметра частицы) –
как силы отталкивания (кривая 2). На
расстоянии
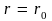 силы отталкивания уравновешиваются
силами притяжения, и результирующая
сила f
взаимодействия обращается в нуль (кривая
3). Энергия взаимодействия при этом
достигает минимального значения u0.
Природа сил притяжения между структурными
частицами может быть различной (она
зависит от природы структурных частиц),
но силы отталкивания имеют одинаковый
для всех тел характер и обусловлены в
основном принципом Паули. При сближении
частиц их электронные оболочки начнут
перекрываться. Это приводит к уменьшению
размеров области пространства, в которой
может двигаться электрон. Уменьшение
области пространства приводит к
уменьшению неопределенности координаты,
что в соответствии с соотношением
неопределенностей приводит к увеличению
неопределенности импульса, а значит, и
самого импульса, а с ним и кинетической
энергии электрона. Это проявляет себя
как действие сил отталкивания. Кро-
силы отталкивания уравновешиваются
силами притяжения, и результирующая
сила f
взаимодействия обращается в нуль (кривая
3). Энергия взаимодействия при этом
достигает минимального значения u0.
Природа сил притяжения между структурными
частицами может быть различной (она
зависит от природы структурных частиц),
но силы отталкивания имеют одинаковый
для всех тел характер и обусловлены в
основном принципом Паули. При сближении
частиц их электронные оболочки начнут
перекрываться. Это приводит к уменьшению
размеров области пространства, в которой
может двигаться электрон. Уменьшение
области пространства приводит к
уменьшению неопределенности координаты,
что в соответствии с соотношением
неопределенностей приводит к увеличению
неопределенности импульса, а значит, и
самого импульса, а с ним и кинетической
энергии электрона. Это проявляет себя
как действие сил отталкивания. Кро-
Рис. 8.2 |
Рис. 8.3 |
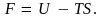
В
этом случае играет роль член
 и F будет
тем меньше, чем больше S,
т.е. чем менее упорядоченным будет
расположение частиц – строгий порядок
в расположении структурных частиц
нарушается.
и F будет
тем меньше, чем больше S,
т.е. чем менее упорядоченным будет
расположение частиц – строгий порядок
в расположении структурных частиц
нарушается.
Частицы
кристалла не могут свободно покидать
свои положения равновесия, так как при
смещении от этих положений энергия
частиц u
увеличивается и появляются силы
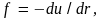 стремящиеся вернуть их в положение
равновесия. Поступательное движение
частиц оказывается невозможным.
Единственной доступной формой теплового
движения частиц является беспорядочные
колебания около положений равновесия.
стремящиеся вернуть их в положение
равновесия. Поступательное движение
частиц оказывается невозможным.
Единственной доступной формой теплового
движения частиц является беспорядочные
колебания около положений равновесия.
Кристаллическое
состояние может существовать только
при относительно низких температурах,
при которых средняя энергия теплового
движения будет оставаться ниже их
энергии связи
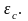 Энергия связи - это положительная
разность между энергией изолированных
частиц
Энергия связи - это положительная
разность между энергией изолированных
частиц
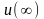 и минимальной энергией частиц в кристалле
и минимальной энергией частиц в кристалле
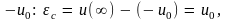 так
как
так
как
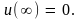 Она определяет работу, необходимую для
удаления частицы из кристалла. Механизм
перехода вещества в кристаллическое
состояние следующий. При понижении
температуры вещества уменьшается
энергия теплового движения его частиц.
При некоторой температуре кинетическая
энергия частиц оказывается недостаточной
для преодоления действия сил притяжения
между ними. Частица переходит в режим
тепловых колебаний около определенных
положений равновесия, отвечающих
минимуму потенциальной энергии
взаимодействия. Наоборот, при нагревании
тела до температуры, при которой энергия
теплового движения частиц становится
сравнимой или превышает энергию связи,
кристалл разрушается – тело переходит
в жидкое состояние.
Она определяет работу, необходимую для
удаления частицы из кристалла. Механизм
перехода вещества в кристаллическое
состояние следующий. При понижении
температуры вещества уменьшается
энергия теплового движения его частиц.
При некоторой температуре кинетическая
энергия частиц оказывается недостаточной
для преодоления действия сил притяжения
между ними. Частица переходит в режим
тепловых колебаний около определенных
положений равновесия, отвечающих
минимуму потенциальной энергии
взаимодействия. Наоборот, при нагревании
тела до температуры, при которой энергия
теплового движения частиц становится
сравнимой или превышает энергию связи,
кристалл разрушается – тело переходит
в жидкое состояние.
В зависимости от того, из каких структурных частиц состоит твердое тело, и в зависимости от характера сил взаимодействия между частицами все кристаллы можно разделить на четыре группы: ионные, атомные, металлические и молекулярные.
Вследствие наличия дальнего порядка в расположении частиц в кристалле расстояние между двумя соседними частицами для разных направлений различно. Иначе говоря, в кристалле вдоль различных направлений частицы размещаются с разной плотностью. Это приводит к анизотропии физических свойств кристаллов. Механические, тепловые, электрические и другие свойства кристаллов оказываются неодинаковыми по разным направлениям. Поликристаллические тела как целое ввиду беспорядочной ориентации зерен обладают изотропией своих физических свойств, и анизотропия имеет место только в пределах каждого отдельно взятого зерна. Изотропны и аморфные тела, так как в них вдоль различных направлений частицы размещаются с одинаковой плотностью.