
- •Металлургия цветных металлов. Комков Алексей Александрович (тел. 236-10-01).
- •Общие вопросы металлургии.
- •Металлы и их классификация.
- •Цветные металлы
- •Классификация металлургических процессов.
- •Пирометаллургические процессы.
- •Плавка.
- •Дистилляция.
- •Гидрометаллургические процессы.
- •Металлургия меди.
- •Традиционные процессы плавки.
- •1. Отражательная плавка.
- •Окислительный обжиг.
- •2. Рудотермическая электроплавка.
- •Автогенные процессы плавки.
- •Плавка во взвешенном состоянии (пвп)
- •Кислородно-факельная плавка (кфп)
- •Характеристики процессов.
- •Особенности технико-экономических показателей с физико-химическими условиями и конструкцией аппарата.
- •3 Стадии превращений:
- •Конвертирование медных штейнов.
- •Периодическое конвертирование медных штейнов в горизонтальных конверторах Пирс-Смитта.
- •2 Основных периода:
- •Первый период конвертирования:
- •Второй период конвертирования:
- •Рафинирование черновой меди.
- •Окислительное (анодное, огненное (высок. T)) рафинирование.
- •Электролиз.
- •Электролизная ванна:
- •Основные технико-экономические показатели при электролизе.
- •Производство никеля из окисленных никелевых руд.
- •Получение Ni из окисленных Cu-Ni руд.
- •Конвертирование.
- •Разделение файнштейна.
- •Традиционная схема обогащния.
- •Плавка на штейн.
- •Получение никеля из сульфидных руд.
Основные технико-экономические показатели при электролизе.
25-40% стоимости всех затрат – затраты на электроэнергию.
Стремятся снизить затраты на электроэнергию: потери в системе, в токопроводящей системе.
проводимость (сопротивление электролита)
Основные факторы, влияющие на сопротивление электролита:
Температура – чем выше, тем ниже сопротивление ниже затраты;
Состав электролита (tоптим электролита = 65 С
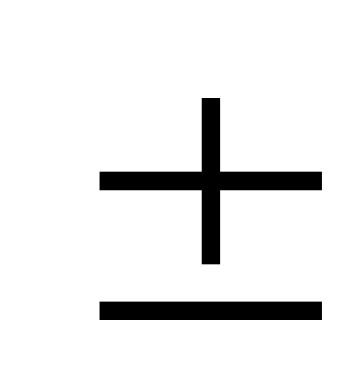 5 С).
5 С).
Выше 75 С температуру не делают, это связанно с санитарными условиями работы в электролизном цехе.
Состав электролита.
концентрации H2SO4 сопротивление электролита, из-за большого количества подвижных ионов водорода.
Побочные явления при повышении концентрации H2SO4:
содержания катионов меди вероятности разрядки примеси на катоде.
Cu2+
+ SO![]() = CuSO4
= CuSO4
Опытным путем определена оптимальная концентрация H2SO4 = 120-200 г. H2SO4 на литр раствора.
Величина силы тока или катодная плотность тока.
Чем выше катодная плотность тока, тем выше производительность, меньше себестоимость.
Но по мере повышения катодной плотности тока:
затраты электроэнергии, удельных затрат;
Катионы двигаются внутри более быстро, больше загрязнения в единицу времени, электролит нужно быстрее выводить.
Взмучивание частиц загрязнение меди, качества меди.
В результате, себестоимость на заводах:
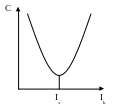
На каждом заводе существует экономическая плотность тока, снижающая себестоимость.
250-300А на м2 на наших заводах.
300-350А на м2 на западе.
Выход по току.
Характеризует эффективность использования электроэнергии.
Выход по току – отношение выделившейся Cu на катоде к количеству Cu, которое должно выделиться теоретически.
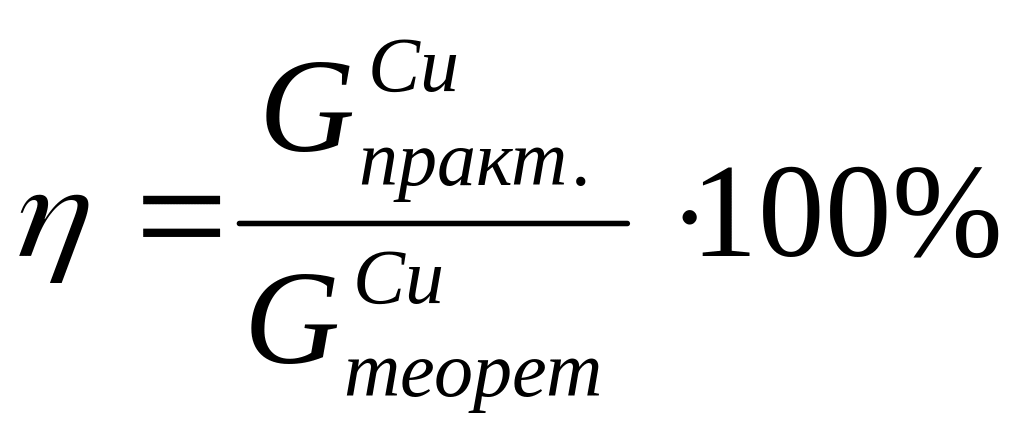
![]() – по закону Фарадея.
– по закону Фарадея.
I – сила тока,
![]() – время, q – электрохимический
эквивалент.
– время, q – электрохимический
эквивалент.
![]()
![]() по закону не равен 100%.
по закону не равен 100%.
на западе 95-96%.
в России 92-95%.
Основные причины потерь электроэнергии – организационные, утечка энергии из-за прочих контактов.
Производство никеля из окисленных никелевых руд.
В мире в год производится 1 млн. никеля.
Область применения: жаропрочная, конструкционная сталь, производство ферросплавов.
Ni дает жаропрочность, кислостойкость. Ni используется в декоративной отделке, никелирование (17% Ni).
Используется в медных расплавах для изготовления монет.
Свойства Ni:
tплавл. = 1450 С.
При высоких температурах хорошо окисляется и образует NiO, Ni2O3.
NiS – неустойчивое соединение, при высоких температурах разлагается.
Ni3S2 – низкоплавкий (tплавл. = 780 С.)
Сырье для производства никеля:
Производится из сульфидных (40%) и окисленных руд (60%) в сопоставимых количествах (40%).
В России никель производится в основном из сульфидных Cu-Ni руд (“Норильский никель”).
На Урале перерабатывают окисленные Cu-Ni руды (Орский, Режский, Уфалийский заводы).
Получение Ni из окисленных Cu-Ni руд.
Окисленные Cu-Ni руды в зависимости от того, концентрация какого оксида высока в этих рудах подразделяются на:
Железистые;
Кремнистые;
Магнезиальные.
В рудах никель присутствует в виде закиси NiO, однако не чистый, а в форме более сложных соединений: силикат, магнезитовый силикат.
Окисленные руды очень трудно обогащать из-за из разброса.
Во всем мире окисленные руды плавятся без обогащения.
Российские никелевые руды – кремнистые.
Содержание кремнезема:
SiO2 = 30-45%;
MgO до 20%;
Fe = 20%;
Ni в форме силиката Ni » 1%.
В России бедные окисленные никелевые руды.
Рентабельность min 0,6-0,7 в РФ.
В мире более богатые руды – 1,5% Ni.
Богатый Cu концентрат:
69-73% Cu;
5% Ni;
22-23% S;
золото, серебро…
Богатый Ni концентрат:
68-73% Ni;
3-4% Cu;
2-3,5% Fe
1.2% Co;
платиноиды
Из Cu концентрата варят черновую медь, ее получают с примесью Ni. Его удаляют из черновой меди продувая ее после варки, окисляя Ni.
В этом шлаке до 20% Ni и до 20% Cu. Из этого шлака сливают черновую медь, а шлак вываливают в твердом виде из конвертора Þ направляют в качестве холодных оборотов в конвертор.
Ni концентрат: 2-3,5% Fe. его обжигают в печи КС, но в первую стадию, т.к. в этой схеме нет необходимости удалять из Ni серу. Поэтому сразу в КС получают закись Ni с серой 1,5%, t = 1100-1200° С.
Далее закись Ni поступает на восстановительную плавку в электродуговых печах. Известковый шлак не доводят т. к. нет смысла глубокой очистки от серы. Требования к восстановителю не жесткие.
Разливают Ni не в виде гранул, а в виде слитков – анодов, на карусельной машине. Эти аноды идут на электролитическое рафинирование Ni.
Цель – получить из огневого Ni – Ni высокой чистоты марок N0 и N1 и получить благородные металлы и Co. В N0 до 17 элементов. Попутно извлекается и Cu в отдельный продукт.
Анодный Ni по составу:
89-92% Ni;
5% Cu;
2-4% Fe;
1-2% Co.
Электролиз Ni проводится в электролизных ванных ящичного типа.
Отличия электролиза Ni обусловлены активностью Ni. Ni близки Co, Fe, Zn Þ при электролизе на катоде они могут вместе с Ni и Cu, H.
Что бы получить на катоде только Ni необходимо соблюдать требования:
Тщательно контролировать состав и температуру электролита. Электролит, находящийся около катода, должен быть тщательно очищен от примесей.
Надо разделить прианодное и прикатодное пространство перегородкой.
Циркуляция электролита.
В Ni электролизе электролит, который получается в прианодном пространстве выводится на очистку от Ni, Cu, Co. Только после очистки электролит заливают в прианодное пространство.
