
- •Введение
- •Обработка результатов физико-химических измерений Погрешность измерений
- •Выражение результатов измерений и расчетов
- •Термохимия Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 1. Определение интегральной теплоты растворения соли и теплоты гидратообразования
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 2. Определение энтальпии диссоциации слабого электролита
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 3 Определение изменения энтальпии реакции нейтрализации
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Коллигативные свойства растворов Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 4. Криометрия
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Фазовые равновесия в однокомпонентных системах Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа №5. Давление насыщенного пара
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка экспериментальных данных
- •Содержание отчета по лабораторной работе
- •Фазовые равновесия в двухкомпонентных системах Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа №6. Получение кривой разгонки
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка экспериментальных данных
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 7. Получение диаграммы состояния двухкомпонентной неконденсированной системы
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка экспериментальных данных
- •Содержание отчета по лабораторной работе
- •Распределение вещества в двухфазной системе. Экстракция Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 9. Экстракция цветных металлов нафтеновой кислотой
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Электропроводность растворов электролитов Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 10. Определение степени диссоциации слабого электролита кондуктометрическим способом
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка экспериментальных данных
- •Содержание отчета по лабораторной работе
- •Лабораторная работа №11. Определение чисел переноса ионов
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Термодинамика электрохимических систем Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 12. Определение стандартных электродных потенциалов
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 13. Определение коэффициента активности электролита
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Ионометрия и рН-метрия Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 14. Определение константы диссоциации слабого электролита потенциометрическим методом
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка экспериментальных данных
- •Содержание отчета по лабораторной работе
- •Строение вещества. Молекулярные спектры Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 15. Определение константы нестойкости тиоцианата (роданида) железа фотометрическим методом
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Химическая кинетика Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 16. Определение константы скорости реакции окисления иодида калия персульфатом аммония
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 17. Исследование кинетики омыления сложного эфира
- •Молекулярная адсорбция
- •Адсорбция на поверхности раздела жидкость – газ
- •Адсорбция на поверхности твердого тела
- •Ионообменная адсорбция
- •Контрольные вопросы
- •Лабораторная работа № 18. Исследование поверхности раздела фаз: раствор пав - воздух
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка экспериментальных данных
- •Лабораторная работа № 19. Исследование молекулярной адсорбции растворенного вещества из растворов на активированном угле
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 20. Исследование обменной адсорбции ионов
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 21. Исследование кинетики ионообменной адсорбции
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа №22. Разделение меди и цинка на катионите
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Устойчивость дисперсных систем Краткие теоретические сведения
- •Контрольные вопросы
- •Лабораторная работа № 23. Получение лиофобных золей
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 24. Определение порога коагуляции визуальным методом
- •Выполнение работы
- •I. Приблизительное определение порога коагуляции
- •Содержание протокола лабораторной работы
- •II. Уточнение значения порога коагуляции
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 25. Изучение коагуляции гидрозоля железа
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 26. Определение размеров частиц дисперсных систем турбидиметрическим методом Краткие теоретические сведения
- •Контрольные вопросы
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Содержание
Выполнение работы
1. Приготовить 5 растворов ПАВ, заданного преподавателем:
в 4 колбы мерной пипеткой отобрать дистиллированной воды;
в химический стакан объемом 100 мл отлить некоторое количество раствора ПАВ, заданного преподавателем;
в колбу № 1 мерной пипеткой отобрать 20 мл исходного раствора ПАВ и перемешивают;
отобрать из колбы № 1 20 мл раствора ПАВ, перенести в колбу № 2, перемешать;
отобрать из колбы № 2 20 мл раствора ПАВ, перенести в колбу № 3, перемешать;
отобрать из колбы № 3 20 мл раствора ПАВ, перенести в колбу № 4, перемешать;
Таким образом в наличии 5 растворов ПАВ: стакан с исходным раствором и 4 колбы, в которых концентрация уменьшается в 2 раза.
2. Определить водяное число сталагмометра N0:
отобрать порцию воды в прибор;
сосчитать сколько капель прокапает при движении мениска жидкости от верхней риски до нижней.
Повторить 2-3 раза.
3. Определить количество капель N для каждого раствора, начиная с самого разбавленного. Каждый опыт повторить 2-3 раза.
Содержание протокола лабораторной работы
1. Наименование ПАВ и его химическая формула
2. Концентрация раствора ПАВ
3. Таблица экспериментальных данных
№ |
Проба |
Число капель |
||
N1 |
N2 |
Nсреднее |
||
1 |
Н2О |
|
|
|
2 |
С/16 |
|
|
|
3 |
С/8 |
|
|
|
4 |
С/4 |
|
|
|
5 |
С/2 |
|
|
|
6 |
С |
|
|
|
Обработка экспериментальных данных
1. Вычислить для каждого опыта величину поверхностного натяжения по уравнению:
![]() ,
,
где 0 и d0 – поверхностное натяжение и плотность чистой воды – взять из приводимой ниже таблицы; N0 – водяное число сталагмометра; d и N – плотность и число капель исследуемого раствора ПАВ.
Плотность и поверхностное натяжение воды
Т, K |
0103, Дж/м2 |
d0103, кг/м3 |
Т, K |
0103, Дж/м2 |
d0103, кг/м3 |
287 |
73,64 |
0,9993 |
293 |
72,75 |
0,9982 |
288 |
73,40 |
0,9991 |
294 |
72,59 |
0,9980 |
289 |
73,34 |
0,999 |
295 |
72,44 |
0,9978 |
290 |
73,19 |
0,9988 |
296 |
72,28 |
0,9976 |
291 |
73,05 |
0,9984 |
297 |
72,18 |
0,9973 |
292 |
72,90 |
0,9983 |
298 |
71,97 |
0,9971 |
и определить среднее значение поверхностного натяжения
2. Полученные результаты занести в таблицу:
№ |
С103, моль/м3 |
1103, Дж/м2 |
2103, Дж/м2 |
ср103, Дж/м2 |
0 |
|
|
|
0 |
1 |
|
|
|
…. |
2 |
|
|
|
|
3. Построить график изотермы поверхностного натяжения ср = f(С).

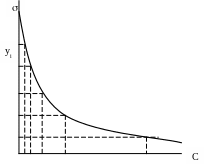
Рис. 15. Изотерма поверхностного натяжения.
4. Определить постоянные уравнения Шишковского:
= 0 i = aln(bCi +1).
= Разделить график, начиная с 0 по оси ординат на 4-5 равных участка.
= Определить по графику концентрации ПАВ, соответствующие выбранным значениям .
= Вычислить значения K как минимум для трех выбранных точек n по уравнению:
![]()
и найти Kср.
= Рассчитать постоянную а уравнения Шишковского (характеризует предельную адсорбцию ПАВ на поверхности):
![]() .
.
= Вычислить постоянную b (характеризует адсорбционную способность вещества в разбавленных растворах) для каждой концентрации (определенной графически)
![]()
и взять среднее арифметическое значение.
5. Определить значения удельной адсорбции Гn для всех концентраций раствора.
= Для значений концентрации ПАВ провести касательные к зависимости σcp = f(С) до пересечения в осью ординат и найти величину yn (см. рис. 1)
= Рассчитать значения Гn
по уравнению:
![]()
Результаты занести в таблицу:
№ |
С103, моль/л |
ср103, Дж/м2 |
Г, моль/м2 |
yn/Cn, Дж/моль |
|
|
|
|
|
6. Построить изотерму адсорбции в координатах Г = f(C) и определить графически предельное значение удельной адсорбции Г∞
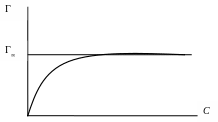
Рис. 16. Изотерма адсорбции Гиббса
7. Рассчитать площадь, занимаемую
одной молекулой ПАВ по уравнению:
![]()
8. Рассчитать длину молекулы
по уравнению:
![]() ,
,
где М – молярная масса ПАВ, г/моль.
Плотности ПАВ
-
ПАВ
d103, кг/м3
Амиловый спирт
0,8144
Изоамиловый спирт
0,8120
Бутиловый спирт
0,8078
Изобутиловый спирт
0,8030
Пропиловый спирт
0,8035
Изопропиловый спирт
0,7855

Рис. 17. График для определения плотности раствора ПАВ (на примере амилового спирта)
