
- •Введение
- •4.3. Титриметрический метод анализа
- •4.3.1. Классификация методов титриметрического анализа
- •4.3.2. Стандартизация раствора титранта
- •4.3.3. Кривые титрования
- •4.3.3. Индикаторы титриметриметрических методов анализа
- •4.3.4. Принцип эквивалентности
- •4.3.5. Расчет результата прямого титрования при разных способах выражения концентрации раствора
- •4.3.6. Расчет результата в методе обратного титрования
- •4.4 Кислотно-основное титрование.
- •4.4.1.Общая характеристика метода
- •4.4.2 Индикаторы в методе кислотно-основного титрования
- •4.4.3. Кривые титрования
- •4.4.4 Кривая титрования сильной кислоты сильным основанием ( и наоборот)
- •Расчет кривой титрования 10,0 мл 0,1 м hCl раствором 0,1 м NaOh
- •Титрование сильного основания сильной кислотой
- •Расчет кривой титрования 10,0 мл 0,1 м сh3cooh раствором 0,1 м NaOh
- •4.4.5. Техника выполнения работ в титриметрических методах анализа
- •3. Стандартизация раствора хлороводородной кислоты по тетраборату натрия.
- •4. Определение содержания щёлочи в растворе
- •Контрольные вопросы :
- •Задачи для самостоятельного решения
- •5. Окислительно-восстановительное титрование .
- •5.1.Классификация методов окислительно-восстановительного титрования
- •5.2. Индикаторы окислительно-восстановительного титрования
- •5.3.Перманганатометрия
- •1. Приготовление раствора титранта кМnO4
- •2. Приготовление раствора первичного стандарта
- •3. Стандартизация раствора титранта кМnO4
- •4. Вычисления
- •5) Определение железа (II)
- •6. Физико - химические методы анализа.
- •Определение концентрации ионов меди в растворе
- •4. Определение меди в исследуемом растворе
- •1. Основные понятия аналитической химии
- •2. Методы качественного анализа
- •3. Классификация катионов в качественном кислотно-основном
- •4. Методы количественного анализа
- •4.3. Титриметрический метод анализа
- •4.4 Кислотно-основное титрование.
- •5. Окислительно-восстановительное титрование .
- •6. Физико - химические методы анализа.
- •4.3. Титриметрический метод анализа
- •4.3.1. Классификация методов титриметрического анализа
- •4.3.2. Стандартизация раствора титранта
- •4.3.3. Кривые титрования
- •4.3.3. Индикаторы титриметриметрических методов анализа
- •4.3.4. Принцип эквивалентности
- •4.3.5. Расчет результата прямого титрования при разных способах выражения концентрации раствора
- •4.3.6. Расчет результата в методе обратного титрования
- •4.4 Кислотно-основное титрование.
- •4.4.1.Общая характеристика метода
- •4.4.2 Индикаторы в методе кислотно-основного титрования
- •4.4.3. Кривые титрования
- •4.4.4 Кривая титрования сильной кислоты сильным основанием ( и наоборот)
- •Расчет кривой титрования 10,0 мл 0,1 м hCl раствором 0,1 м NaOh
- •Титрование сильного основания сильной кислотой
- •Расчет кривой титрования 10,0 мл 0,1 м сh3cooh раствором 0,1 м NaOh
- •4.4.5. Техника выполнения работ в титриметрических методах анализа
- •3. Стандартизация раствора хлороводородной кислоты по тетраборату натрия.
- •4. Определение содержания щёлочи в растворе
- •Контрольные вопросы :
- •Задачи для самостоятельного решения
- •5. Окислительно-восстановительное титрование .
- •5.1.Классификация методов окислительно-восстановительного титрования
- •5.2. Индикаторы окислительно-восстановительного титрования
- •5.3.Перманганатометрия
- •1. Приготовление раствора титранта кМnO4
- •2. Приготовление раствора первичного стандарта
- •3. Стандартизация раствора титранта кМnO4
- •4. Вычисления
- •5) Определение железа (II)
- •6. Физико - химические методы анализа.
- •Определение концентрации ионов меди в растворе
- •4. Определение меди в исследуемом растворе
- •1. Основные понятия аналитической химии
- •2. Методы качественного анализа
- •3. Классификация катионов в качественном кислотно-основном
- •4. Методы количественного анализа
- •4.3. Титриметрический метод анализа
- •4.4 Кислотно-основное титрование.
- •5. Окислительно-восстановительное титрование .
- •6. Физико - химические методы анализа.
3. Стандартизация раствора хлороводородной кислоты по тетраборату натрия.
1. Заполнить бюретку приготовленной соляной кислотой. Для этого чистую бюретку сполоснуть приготовленным раствором HCl и заполнить носик бюретки сплошным столбом раствора удалив пузырьки воздуха, и проверить при этом действие шарикового затвора – не пропускает ли он раствор. Налить раствор кислоты через воронку выше нулевой отметки (воронку при этом приподнять для свободного выхода воздуха), убрать воронку и установить уровень кислоты на нулевом делении по нижнему мениску, выливая лишнюю кислоту через носик бюретки.
2. Чистую пипетку вместимостью 10мл ополоснуть раствором буры. Затем в две конические колбы для титрования отмерить этой пипеткой аликвотные части раствора буры (Vб=10мл). Для этого из мерной колбы раствор буры перенести в стаканчик, предварительно сполоснув этим раствором.
3. В каждую колбу добавить по 1-2 капле метилоранжа и титровать до перехода окраски индикатора из жёлтой в оранжевую (малиновую), записывая каждый раз объём израсходованной кислоты по бюретке и доливая её до «0».
4. Объёмы двух параллельных определений V1 и V2 не должны отличаться друг от друга более чем на 0,20мл в противном случае нужно провести ещё одно титрование. Из двух определений рассчитать средний арифметический Vк.

5. Рассчитать с точностью до четвёртой значащей цифры концентрацию кислоты по формуле:
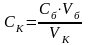
6. Полученный результат показать преподавателю и получить контрольную задачу у лаборанта.
4. Определение содержания щёлочи в растворе
1. Заполнить бюретку рабочим раствором хлороводородной кислоты (Ск).
2. Получить у лаборанта мерную колбу (Vм.к.) с неизвестным объёмом раствора щёлочи, довести его до метки дистиллированной водой, тщательно перемешать.
3. Взять пипеткой (Vпип=10 мл) аликвоту раствора щёлочи в две колбочки для титрования, добавить в каждую порцию по 1-2 капли метилоранжа и титровать кислотой до перехода жёлтой окраски в оранжевую (малиновую).
4. Объёмы параллельных титрований не должны отличаться друг от друга более чем на 0,20мл. Затем из полученных объёмов рассчитать средний арифметический (Vк).
5. Рассчитать с точностью до четвёртой значащей цифры массу щёлочи (m, мг) по формуле:

где Мэ (щёлочи) – молярная масса эквивалента щёлочи.
6. Показать преподавателю выполненную работу, получить у него правильный результат (mпр) и рассчитать относительную погрешность по формуле:

Погрешность анализа не должна превышать ± 2%. Если она больше 2%, то надо проанализировать выполнение работы и по указанию преподавателя повторить её.
В ходе всей работы аккуратно вести записи в лабораторном журнале.
Контрольные вопросы :
Что называется эквивалентом вещества?Как определяется эквивалент в реакциях кислотно-основного титрования?
Какие вещества и почему могут быть использованы в качестве стандартных для установления точной концентрации кислоты?
Что такое титрованный раствор? Какие концентрации рабочих растворов обычно используют в методе нейтрализации?
Как практически фиксируется точка эквивалентности в методе нейтрализации?
Как выражают концентрацию растворов в титриметрическом анализе?Дать определение молярной концентрации эквивалента,титра,титра по определяемому веществу.
Написать формулу для расчета молярной концентрации рабочего раствора,если известен: а) титр раствора;б) титр раствора по определяемому веществу.
Для чего титрование раствора одного и того же вещества нужно проводить не менее двух раз. В каких случаях нужно увеличить число титрований?
Чем отличается установка нормальности рабочего раствора по методу пипетирования и методу отдельных навесок?
Что называется кривой титрования?Для какой цели строят кривые тирования?
Какие индикаторы используют в кислотно-основном титровании?
