
- •Луганск 2007
- •Луганск 2007
- •Занятия 1, 2, 3 Оценка антропогенной нагрузки на окружающую среду балансовым методом
- •Задание для самостоятельной работы
- •1. Производство – синтез аммиака
- •Исходные данные
- •Состав сырого азота и водорода
- •Параметры процесса синтеза аммиака
- •2. Производство азотной кислоты окислением аммиака
- •Исходные данные
- •3. Производство серной кислоты контактным способом
- •Состав сухого колчедана
- •Параметры производства
- •Параметры источника выброса
- •Термодинамические параметры производства
- •Контрольные вопросы
- •Занятие 4 Оценка экологической эффективности промышленного производства
- •Алгоритм определения категории безотходности производства
- •Расчет коэффициента полноты использования материальных ресурсов
- •Расчет коэффициента полноты использования энергетических ресурсов
- •Расчет коэффициента соответствия экологическим требованиям
- •Коэффициент соответствия производства экологическим требованиям по отношению к гидросфере
- •Коэффициент соответствия производства экологическим требованиям по отношению к атмосфере
- •Задание для самостоятельной работы
- •Контрольные вопросы
- •ЛитературА
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ УКРАИНЫ
ВОСТОЧНОУКРАИНСКИЙ НАЦИОНАЛЬНЫЙ УНИВЕРСИТЕТ
имени Владимира ДАЛЯ

МЕТОДИЧЕСКИЕ УКАЗАНИЯ
к практическим занятиям по дисциплине
«Нормирование антропогенной нагрузки на окружающую среду»
занятия 1 – 4
(электронное издание)
Луганск 2007
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ УКРАИНЫ
ВОСТОЧНОУКРАИНСКИЙ НАЦИОНАЛЬНЫЙ УНИВЕРСИТЕТ
имени Владимира ДАЛЯ
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
к практическим занятиям по дисциплине
«Нормирование антропогенной нагрузки на окружающую среду»
занятия 1 – 4
(для студентов специальности «Экология и охрана окружающей среды»)
электронное издание
У Т В Е Р Ж Д Е Н О
на заседании кафедры
экологии.
Протокол № 8 от 28.11.06
Луганск 2007
УДК 504.75
Методические указания к практическим занятиям по дисциплине «Нормирование антропогенной нагрузки на окружающую среду» (для студентов специальности «Экология и охрана окружающей среды») / Сост. О.Р. Игнатов, Ю.И. Шеховцов. – Луганск: Изд-во ВНУ им. В. Даля, 2006. – 56 с.
Приведены примеры решения задач практических занятий по дисциплине «Нормирование антропогенной нагрузки на окружающую среду», а также даны варианты заданий для самостоятельного выполнения. Показан порядок оценки и пример расчета антропогенной нагрузки промышленного производства на окружающую среду методом материального и энергетического балансов, сопровождаемый необходимыми схемами и таблицами, а также порядок аттестации производства по критериям безотходности. Методические указания предназначены для студентов специальности «Экология и охрана окружающей среды», однако они могут быть использованы студентами инженерных специальностей при выполнении раздела дипломного проекта по промышленной экологии.
Составители: О.Р. Игнатов, доц.,
Ю.И. Шеховцов, асс.
Отв. за выпуск Л.С. Заиграев, доц.
Рецензент Б.Т. Харьковский, проф.
Занятия 1, 2, 3 Оценка антропогенной нагрузки на окружающую среду балансовым методом
Анализ причин негативного влияния производственной деятельности на естественные экосистемы показывает, что они обусловлены различием круговорота веществ в хозяйственных системах по сравнению с экосистемами, в которых приток и расход вещества сбалансированы.
В хозяйственных системах из взятого у природы вещества используется незначительная его часть (1…3 %), остальное возвращается в биосферу, как правило, наделенное в процессе производства новыми, разрушительными для экологических систем физико-химическими свойствами. Выделенная полезная часть вещества не всегда возвращается в процесс производства и теряется безвозвратно, выбывая из хозяйственного оборота.
Причины негативного воздействия производства на окружающую среду объясняются и несовершенством технологий, и экспоненциальным ростом масштабов производства. При сохранении такой тенденции ресурсо- и энергосберегающие технологии не оказывают заметного влияния на уменьшение воздействия на окружающую среду, так как удельная экономия материалов и энергии на единицу продукции отстает от роста объемов производства.
Улучшение экологической ситуации должно реализовываться в комплексе с решением бережного и рационального использования природных ресурсов для нужд человека, управлением демографической ситуации и переходом от экстенсивных форм хозяйствования, жизнеспособность которых зависит от увеличения объемов производства, к интенсивным – задачей которых является использование внутренних резервов производства как технологических, так и возможностью глубокой переработки сырья и применением материалов, поддающихся утилизации или биодеградации.
Экологический подход к оценке воздействия производственной деятельности на окружающую среду включает в себя качественную и количественную картину поступления вредных веществ в естественную экосистему, а также степень совершенства производства с позиции рационального использования материальных и энергетических ресурсов в нем.
Использование системного подхода с целью анализа комплексного воздействия производственной деятельности на окружающую среду нашло отражение в методике полного жизненного цикла продукта. Основная идея использования такой методики заключается в максимально полном охвате всех стадий «жизни» продукта, начиная от поиска сырья для его изготовления до вывода его из эксплуатации и утилизации (рис. 1.1). Применение такой методики позволяет оценить воздействие на природную среду любого продукта, как на отдельных стадиях его изготовления, так и в течение всего производственного цикла.

Рис. 1.1. Обобщенная схема жизненного цикла продукта
Стадии полного жизненного цикла продукта можно охарактеризовать тремя критериями:
количеством материальных ресурсов, вовлеченных в цикл производства;
количеством энергетических ресурсов, необходимых для поддержания цикла производства;
количеством и толерантностью отходов, попадающих в природные среды (водные объекты, воздух и почву), к биотическим и абиотическим компонентам экосистемы.
Оценка жизненного цикла продукта связана с экологическими аспектами и потенциальными воздействиями на окружающую среду в течение полного жизненного цикла продукта: от добычи сырья, использования готовой продукции до переработки отслуживших свой срок изделий и захоронения отходов. Основными видами воздействий на окружающую среду, которые принимаются во внимание, являются: истощение невозобновляемых природных ресурсов, ухудшение здоровья людей, деградация экосистем.
Оценка жизненного цикла продукта может быть полезна:
для определения потенциальных возможностей повышения экологической безопасности продукции на различных стадиях ее жизненного цикла;
как основа для принятия решений в промышленности, государственных органах, неправительственных организациях (например, стратегическое планирование, выбор приоритетов, разработка новых изделий или технологий, либо модернизация старых);
для выбора достоверных индикаторов экологических характеристик продукции, включая методики их определения;
в маркетинге (как индикаторе экологической безопасности продукции, для экологической маркировки, для подготовки экологической декларации на продукцию, которая повышает ее конкурентоспособность).
Методы составления материальных и энергетических расчетов являются сегодня наиболее ценными и эффективными для определения масштабов загрязнения окружающей человека среды. В основе таких расчетов лежит балансовый метод, заключающийся в установлении однозначной связи между входными и выходными потоками вещества и энергии в производственной системе на основе законов сохранения вещества и энергии.
При расчетах материальных потоков производственного процесса балансовый метод позволяет установить состав и количество вредных веществ с учетом химического состава и свойств исходного сырья, особенностей оборудования и применяемых технологий, оптимальных параметром технологического процесса, обеспечивающих требуемую программу выпуска продукта. Анализ структуры материального баланса производства позволяет установить полноту (эффективность) использования исходного сырья и материалов и наметить пути снижения материалоемкости производства.
Энергетический баланс позволяет установить масштаб и структуру задействованных энергетических ресурсов в производственном процессе, полноту (эффективность) их использования, пути повышения энергетической эффективности производства, наличие вторичных источников энергетических ресурсов, а также неизбежные потери энергии, определяющие масштаб энергетического загрязнение окружающей среды.
Целью практических занятий является изучение студентами метода материального и энергетического балансов промышленного производства, как способа оценки масштаба антропогенной нагрузки на окружающую среду, и приобретение практических навыков его использования.
Оценка влияния производственной деятельности человека на окружающую среду представляет собой трудоемкий процесс. Это обусловлено, прежде всего, сложностью техносферы, созданной человеком. Для принятия решений по сложившейся или прогнозируемой экологической ситуации необходимо располагать фактическими данными о конкретном производственном объекте, которые не всегда можно получить посредством прямого измерения и контроля узловых участков технологических процессов производства.
Производственный (техногенный) объект можно анализировать с позиции его материальных и энергетических потоков. По степени сложности материальных потоков техногенные объекты могут быть простыми и сложными.
Простые объекты характеризуются неразветвленной структурой материальных потоков, например, участок погрузки-разгрузки. Для сложных объектов характерна разветвленная система материальных потоков, в которой возможны последовательные, параллельные, параллельно-последовательные и перекрестные схемы материальные потоков.
По степени замкнутости техногенные объекты разделяются на закрытые и открытые. Первые с внешней средой не обмениваются веществом, вторые, наоборот, поддерживают обмен с внешней средой.
Наиболее общий случай взаимодействия системы с ее окружением, представлен на рис. 1.2.

Рис. 1.2. Схема материальных и энергетических потоков в техногенном объекте
В основе формирования материальных и энергетических балансов лежат законы сохранения вещества и энергии. Это означает, что, сколько мы использовали для производства какого-либо продукта, вещества и энергии, столько же вещества и энергии мы должны получить после завершения производственного цикла, но уже в другом виде. С помощью законов сохранения представляется возможным установить однозначную связь между входными и выходными потоками вещества и энергии.
Для сложных производственных процессов такая связь может устанавливаться эмпирически, путем представляя производственного процесса в виде «черного ящика». В этом случае с помощью регрессионной зависимости устанавливают связь между входными и выходными параметрами производственного процесса. Полученная регрессионная зависимость позволяет рассчитать материальные и энергетические потоки с учетом режима работы применяемого технологического оборудования в рассматриваемом производстве.
Для остальных случаев, когда характер и технология процесса производства достаточно изучены, используются известные физические и химические закономерности, отражающие законы сохранения конкретного явления или процесса, наблюдаемого в производственном процессе. Примером этого могут служить химические процессы, для которых известен химизм протекающих реакций. Достаточно записать уравнение химической реакции, задаться величинами исходных продуктов, и уже можно анализировать материальные потоки этого процесса. Здесь уравнение химической реакции отражение закона сохранения вещества.
В общем виде материальные потоки в производственном объекте в соответствии с законом сохранения вещества записывают в балансовой форме
![]() (1.1)
(1.1)
Здесь М1 и М2 – суммарные входящие в объект и выходящие из него материальные потоки; Мо – поток вещества, поступающий из окружения; ∆M – изменение массы вещества в объекте, в стационарных процессах эта величина равна нулю.
Энергетические потоки в техногенном объекте сбалансированы соответственно уравнения
![]() (1.2)
(1.2)
Здесь Q1 и Q2 – суммарные потоки тепла, входящие в объект и выходящие из него; L1 и L2 – суммарная работа, подводимая к объекту и получаемая от него; Qо – тепло, отдаваемое в окружающую среду или получаемое от нее.
Рассмотрим частный случай энергетического баланса – тепловой баланс, как наиболее часто встречающийся. Если объект обменивается с другим объектом энергией в форме тепла, то энергетический баланс записывается в виде уравнения теплового баланса:
![]() (1.3)
(1.3)
Тепло, подведенное к объекту извне Q1 и не принимающее участия в химических реакциях, рассчитывается по теплотворной способности топлива или теплосодержанию газообразного, жидкого или твердого теплоносителя.
Тепло Q2 экзотермических реакций и физических превращений исходных веществ из одного агрегатного состояния в другое при плавлении, испарении жидкости или в процессах растворения и кристаллизации, определяется из экспериментальных данных или путем термохимического расчета по закону Гесса.
Физическое тепло Q3 и Q5, введенное в процесс с исходными веществами и выведенное с продуктом и отходами производства, определяется теплосодержанием вещества – Q = mCt. Здесь m – масса исходных веществ или продуктов; С – средняя удельная массовая теплоемкость веществ при температуре их поступления или вывода из производственного цикла (кДж/(кг · °С); t – температура исходных веществ или продуктов, обычно выражается в градусах Цельсия (°C).
Полезное тепло Q4 – это то тепло, которое необходимое затратить для осуществления процесса производства. Определяется из термодинамической эффективности производственного процесса (по известному КПД) или путем исследования термодинамических циклов производственного процесса.
Потери тепла в окружающую среду Q6 обусловлены теплопроводностью наружных стенок аппарата, излучением и конвекцией, рассчитываются на основе законов теплопередачи или берутся из практических данных, или по разности между суммой приходных и расходных статей энергетического баланса.
Если в справочной литературе нет значений величин, входящих в структуру энергетического баланса, то пользуются законами, формулами и практическими данными, позволяющими произвести соответствующие расчеты. Например, если в справочной литературе нет данных о тепловом эффекте реакций или их экспериментальное определение затруднительно, то их вычисляют, руководствуясь законом постоянства сумм Гесса, согласно которому тепловой эффект реакции равен алгебраической сумме теплот образования реагентов из простых веществ. В этом случае тепловой эффект определиться как разность между теплотой образования химических соединений в правой и левой частях химических уравнений.
Величина теплоемкости для заданной
температуры может определяться по
интерполяционному уравнению
![]() ,
где а, b, c
– характерные для данного вещества
постоянные, которые находятся в справочной
литературе.
,
где а, b, c
– характерные для данного вещества
постоянные, которые находятся в справочной
литературе.
Если в справочной литературе отсутствуют данные о величине теплоемкости, то пользуются следующими приближенными данными.
Для большинства твердых тел теплоемкости элементов почти одинаковы и близки к 26,8 кДж/(моль · град.) (это не относится к Н, В, С, Si, P, О, S, F), а мольные теплоемкости равны сумме атомных теплоемкостей, составляющих молекулу элементов. Следует иметь в виду, что при протекании процессов плавления или кристаллизации теплосодержание жидких веществ включает теплоту плавления, а при процессах парообразования или конденсации газообразных веществ включает теплоту парообразования.
Анализ теплофизических свойств веществ и материалов позволяет в некоторых случаях наметить необходимые энергосберегающие мероприятия без привлечения сложных математических расчетов и оценок. Например, плотность и теплоемкость являются весьма важными показателя. Теплоносители более высокой плотности и теплоемкости позволяют при небольших перепадах температур между стенкой и жидкостью отвести или подвести большие тепловые потоки. С этой точки зрения вода имеет значительные преимущества по сравнению с теплоносителями меньшей плотности, например, с воздухом и газами.
Теплопроводность существенно влияет на интенсивность теплоотдачи. Чем больше теплопроводность теплоносителя при прочих равных условиях, тем выше коэффициент теплоотдачи от жидкости к стенке теплообменника и наоборот. Жидкие металлы, обладающие высокой теплопроводностью, имеют преимущества по сравнению с водой и газовыми теплоносителями, у которых теплопроводность невелика. Хотя сравнение теплофизических свойств веществ позволяет выбрать наиболее выгодные материалы, необходимо учитывать и экологический аспект такого выбора. Используемые материалы должны быть экологически чистыми в отношении их получения, эксплуатации и дальнейшей утилизации.
Анализ материального и энергетического балансов производства можно производить по алгоритму изображенному на рис. 1.3.
Информация о структуре производства или его части берется из проектных и технологических данных, если это не сложное производство, то структуру определяют по результатам натурных исследований.
На основе сведений о структуре и технологических объектах производства описываются физические и химические процессы, протекающие в структурных технологических подразделениях производства. Для этого можно использовать справочную литературу, описывающую подобные производства, проектные данные или данные натурных исследований.
Физическое описание процессов, протекающих в каждом технологическом объекте производства, позволяет формулировать математическое описание компонентов материального и энергетического балансов, которое показывает объем исходных данных, необходимый для реализации расчета материальных и энергетических потоков.

Рис.1.3. Порядок анализа материальных и энергетических потоков производства
Результатом проведенной подготовительной работы является четкая структура материальных потоков, которая строится на основе технологической схемы рассматриваемого производства. При этом количество вычислительных блоков может отличаться от количества технологических объектов, как в большую, так и в меньшую сторону, в зависимости от расчетных потребностей.
В общем случае схема производства, если это нужно, разбивается на отдельные вычислительные блоки таким образом, чтобы в каждый такой блок попадало не более одной неизвестной величины. Блок рассматривается как целостная система, для которой можно составить материальный и энергетический баланс.
На основе результатов расчета материального и энергетического балансов проводится анализ и оценка антропогенной нагрузки производства на окружающую среду и перечень рекомендаций по улучшению экологических показателей производства.
Рассмотрим методику составления материального и энергетического балансов на следующем примере.
Пример
Рассчитать и сделать анализ материального и энергетического балансов производства нитробензола по технологии представленной на рис. 1.4. Оценить масштаб антропогенной нагрузки на окружающую среду.

Рис. 1.4. Схема процесса получения нитробензола
Реакция получения нитробензола (С6H5NO2) протекает в присутствии серной кислоты (H2SO4) и избытке бензола (С6Н6) из расчета 1 кмоль бензола на 0,95 кмоль азотной кислоты (HNO3):
![]() .
.
Азотная и серная кислоты поступают в виде растворов с массовыми концентрациями 2 и 3. Концентрация серной кислоты в течение процесса получения нитробензола уменьшается до величины 6. Вода, образующаяся в ходе реакции и поступающая с раствором азотной кислоты, уменьшает концентрацию серной кислоты в растворе.
Введение исходных продуктов в систему и выведение из нее продуктов реакции осуществляется при температуре окружающей среды t1. Реакция получения нитробензола протекает при температуре t2 > t1 с эффективностью, которая определяется выходом реакции ().
В процессе смешения реагентов происходит выделение тепловой энергии при взаимодействии бензола с азотной кислотой и в результате разбавления серной кислоты реакционной водой и водой, поступающей с исходными реагентами. Количество выделяемой тепловой энергии определяется соответственно удельным тепловым эффектом нитрования бензола и (q1) и удельной теплотой разбавления серной кислоты (q2). Потери тепловой энергии нормируются коэффициентом тепловых потерь (), который определяет долю тепла, теряемую от общего входного потока тепловой энергии.
При расчете принимаются следующие исходные данные:
|
М1 = 100 кг; |
|
С1 = 1,72 кДж/(кг · °С); |
|
С2 = 2,51 кДж/(кг · °С); |
|
С3 = 1,42 кДж/(кг · °С); |
|
2 = 0,7 (масс. доли); |
|
3 = 0,92 (масс. доли); |
|
6 = 0,72 (масс. доли); |
|
= 0,8; |
|
t1 = 20 °С; |
|
t2 = 50 °С; |
|
q1 = 153 кДж/моль; |
|
= 0,2. |
Решение
Материальный баланс. На основании закона сохранения вещества (массы) формируется материальный баланс производства нитробензола, который устанавливает связь между входными и выходными потоками вещества:
![]() , (1.4)
, (1.4)
где Мвх – масса входного потока вещества;
Мвых – масса выходного потока вещества.
Для расчетного анализа материальных потоков необходимо изучить упрощенную схему производства нитробензола (рис. 1.3). На ее основе составить подробную схему материальных потоков и подобрать не достающие исходные данные. Технологическую схему на рис. 1.4, можно представить как одну технологическую единицу, в которой структурные составляющие не различаются, и условно распределить в ней потоки вещества, так, как это сделано на рис. 1.5.

Рис. 1.5. Схема материальных потоков процесса получения нитробензола:
1 – зона входных потоков вещества; 2 – зона выходных потоков вещества
Входной поток вещества представляют как сумму составляющих его компонентов по формуле
![]() (1.5)
(1.5)
где М1 – масса бензола С6Н6 (известна по условию), кг;
М2 – масса раствора азотной кислоты HNO3, кг;
М3 – масса раствора серной кислоты H2SO4, кг.
По известному из условия оптимальному мольному соотношению исходных веществ определяем количество вещества HNO3 требуемого для реакции:
![]() ,
,
где n1 – количество вещества С6Н6,
![]()
1 – мольная масса бензола, кг/кмоль, 1 = 78 кг/кмоль.
С другой стороны количество молей HNO3 определяется аналогично бензолу:
![]() (1.6)
(1.6)
где М2 HNO3 – масса HNO3, кг;
2 – мольная масса HNO3, кг/кмоль, 2 = 63 кг/кмоль.
Отсюда
![]() (1.7)
(1.7)
Так как НNO3 поступает в реактор-смеситель в виде раствора, то окончательно масса раствора HNO3 (М2) равна:
![]() (1.8)
(1.8)
где 2 – массовая доля HNO3 в водном растворе по условию.
Необходимое количество раствора Н2SO4, поступающего в реактор–смеситель, будет рассчитываться с учетом количества воды, образовавшейся в реакторе-смесителе.
Количество воды (M2 Н2О), поступившей в реактор вместе с раствором азотной кислоты,
![]() (1.9)
(1.9)
Количество реакционной воды (Mр Н2О) находится из уравнения реакции по исходному веществу, находящемуся в недостатке (НNO3):
![]() (1.10)
(1.10)
где n2 – количество вещества НNO3 по формуле (1.6),
![]()
в – мольная масса H2O, кг/кмоль, в = 18 кг/кмоль;
– выход реакции по условию.
Подставляя полученные значения в выражение (1.10), определим количество воды по реакции нитрования бензола:
![]()
Общая масса воды (МН2О) на разбавление H2SO4 в реакторе-смесителе определяется как сумма M2 Н2О и Mр Н2О:
![]() (1.11)
(1.11)
Серная кислота в реактор-смеситель поступает в виде раствора с начальной массовой концентрацией 3. В ходе реакции концентрация раствора уменьшается до конечной величины 6 за счет разбавления реакционной водой и водой, поступившей с азотной кислотой. На основании этого, можно записать, руководствуясь определением массовой доли вещества в растворе, выражение массовых концентраций Н2SO4 на входе и выходе реактора-смесителя:
![]() и
и
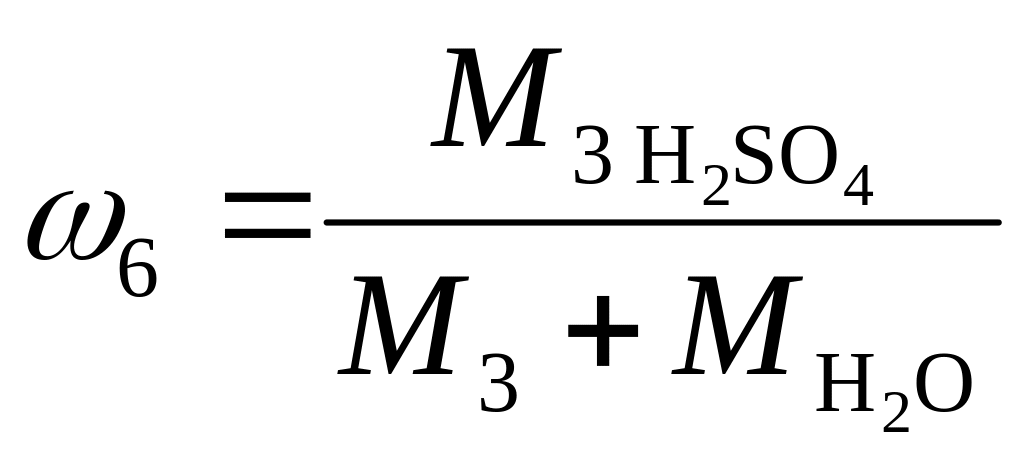 .
.
Разделим первое выражение на второе и решим полученное уравнение относительно массы раствора серной кислоты M3:
 (1.12)
(1.12)
Выходной поток вещества. После послойного разделения в отстойнике на выходе из технологической установки получения нитробензола имеем следующий поток вещества:
![]() (1.13)
(1.13)
![]()
Масса нитробензола (М4), полученная по реакции нитрования бензола, определяется из уравнения химической реакции по веществу находящемуся в недостатке (HNO3):
![]() (1.14)
(1.14)
где 4 – мольная масса С6H5NO2, кг/кмоль, 4 = 123 кг/кмоль.
Количество избыточного бензола (М5), необходимого для обеспечения заданного технологического режима, определяется выражением:
![]() (1.15)
(1.15)
Количество отработанной серной кислоты (М6) складывается из массы раствора серной кислоты поступающей в реактор-смеситель и массы воды, содержащейся в растворе азотной кислоты и образованной при смешении реагентов:
![]() (1.16)
(1.16)
Побочные продукты (М7) производства нитробензола, например, можно определить по выходу конечных продуктов реакции:
![]() (1.17)
(1.17)
Подставляя численные значения компонентов, получим массовый выход побочных продуктов:
![]()
Сравнивая полученные значения величин входных и выходных материальных потоков по уравнению (1.4), делаем проверку материального баланса и получаем очевидное тождество:
391,1 кг = 391,1 кг.
Структуру материального баланса удобно представлять в графическом виде. Для этого строится гистограмма входных и выходных материальных потоков (рис. 1.6), которая наглядно показывает соотношения компонентов (статей) в структуре материального баланса.

Рис. 1.6. Структура материального баланса производства нитробензола
Энергетический баланс. Энергетический баланс производства нитробензола представляет собой тепловой баланс и складывается из тепловых потоков возникающих в ходе технологического процесса. По аналогии с материальным балансом запишем общее уравнение энергетического баланса, представляющее собой равенство приходного и расходного тепловых потоков:
![]() (1.18)
(1.18)
где Qвх – приходный поток теплового баланса;
Qвых – расходный поток теплового баланса.
При рассмотрении энергетического баланса теплосодержание исходных продуктов и продуктов реакции не учитывается, так как ввод исходных продуктов и вывод продуктов реакции осуществляется при температуре окружающей среды t1.
Приход тепловой энергии. Приход тепловой энергии определяется термохимическим процессом нитрования бензола, процессом разбавления серной кислоты и подогревом реакционной смеси до температуры t2:
![]() (1.19)
(1.19)
![]()
Тепловой эффект реакции нитрования бензола (Q1) определяется по следующему уравнению:
![]() (1.20)
(1.20)
где q1 – удельная теплота реакции нитрования, кДж/моль;
n4 – количество молей нитробензола, моль,
![]()
Для определения выделившейся тепловой энергии при разбавлении серной кислоты, запишем возможные пути разбавления серной кислоты водой:
![]() – путь 1,
– путь 1,
![]() – путь 2,
– путь 2,
![]() – путь 3.
– путь 3.
В реактор попадает готовый раствор серной кислоты, в котором вода находится в связанном состоянии. Энергия, высвободившаяся при получении раствора, не должна учитываться при разбавлении в ходе процесса нитрования. Предполагается, что разбавление исходного раствора серной кислоты протекало по первому уравнению (путь 1), т. е. разбавление шло при одинаковом мольном соотношении исходных веществ. Учитывая это, количество серной кислоты связанной с водой равно количеству воды связанной с серной кислотой, отсюда:
![]()
где n3 – количество серной кислоты связанной с водой, моль.
Количество молей серной кислоты (n3), поступающей на разбавление, в соответствии с материальным балансом производства и учетом начального разбавления определяется по выражению:
![]()
где 3 – мольная масса H2SO4, кг/кмоль, 3 = 98 кг/кмоль.
Количество молей воды (nН2О) для разбавления соответствует массе воды, полученной в ходе реакции, и поступающей с раствором азотной кислоты:
![]()
Из полученного мольного соотношения воды и серной кислоты, видно, что количество воды в три раз больше, чем серной кислоты, поэтому разбавление может рассматриваться по реакциям 2 или 3 (путь 2 и 3). Рассчитаем количество гидратов, образовавшихся при разбавлении, с двумя и четырьмя присоединенными молями воды:
![]() или
или
![]()
где x – количество молей H2SO4 по реакции 2, моль;
y – количество молей H2SO4 по реакции 3, моль.
Решая систему уравнений, получим следующее:
![]()
Теплота (Q2), полученная в результате разбавления серной кислоты, определяется как сумма теплоты при разбавлении по 2 и 3 пути:
![]() (1.21)
(1.21)
где 41,92 и 54,06 – удельная теплота разбавления, соответственно по реакции 2 и 3, кДж/моль.
Затраты энергии на подогрев реакционной смеси могут компенсироваться тепловыделением в ходе непрерывного производства. В этом случае эти затраты энергии включаются только в расходную часть энергетического баланса. В данном примере принимается, что производство работает периодически и при запуске эти затраты энергии не могут быть компенсированы тепловыделением. Поэтому они включаются также и в приходную часть энергетического баланса.
Подогрев реакционной смеси от t1 до t2, определяется количеством тепловой энергии, затраченной в единицу времени, на нагревание ее компонентов:
![]() (1.22)
(1.22)
![]()
где Мi – масса исходных продуктов (М1, М2, М3), кг;
Сi – удельная теплоемкость исходных веществ (C1, C2, С2), кДж/(кг · ºС),
t1 и t2 – соответственно, начальная температура реакционной смеси и температура реакции, С.
Расход тепловой энергии. Выходной поток тепловой энергии показывает распределение входного потока тепловой энергии в зависимости от производственных потребностей. В данном примере, входной поток тепловой энергии расходуется на технологические нужды (осуществление химического процесса) и компенсацию тепловых потерь в окружающую среду. Следуя этому, запишем уравнение выходного теплового потока для производства нитробензола:
![]() (1.23)
(1.23)
Полезная тепловая энергия, используемая для осуществления процесса получения нитробензола, определяется количеством тепловой энергии затраченной на подогрев реакционной смеси:
![]() (1.24)
(1.24)
Тепловые потери (Q4), по условию нормируемые от прихода тепловой энергии, рассчитываются по формуле
![]() (1.25)
(1.25)
где – суммарная доля тепловых потерь установки по производству нитробензола.
Тепловая энергия (Q5), поступающая в систему охлаждения, определяется из основного уравнения теплового баланса (1.18):
![]() (1.26)
(1.26)
![]()
Понятно, что сравнивать энергетические потоки нет необходимости, так как уравнение (1.26) раскрывает взаимосвязь между компонентами прихода и расхода энергии в системе. В таком случае требуется лишь тщательный подсчет известных компонентов энергетического баланса во избежание расчетной ошибки. На рис. 1.7 показана структура энергетического баланса производства нитробензола.

Рис. 1.7. Структура энергетического баланса производства нитробензола
Задание для самостоятельной работы состоит из одной комплексной задачи, заключающейся, соответственно, в расчете материального и энергетического балансов заданного производства, построении гистограмм входных и выходных потоков вещества и энергии, анализе структуры материального и энергетического балансов.
Ниже приведено условие задания.
