
- •Основы радиационной экологии
- •Введение
- •1 Основные понятия, термины и определения
- •2 Из чего сделано вещество. Немного истории
- •2.1 Атомы
- •2.2 Элементарные частицы
- •2.3 Кварки
- •3 Элементарные частицы
- •3.1 Фундаментальные взаимодействия
- •3.2 Аннигиляция
- •4.1 Состав атомных ядер
- •4.2 Изотопы
- •4.3 Атом водорода
- •4.4 Дефект массы
- •4.5 Постулаты Бора
- •4.6 Корпускулярно-волновой дуализм
- •4.7 Энергия связи ядер
- •4.7.1 Энергетические уровни ядра
- •4.7.2 Насыщение ядерных сил
- •4.7.3 Импульс движения
- •4.7.4 Магнетон Бора
- •4.7.5 Спин ядра
- •4.8 Единицы атомной и ядерной физики
- •5 Радиоактивность
- •5.1 Естественная радиоактивность
- •5.2 Превращения ядерных частиц
- •5.7.1 Устойчивость ядер
- •5.3 Закон радиоактивного распада
- •5.4 Ядерные реакции
- •5.4.1 Первая ядерная реакция
- •5.4.2 Ядерные реакции под действием α- частиц
- •5.4.3 Ядерные реакции под действием протонов
- •5.4.4 Ядерные реакции под действием нейтронов
- •5.4.5 Реакция деления тяжелых ядер
- •5.4.5.1 Цепная реакция
- •5.4.5.2 Критическая масса
- •5.4.5.3 Ядерные реакторы
- •5.5 Синтез атомных ядер
- •5.5.1 Протон - протонная реакция
- •5.5.2 Углеродно – азотный цикл
- •5.5.3 Управляемый термоядерный синтез
- •6 Проявление радиоактивности
- •6.1 Ионизация
- •6.1.1 Потенциал ионизации
- •6.2 Взаимодействие ионизирующего излучения с веществом
- •6.2.1 Радиолиз воды
- •8.2.2 Свободные радикалы
- •6.3 Наведенная радиоактивность
- •Дозиметрия радиационных явлений
- •7.1 Радиоактивность, единицы измерения
- •7.2 Доза излучения
- •6.2.1 Экспозиционная доза
- •6.2.2 Поглощенная доза
- •6.2.3 Эквивалентная доза
- •6.2.4 Мощность дозы
- •8 Дозиметрия ионизирующих излучений
- •8.1 Детекторы ионизирующих излучений
- •8.1.1 Ионизационные камеры
- •8.1.1.1 Газоразрядные счетчики
- •8.1.2 Химические детекторы
- •8.1.3 Сцинтилляционные счетчики
- •8.1.4 Фотографические детекторы
- •8.1.6 Другие виды детекторов
- •8.2 Дозиметрические приборы
- •8.2.1 Некоторые дозиметрические приборы старшего поколения
- •8.2.2 Современные дозиметрические приборы
- •8.2.2.1 Многофункциональные приборы для контроля альфа, бета, гамма и нейтронного излучения
- •8.2.2.2 Приборы для контроля альфа - излучения
- •8.2.2.3 Приборы для контроля гамма – излучения
- •8.2.2.4 Системы индивидуальной дозиметрии
- •8.2.2.5 Приборы радиационного дозиметрического контроля
- •8.2.2.6 Радиометры
- •Приборы ветеринарного контроля
- •8.2.2.8 Системы радиационного контроля и мониторинга
- •8.2.2.9 Приборы радиационного контроля общего назначения
- •Заключение
- •Литература
- •Содержание
3.1 Фундаментальные взаимодействия
Процессы, в которых участвуют различные элементарные частицы, сильно различаются по характерным временам их протекания и энергиям. Согласно современным представлениям, в природе осуществляется четыре типа взаимодействий, которые не могут быть сведены к другим, более простым видам взаимодействий: сильное, электромагнитное, слабое и гравитационное. Эти типы взаимодействий называют фундаментальными.
Сильное (или ядерное) взаимодействие – это наиболее интенсивное из всех видов взаимодействий. Оно обуславливает исключительно прочную связь между протонами и нейтронами в ядрах атомов. В сильном взаимодействии могут принимать участие только тяжелые частицы – адроны (мезоны и барионы). Сильное взаимодействие проявляется на расстояниях до 10–15 м. Поэтому его называют короткодействующим.
Электромагнитное взаимодействие. В этом виде взаимодействия могут принимать участие любые электрически заряженные частицы, а так же фотоны – кванты электромагнитного поля. Электромагнитное взаимодействие ответственно, в частности, за существование атомов и молекул. Оно определяет многие свойства вещества в твердом, жидком и газообразном состояниях. Кулоновское отталкивание протонов приводит к неустойчивости ядер с большими массовыми числами. Электромагнитное взаимодействие обуславливает процессы поглощения и излучения фотонов атомами и молекулами вещества и многие другие процессы физики микро- и макромира.
Слабое взаимодействие – наиболее медленное из всех взаимодействий, протекающих в микромире. В нем могут принимать участие любые элементарные частицы, кроме фотонов. Слабое взаимодействие ответственно за протекание процессов с участием нейтрино или антинейтрино, например, β- - распад нейтрона

а также безнейтринные процессы распада частиц с большим временем жизни (τ ≥ 10–10 с).
Гравитационное взаимодействие присуще всем без исключения частицам, однако из-за малости масс элементарных частиц силы гравитационного взаимодействия между ними пренебрежимо малы и в процессах микромира их роль несущественна. Гравитационные силы играют решающую роль при взаимодействии космических объектов (звезды, планеты и т. п.), которые обладают значительными массами.
3.2 Аннигиляция
Способность к взаимным превращениям – это наиболее важное свойство всех элементарных частиц. Элементарные частицы способны рождаться и уничтожаться (испускаться и поглощаться). Это относится также и к стабильным частицам с той только разницей, что превращения стабильных частиц происходят не самопроизвольно, а при взаимодействии с другими частицами. Примером может служить аннигиляция (т. е. исчезновение) электрона и позитрона, сопровождающаяся рождением фотонов большой энергии. Может протекать и обратный процесс – рождение электронно-позитронной пары, например, при столкновении фотона с достаточно большой энергией с ядром. Такой двойник, каким для электрона является позитрон, есть и у протона. Он называется антипротоном. Электрический заряд антипротона отрицателен. В настоящее время античастицы найдены у всех частиц. Античастицы противопоставляются частицам потому, что при встрече любой частицы со своей античастицей происходит их аннигиляция, т. е. обе частицы исчезают, превращаясь в кванты излучения или другие частицы.
Античастица обнаружена и у нейтрона. Нейтрон и антинейтрон отличаются только знаками магнитного момента и так называемого барионного заряда. Возможно существование атомов антивещества, ядра которых состоят из антинуклонов, а оболочка – из позитронов. При аннигиляции антивещества с веществом энергия покоя превращается в энергию квантов излучения. Это огромная энергия, значительно превосходящая ту, которая выделяется при ядерных и термоядерных реакциях.
Мы уделили много внимания элементарным частицам, так как именно они определяют весь спектр действия ядерных превращений. Ядра атомов состоят из элементарных частиц и, в конечном счете, элементарные частицы обеспечивают передачу энергии ядерных реакций любому объекту.
4 Атом
Атом (от греч. atomos - неделимый), мельчайшая частица химического элемента, сохраняющая его свойства. В центре атома находится положительно заряженное ядро, в котором сосредоточена почти вся масса атома; вокруг движутся электроны, образующие электронные оболочки, размеры которых (~10-8 см) определяют размеры атома (рисунок 1.). Ядро атома состоит из протонов и нейтронов. Число электронов в нейтральном атоме равно числу протонов в ядре (заряд всех электронов атома равен заряду ядра), число протонов равно порядковому номеру элемента в периодической системе.
Атомы могут присоединять или отдавать электроны, становясь отрицательно или положительно заряженными ионами. Химические свойства атомов определяются в основном числом электронов во внешней оболочке; соединяясь химически, атомы образуют молекулы. Важная характеристика атома — его внутренняя энергия, которая может принимать лишь определенные (дискретные) значения, соответствующие устойчивым состояниям атома, и изменяется только скачкообразно путем квантового перехода. Поглощая определенную порцию энергии, атом переходит в возбужденное состояние (на более высокий уровень энергии).
Из возбужденного состояния атом, испуская фотон, может перейти в состояние с меньшей энергией (на более низкий уровень энергии). Уровень, соответствующий минимальной энергии атома, называется основным, остальные — возбужденными. Квантовые переходы обусловливают атомные спектры поглощения и испускания, индивидуальные для атомов всех химических элементов. На рисунке 2. показано образование спектральных серий в излучении атома водорода при переходе электрона с высоких стационарных орбит на более низкие.
Спектральные линии – это узкие участки в оптических спектрах, каждый из которых можно охарактеризовать определённой длиной волны (или частотой υ = с / λ , где с — скорость света). Они наблюдаются в спектрах испускания как светлые (цветные) линии на тёмном фоне, в спектрах поглощения — как тёмные линии на светлом фоне. Каждая линия соответствует определённому квантовому переходу в атоме (молекуле, кристалле). Спектральные линии не являются строго монохроматичными: каждая из них имеет некоторую ширину .
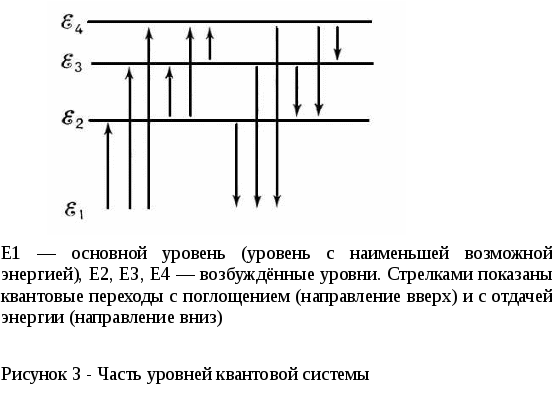
Квантовые переходы - скачкообразные переходы квантовой системы (атома, молекулы, атомного ядра, твёрдого тела) из одного состояния в другое. Наиболее важными являются переходы между стационарными состояниями, соответствующими различной энергии квантовой системы, - квантовые переходы системы с одного уровня энергии на другой. При переходе с более высокого уровня энергии Ek на более низкий Ei система отдаёт энергию Ek — Ei, при обратном переходе — получает её (рисунке 3.). Квантовые переходы могут быть излучательными и безызлучательными. При излучательных - система испускает (переход Ek Ei) или поглощает (переход Ei Ek) квант электромагнитного излучения - фотон - энергии h ( - частота излучения, h - постоянная Планка), удовлетворяющей фундаментальному соотношению Ek - Ei = h, которое представляет

собой закон сохранения энергии при таком переходе). В зависимости от разности энергий состояний системы, между которыми происходит квантовые переходы испускаются или поглощаются фотоны радиоизлучения, инфракрасного, видимого, ультрафиолетового, рентгеновского излучения, γ-излучения. Совокупность излучательных квантовых переходов с нижних уровней энергии на верхние образует спектр поглощения данной квантовой системы, совокупность обратных переходов — её спектр испускания.
Важнейшей характеристикой любого квантового перехода является вероятность перехода, определяющая, как часто происходит данный квантовый переход. Вероятность перехода измеряют числом переходов данного типа в рассматриваемой квантовой системе за единицу времени (1 сек); поэтому она может принимать любые значения от 0 до (в отличие от вероятности единичного события, которая не может превышать 1). Вероятности переходов рассчитываются методами квантовой механики.
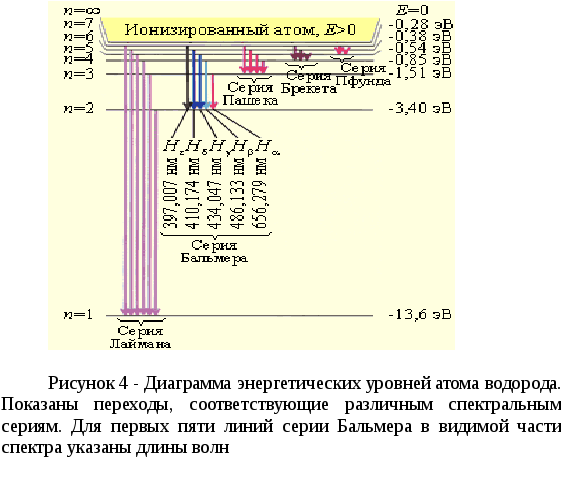
На рисунке 4. изображена диаграмма энергетических уровней атома водорода и указаны переходы, соответствующие различным спектральным сериям.
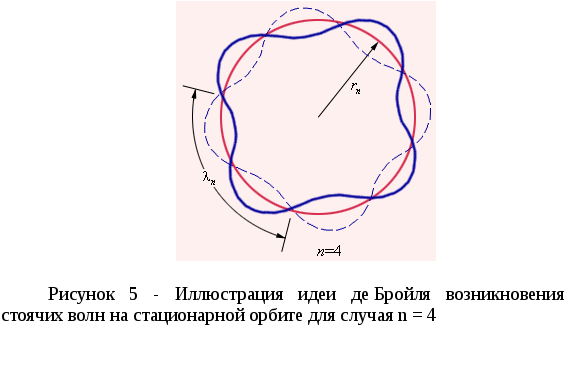
Согласие теории атома водорода Бора с экспериментом служило веским аргументом в пользу ее справедливости. Однако попытки применить эту теорию к более сложным атомам не увенчались успехом. Бор не смог дать физическую интерпретацию правилу квантования. Это было сделано десятилетием позже де Бройлем на основе представлений о волновых свойствах частиц. Де Бройль предложил, что каждая орбита в атоме водорода соответствует волне, распространяющейся по окружности около ядра атома. Стационарная орбита возникает в том случае, когда волна непрерывно повторяет себя после каждого оборота вокруг ядра, т.е. стационарная орбита соответствует круговой стоячей волне де Бройля на длине орбиты (рисунок 5.). Это явление очень похоже на стационарную картину стоячих волн в струне с закрепленными концами.
Простое, и для нашего дальнейшего рассмотрения достаточное, представление атома состоящего из тяжёлого ядра, обладающего положительным электрическим зарядом, и окружающих его более лёгких электронов с отрицательными электрическими зарядами, образующих электронные оболочки. Размеры атома определяются размерами его электронной оболочки и значительно превосходят размеры ядра (таблица 2.).
Таблица 2 - Характерные порядки размеров
|
|
Линейные размеры |
Площадь* |
Объем |
|
Атом |
10—8 см |
10—16 см2 |
10—24 см3 |
|
Ядро |
10—12 см |
10—24 см2 |
10—36 см3 |
|
Отношение |
104 |
108 |
1012 |
* Поперечное сечение
Электронные оболочки атома не имеют строго определённой границы (рисунок 5.), поэтому его размер в большей или меньшей степени зависит от способов определения и может значительно различаться.
