
- •Руководство
- •Оглавление
- •Глава 1. Растворы……………………..………………………………………………..…...7
- •Глава 2. Элементы химической термодинамики и био-
- •Глава 1. Растворы
- •1.1. Способы выражения концентрации растворов
- •Примеры решения задач Массовая доля компонента.
- •Молярная концентрация
- •Молярная концентрация эквивалента (нормальная концентрация)
- •Моляльная концентрация
- •Лабораторная работа Приготовление растворов заданной концентрации
- •Вопросы и задачи для самоподготовки.
- •1.2. Растворы сильных и слабых электролитов
- •Примеры решения задач
- •Вопросы и задачи для самоподготовки.
- •1.3. Автопротолиз воды. Ионное произведение воды. Водородный и гидроксильный показатели. Гидролиз солей
- •Примеры решения задач
- •Гидролиз солей
- •1.4. Буферные растворы
- •Приготовление буферных растворов и определение буферной ёмкости
- •Примеры решения задач
- •Вопросы и задачи для самоподготовки.
- •1.5. Гетерогенное равновесие
- •Лабораторная работа Ислледование гетерогенных равновесий на реакциях ионного обмена
- •Примеры решения задач
- •Вопросы и задачи для самоподготовки
- •1.6. Коллигативные свойства растворов неэлектролитов
- •Примеры решения задач
- •Вопросы и задачи для самоподготовки.
- •Глава 2. Элементы химической термодинамики и биоэнергетики. Термохимия
- •Примеры решения задач
- •Вопросы и задачи для самоподготовки.
- •Глава 3. Химическая кинетика и катализ. Равновесие
- •3.1. Химическая кинетика и катализ
- •Скорость химической реакции
- •Примеры решения задач
- •Вопросы и задачи для самоподготовки.
- •3.2. Химическое равновесие
- •Химическое равновесие
- •Примеры решения задач
- •Вопросы и задачи для самоподготовки
- •Глава 4. Основы электрохимии
- •4.1. Электрическая проводимость растворов электролитов. Кондуктометрия
- •Кондуктометрические измерения
- •4.2. Потенциометрическое измерение рН растворов
- •Потенциометрическое измерение рН растворов
- •Примеры решения задач
- •Вопросы и задачи для самоподготовки
- •Глава 5. Поверхностные явления
- •5.1. Адсорбция на твердой поверхности
- •Адсорбция на твердом теле
- •Исходя из термодинамических представлений, д.Гиббс вывел зависимость между адсорбцией и поверхностным натяжением, т.Е. Уравнение изотермы адсорбции на жидкой поверхности: ,
- •Адсорбция на жидкой поверхности
- •5.3. Хроматография
- •Гель-фильтрация голубого декстрана и витамина в2 (рибофламина) на сефадексе g-25
- •Примеры решения задач
- •Вопросы и задачи для самоподготовки
- •Глава 6. Лиофобные коллоидные системы
- •6.1. Получение и очищение коллоидных растворов
- •Получение золей
- •6.2. Электрические свойства коллоидных систем
- •Определение знака заряда коллоидных частиц
- •6.3. Коагуляция в коллоидных растворах
- •Определение зависимости коагулирующей способности электролитов
- •Примеры решения задач
- •Вопросы и задачи для самоподготовки
- •Глава 7. Высокомолекулярные соединения
- •7.1. Свойства растворов высокомолекулярных соединений
- •Свойства растворов высокомолекулярных соединений
- •7.2. Вязкость растворов высокомолекулярных соединений
- •Вискозиметрическое определение молекулярной массы полиэтиленгликоля
- •Примеры решения задач
- •7.3. Углеводы
- •Определение константы скорости гидролиза сахарозы
- •Вопросы и задачи для самоподготовки
- •Глава 8. Мицеллярные поверхностно-активные вещества (системы с самопроизвольным мицеллообразованием, полуколлоиды)
- •Определение критической концентрации мицеллообразования методом измерения поверхностного натяжения
- •Вопросы и задачи для самоподготовки
- •Глава 9. Микрогетерогенные системы
- •Свойства эмульсий и пен
- •Примеры решения задач
- •Вопросы и задачи для самоподготовки
- •Образец билета модуля № 1 «Элементы общей химии. Поверхностные явления. Коллоидные системы»
- •Образец билета модуля № 2 «Микрогетерогенные системы»
Гель-фильтрация голубого декстрана и витамина в2 (рибофламина) на сефадексе g-25
Задачи работы: изучение разделения смеси веществ методом гель-фильтрации
Оборудование и реактивы: хроматографическая колонка, заполненная грану-
81
лами сефадексе G-25, смесь голубого декстрана и витамина В2 (рибофламина), дистиллированная вода, пипетки, штатив с пробирками, стакан.
Выполнение работы: конец пластиковой трубки, отходящей от колонки, опустить в стакан и спустить раствор в колонке до уровня геля. Затем поднять конец трубки выше уровня геля и аккуратно по стенке колонки внести (наслоить) 1 мл разделяемого раствора, стараясь не взмучивать гель. Конец пластиковой трубки поместить в первую пробирку штатива и дать впитаться нанесенному раствору. Затем на поверхность геля осторожно нанести 10 мл дистиллированной воды и последовательно собирать фракции элюата по 2 мл в каждую из 5 пробирок. После сбора последней фракции конец трубки поднять выше уровня геля и закрепить к колонке (на поверхности геля обязательно должен остаться слой воды высотой примерно 1 см).
Порядок оформления работы: записать принцип метода гель-фильтрации, ход работы, зарисовать колонку, объяснить, какой компонент – голубой декстран (молекулярная масса 2 млн) или зеленовато-желтый рибофлавин (молекулярная масса 376,4) элюируется первым? Сделать вывод об эффективности разделения высоко- и низкомолекулярных веществ данным методом.
Примеры решения задач
Пример 1. Вычислите по данным сталагмометрического исследования поверх-ностное натяжение этанола при 250С, если число капель воды – 32, а спирта 64. Поверхностное натяжение воды при этой температуре равно 72,56 мДж/м2.
|
Дано: s(Н2О) = 72, 56 мДж/м2 N(H2O) = 32 N(спирта) = 64 s |
Решение: поверхностное натяжение этанола вычисляем относительно поверхностного натяжения воды по формуле:
Ответ: 36,28 мДж/м2 |
Пример 2. Предельная адсорбция ПАВ некоторым адсорбентом составляет 0,005 моль/г. Вычислите массу адсорбированного ПАВ из раствора равновесной кон-центрацией 0,1 моль/л адсорбентом массой 2 г. Относительная молекулярная масса ПАВ равна 60, а константа равновесия 0,06 моль/л.
|
Дано: Гмакс = 0,005 моль/г С = 0,1 моль/л K = 0,06 моль/л m m(ПАВ) − ? |
Решение:
2) количество ПАВ, адсорбированное двумя граммами адсорбента будет 2 раза больше: v(ПАВ) = 2Г = 0,0062 моль 3) вычисляем массу ПАВ: m(ПАВ) = v(ПАВ).М = 0,0062.60 = 0,37 г. Ответ: 0,37 г. |
82
Пример 3. Определить адсорбцию масляной кислоты при 290 K, если для её растворов при концентрации 0,0103 кмоль/м3 значение поверхностного натяжения равно 65,45.10−3 Дж/м2, а при 0,0206 кмоль/м3 – 59,78.10−3 Дж/м2. R =8,314.103Дж/(кмоль.К).
|
Дано: T = 290 K C1 = 0,0103 кмоль/м3 s1 = 65,45.10−3 Дж/м2 C2 = 0,0206 кмоль/м3 s1 =59,78.10−3 кмоль/м3 R Г − ? |
Решение:
адсорбция жидкости на жидкой поверхности
вычисляется по уравнению Гиббса:
Ответ: 3,6.10−9 кмоль/м2 |
Пример 4. Для проведения адсорбции к 50 мл раствора уксусной кислоты внесено 2 г активированного угля. Температура опыта 25оС. Объемы 0,1 М раствора NaOH, израсходованных на титрование 20 мл растворов кислоты до и после адсорбции составили 2,6 и 0,6 мл. Вычислите величину адсорбции.
|
Дано: m(адсорбента) = 2 г V1(CH3COOH) = 50 мл V2(CH3COOH) = 20 мл C(NaOH) = 0,1 моль/л V1(NaOH) = 2,6 мл V2(NaOH) = 0,6 мл Г − ?
|
Решение:
адсорбция жидкости на твердой
поверхности вычисляется по уравнению:
1) вычисляем концентрации кислоты до и после адсорбции по закону эквивалентов:
2) вычисляем адсорбцию:
Ответ: 0,25 ммоль/г. |
Пример 5. Величина предельной адсорбции бутанола составляет 7,69.10−6 моль/м2. Вычислите площадь, занимаемой одной молекулой и длину молекулы бутанола. Плотность бутанола равна 0,809 г/мл, молярная масса 74 г/моль.
|
Дано: Гмакс = 7,69.10−6 моль/м2 d = 0,809 г/мл M(C4H9OH) = 74 г/моль NA = 6,02.1023 S l − ? |
Решение: 1) площадь, занимаемой одной молекулой в плотном мономолекулярном слое вычисляем по формуле:
2) длину молекулы рассчитываем по формуле:
83
Ответ: S = 2,16.10−19 м2; l = 7,03.10−10 м. |

 (спирта)
− ?
(спирта)
− ? = 8,314.103Дж/(кмоль.К)
= 8,314.103Дж/(кмоль.К)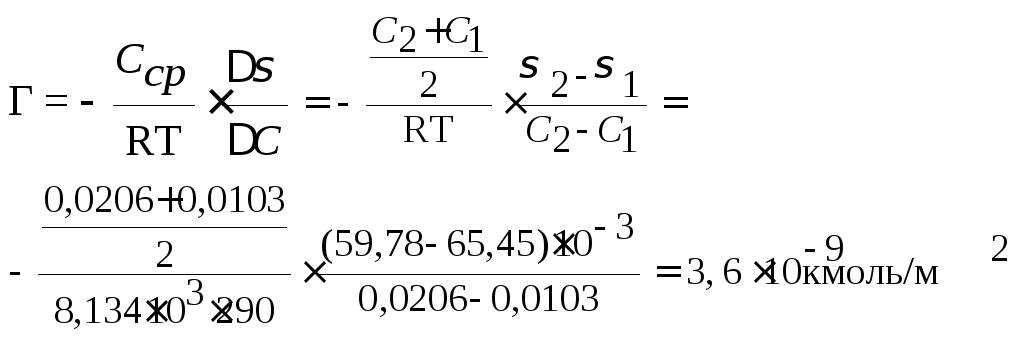
 моль/л
моль/л −?
−?