
-
В водной среде прямая ацидиметрия.
Титрование по варианту вытеснения прямое, индикатор тропеолин 00 окраска из желтой в красноватую.
CH3COOK+ HCl→ CH3COOH+ KCl
Хранение: в хорошо укупоренной таре, предохраняющей от влаги.
Применение: источник калия при гипокалийемии и диуретик.
Кальция лактат Calcii lactas (ЛН) Calcium lactate (МНН)

Получение
Кальция лактат получают из глюкозы, при молочнокислом брожении. При температуре 35-45°С образуется молочная кислота. Молочную кислоту нейтрализуют кальция карбонатом.

глюкоза

Описание
лактат - белый мелкий аморфный порошок без запаха, выветривающийся на воздухе. Медленно растворим в воде, легко - в горячей воде, очень мало растворим в спирте, эфире и хлороформе
Подлинность
-
ИК – спектр в рекомендуемых ФС условиях, который должен полностью совпадать с полосами поглощения прилагаемого рисунка спектра стандартного образца.
-
Доказывают катион Ca2+по известным реакциям (см. ГФ Х1, Т.1, с.161,162).
1)ФС Реакция образования оксалата кальция – белый осадок.

2) ФС пламя горелки – кирпично-красного цвета.
-
лактат-ион – используют его свойство окисляться за счёт спиртовой группы.
1) не ФС реакция йдоформная проба . Желтый осадок и запах йодоформа.
CH3CH(OH)COOН + 3I2+ 5NaOH→ CHI3↓+ 3NaI + 2CH3COONa + 4H2O
2) ФС реакция основана на его окислении калия перманганатом в серной кислоте до ацетальдегида, который обнаруживается по запаху свежих яблок. Перманганат-ион (розовая окраска) восстанавливается при этом до иона марганца (II) и раствор обесцвечивается
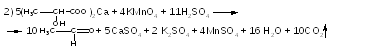
Ацетальдегид можно доказать также
-
по почернению бумажки, смоченной реактивом Несслера или темно-бурый осадок,
-
по синей окраске с нитропруссидом натрия
Чистота
-
избыточная кислотность или щелочность в пределах ФС. 5% раствор кальция лактата не должен давать розовой окраски по фенолфталеину - она должна появиться только после прибавления не более 0,6 мл 0,02 М раствора гидроксида натрия.
-
прозрачность и цветность в сравнении с эталонами.
-
допустимое содержание общих примесей: хлориды, сульфаты, тяжёлые металлы, мышьяк, железо (III).
-
«Потеря в массе при высушивании» не должна превышать30%.
Количественное определение
-
комплексонометрия в среде аммиачного буфера по индикатору кислотному хром темно-синему до сине-фиолетового окрашивания. Расчет на безводный препарат.

fэкв. ЛВ = 1, М.э =М.м
-
Пермангонатометрия
(CH3CH(OH)COO-)2Ca + (NH4)2C2O4→CaC2O4 + CH3CH(OH)COONH4
CaC2O4 +H2SO4→ H2C2O4 + CaSO4
5 H2C2O4 +2KMnO4+ 3H2SO4→ K2SO4 +2MnSO4 + 8H2O+ 10CO2
Хранение в хорошо укупоренной таре.
Применение источник кальция, антиаллергическое средство
ФП
ХII
Кальция глюконат Calcii
gluconas
(ЛН)
Calcium
Gluconate
(МНН)
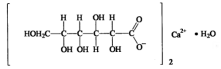
Получение
глюконата кальция – электрохимическим окислением глюкозы в присутствии бромида кальция и карбоната кальция.
CaBr2→ Ca2+ + 2Br-
катод: Са2+ + 2ē→Са
анод: 2Br- -2ē→ Br2
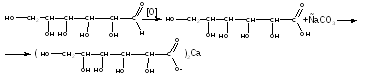

Описание
глюконат – белый зернистый или кристаллический порошок без запаха. Растворимость
Легко растворим в кипящей воде, умеренно (медленно) растворим в воде, практически нерастворим в спирте.
Подлинность
1. ФС ИК – спектр в рекомендуемых ФС условиях, который должен полностью совпадать с полосами поглощения прилагаемого рисунка спектра стандартного образца.
2. катион Ca2+по известным реакциям (см. ГФ Х1, Т.1, с.161,162).
1) ФС пламя горелки – кирпично-красного цвета.
2) ФС Реакция образования оксалата кальция – белый осадок.
3. глюконат-ион
1) ФС реакция солеобразования с хлоридом железа (III). Образуется растворимая соль, имеющая светло-зелёную окраску

2) реакция восстановления нитрата серебра в нейтральной среде!!! (в кислой и в аммиаке нет восстановления).
Чистота
-
избыточная кислотность или щелочность в пределах ФС, в 5% растворе – нейтральный на лакмус.
-
допустимое содержание общих примесей: хлориды, сульфаты, тяжёлые металлы, мышьяк, магний и щелочные металлы.
-
«Потеря в массе при высушивании» не должна превышать 1%.
-
рН раствора кальция глюконата определяют потенциометрически, его значение должно быть 6,0-7,2 (2% раствор кальция глюконата).
-
Специфические – декстрин и сахароза – реакция с реактивом Фелинга после действия НCl (кислотный гидролиз) д.б. отрицательной, не должно наблюдаться образование красного осадка.
-
Бактериальные эндотоксины (инъекционная субстанция)
Количественное определение
1. Комплексонометрия в среде аммиачного буфера по инд. кислотному хром темно-синему до сине-фиолетового окрашивания. Расчет на кристаллогидрат.
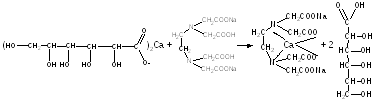 fэкв. ЛВ = 1
fэкв. ЛВ = 1
Хранение в хорошо укупоренной таре.
Применение источник кальция, антиаллергическое средство
Натрия цитрат для инъекций Natrii citras pro injectionibus (ЛН)
Sodium citrate (МНН)
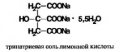
Получение
Натрия цитрат – нейтрализация лимонной кислоты карбонатом натрия до слабощелочной реакции. Источником получения кислоты лимонной являются листья хлопчатника, её содержание в них составляет 5-6%.
 лимонная кислота
натрия цитрат
лимонная кислота
натрия цитрат
Описание. Бесцветные кристаллы или белый кристаллический порошок
без запаха, выветривается на воздухе.
Растворим в воде, практически не растворим в спирте.
Подлинность
-
ФС ИК – спектр в рекомендуемых ФС условиях, который должен полностью совпадать с полосами поглощения прилагаемого рисунка спектра стандартного образца.
-
катион Na+ по известным реакциям (см. ГФ Х1, Т.1, с.161,162).
ФС пламя горелки – желтый цвет.
-
цитрат -ион –(см. ГФ Х1, Т.1).
а) ФС Реакция осаждения кальция хлоридом при нагревании. Осадок растворим в соляной кислоте
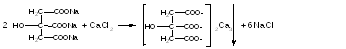
б) Реакция конденсации с уксусным ангидридом при нагревании; через 20-40 секунд появляется красное окрашивание.
Чистота
-
определяется прозрачность и цветность 10% раствора препарата
-
рН 10% раствора потенциометрически (7,8-8,3).
-
допустимое содержание общих примесей: хлориды, сульфаты, тяжёлые металлы Fe3+,Са2+,
-
мышьяк должен отсутствовать в натрия цитрате для инъекций.
-
вода - потеря в весе при высушивании или реактивом Фишера должна быть не менее 25 и не более 28%.
-
Специфические: тартраты и другие обугливающиеся примеси с концентрированной серной кислотой, окрашивание не д.превышать эталон.
