
- •1. Алкени. Гомологічний ряд алкенів.
- •Електронна будова подвійного зв’язку
- •Ізомерія
- •Одержання
- •Фізичні властивості
- •Хімічні властивості
- •Алкадієни. Реакція полімеризації. Полімери. Одержання, властивості і застосування пластмас.
- •Застосування
- •Дієнові вуглеводні (алкадієни). Типи алкадієнів.
- •Одержання алкадієнів
- •Хімічні властивості алкадієнів
- •Полімеризація дієнових сполук
- •Добування
- •Фізичні властивості алкінів
- •Хімічні властивості
- •I. Реакції приєднання:
- •1) Гідрування:
- •2) Галогенування:
- •Застосування
- •Ароматичні вуглеводні (арени)
- •Будова молекули бензолу (бензену)
- •Гомологи бензолу. Ізомерія. Гомологи бензолу можна розглядати як похідні бензолу, в яких один або декілька атомів вуглецю заміщені різними вуглеводневими радикалами.
- •Фізичні властивості
- •Хімічні властивості
- •І. Реакції заміщення:
- •1) Галогенування
- •Правила орієнтації в бензольному ядрі
Лекція №5
Ненасичені вуглеводні. Алкени. Алкадієни. Алкіни. π-звязок. Хімічні властивості та застосування. Реакція полімеризації. Ароматичні вуглеводні. Системи спряження. Правила орієнтації в ароматичному ядрі.
Ненасичені вуглеводні
До ненасичених сполук відносять алкени (олефіни, або етиленові вуглеводні), дієнові вуглеводні (алкадієни) та алкіни (ацетиленові вуглеводні). Всі ці сполуки містять подвійні або потрійні вуглець-вуглецеві зв’язки.
1. Алкени. Гомологічний ряд алкенів.
АЛКЕНИ (олефіни, або етиленові вуглеводні) містять в молекулі один подвійний зв'язок. |
Загальна формула алкенів CnH2n.
Назви алкенів утворені від грецьких і латинських числівників з додаванням суфікса –ен.
Алкени утворюють гомологічний ряд. Перший найпростіший ненасичений вуглеводень є Етилен (етен):
Електронна будова подвійного зв’язку
Розглянемо будову молекули етилену С2Н4 (СН2=СН2): у кожного атома вуглецю стають гібридними 3 електронні орбіталі, утворені 1s- і 2р - електронами (sp2- гібридизація). Гібридні орбіталі утворюють - зв’язок з атомами водню і між атомами вуглецю. Негібридні орбіталі (р - електрони) утворюють π-зв’язок між атомами вуглецю, вони знаходяться в площині, перпендикулярній площині розміщення - зв’язків.
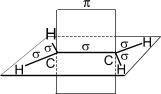
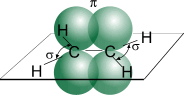
Рис.3. Утворення подвійного зв’язку в молекулі етилену
Подвійний зв’язок – це ковалентний зв’язок, який складається з одного - і одного π-зв’язку. Подвійному зв’язку відповідає sp2- гібридизація. |
Ізомерія
Для алкенів характерні два види ізомерії: структурна і просторова. Структурні ізомери – це ізомери, що мають різний порядок сполучення атомів у молекулі і різні структурні формули. Розрізняють ізомерію вуглецевого скелету та положення кратного зв’язку:
|
бутен-1 |
|
|
CH2=CH–CH2–CH3 бутен-1
|
CH3–CH=CH–CH3 бутен-2 |
Одержання
1) крекінг і піроліз нафтопродуктів;
2) дегідрогенізація алканів при підвищеній температурі в присутності каталізатора:
CH3–CH2–CH2–CH3 ––300°C,Cr2O3– бутан |
| | |
→ CH2=CH–CH2–CH3 + H2 бутен-1 → CH3–CH=CH–CH3 + H2 |
3) в лабораторії - дегідратація спиртів (відщеплення води): CH3–CH2–OH ––t°,Al2O3→ CH2=CH2 +H2О етанол етилен

CH3– |
CH–C I I |
H–CH3 (бутанол-2) CH3–CH=CH–CH3 (бутен-2) + H2O |
|
OH H |
|
Фізичні властивості
За фізичними властивостями алкени близькі до алканів, але мають більш низьку температуру кипіння і плавлення. Нищі алкени (С2-С4) за нормальних умов – гази, С5-С17 – рідини, решта – тверді речовини. Всі алкени нерозчинні у воді, але розчинні у полярних органічних розчинниках.
Хімічні властивості
Алкени відносяться до ненасичених органічних сполук. Це означає, що не всі валентні можливості алкенів використані в повному обсязі, і алкени можуть приєднувати до себе хімічні сполуки, тобто „насичуватися”. Така ненасиченість алкенів пояснюється наявністю подвійного зв’язку: розкривається π-зв’язок і утворюється два неспарених електрона, які здатні утворювати нові зв’язки.
Оскільки π-зв’язок менш міцний, ніж σ-звязок, легко розривається, тому для алкенів найбільш типовими є реакції приєднання:
1) галогенування – приєднання галогенів:
H2C=CH2 + Br2 → BrCH2–CH2Br
Якісна реакція на подвійний зв'язок - знебарвлення алкеном бромної води.
2) гідрування – приєднання водню Н2:
CH3–CH=CH2 + H2 ––Ni→ CH3–CH2–CH3
гідрогалогенування – приєднання галогеноводню НСl, HBr:
H2C=CH2 +
HBr → CH3–CH2Br

CH3−CH=CH2 + HCl → CH3− |
CH−CH3 I Cl |
4) окиснення – алкени легко окиснюються:
a) киснем повітря (реакція горіння – повнеокиснення): H2C=CH2 + 3O2 → 2CO2 + 2H2O
6) полімеризація – утворення полімеру.
