
Билет 14
1. Молочная кислота ( лактат), накапливающаяся в клетках и, особенно а интенсивно работающих скелетных мышцах, не является метаболитом, который подлежит выделению из организма человека. Из клеток ,в которых происходит анаэробный дихотомический распад глюкозы лактат поступает в кровь. Далее по крови лактат попадает в печень, где используется как субстрат для глюконеогенеза. В печени под воздействием лактатдегидрогеназы (ЛГД1,2) молочная кислота окисляется сначала до пирувата:
CH3 НАДН2 CH3
ǀ ǀ
H- C-OH НАД 3АТФ + HOH + C
ǀ ЛГД 1,2 ǀ
COOH COOH
Лактат Пируват
CH3 COOH CO2
ǀ ǀ ГФД
C=O карбоксилаза CH2 CH2
ǀ ǀ ГТФ ǀǀ
COOH C=O фосфоенолпируват C-O-PO3H2
Пируват ǀ карбоксилаза ǀ
COOH COOH
Оксалоацетат Фосфоенопируват
CH2
ǀǀ
C-O-PO3H2 фруктоза-1,6-дифосфат фруктоза-6-фосфат
ǀ фосфатаза
COOH
Фосфоенопируват
Фруктоза-6-фосфат глюкоза-6-фосфат глюкоза
Изомераза фосфатаза
2. Витамин Н(биотин, биос2) – антисеборейный витамин.
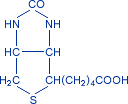
циклическое производное мочевины (имидазоловое и тиоэфирные кольца), боковая цепь которого представлена валериановой кислотой. Источники – яичный желток, печень, горох, соя. Биофун-я: определяет каталитическую активность биотиновых ферментов: пируваткарбоксилаза, ацетил-КоА-карбоксилаза, пропионил-КоА-карбоксилаза, карбомоилфосфатситетаза. Биотин является кофактором в метаболизме жирных кислот, лейцина и в процессе глюконеогенеза
3. Микросомальное окисление осущ-ся ферментнми системами, локализованными преимущественно во фракциях микросом печени и надпочечников. В процессах микросомального окисления активированный кислород непосредственно внедряется в окисляемое вещество. Микросомальное окисление- механизм использования кислорода с «пластическими» целями. Ферментативные системы, локализованные в микросомной фракции и способные использовать молекулярный кислород для окисления специфичесих органических соединений, делятся на 2 группы: диоксегеназы и монооксигеназы. Диоксегеназы катализируют реакции, в которых в мелкулу органического субстрата вкл.оба атома молекулы кислорода А+О2 АО2 . Монооксигеназы присоединяют к субстрату только 1 из двух атомов кислорода. Обычно поставщиком атомов водорода для восстановления второго атома килорода до воды служит НАДФН» анпример: RH + O2 + НАДФН2 RОH+ Н2О + НАДФ.
Оксидазного типа происходит на мемранах эндоплазматического ретикулума и во внутр.мембране митохондрии.Ферменты- Оксидазы. По строению яв-ся металлофлавопротеинами.Находятся оксидахы в пероксисомах. Отнимают Н2 от субстрата и передают его на О2 с образованием Н2О2-перикиси водорода. Эти ферменты обычно обладают широкой субстратной специфичностью и невысокой активностью.
Пероксидное окисление липидов (ПОЛ) — один из наиболее важных окислительных процессов в организме. Это естественный метаболический процесс. Он необходим для осуществления процессов обновления липидов мембран, синтеза метаболитов арахидоновой
кислоты, являющихся биорегуляторами; активации макрофагов, разрушения чужеродных веществ, попавших в организм, уничтожения переродившихся клеток и т. д. При ряде патологических состояний (хроническом стрессе, действии жесткого ультрафиолетового света, ионизирующего излучения, лучевой болезни, канцерогенезе и др.) происходит активация ПОЛ.
4. Дегидрогеназы и первичные акцепторы водорода - НАД и флавопротеиды; НАДН-дегидрогеназы. В тканях никатиновая кислота и никотинамид используется для синтеза коферментов НАД и НАДФ. Синтез НАД может идти непосредственно из триптофана через стадию образования кинуренина, 3-гидрооксикинунерина идр. НАД используется как субстрат ДНК-лигазной реакйции, т.е синтеза ДНК. НАД и НАДФ являются аллостерическими регуляторами ферментов цикла Кребса, ключевых ферментов глюконеогенеза. Никотинамидадениндинуклеоти́д (НАД, NAD) — кофермент, присутствующий во всех живых клетках, входит в состав ферментов группы дегидрогеназ, катализирующих окислительно-восстановительные реакции; выполняет функцию переносчика электронов и водорода, которые принимает от окисляемых веществ. Восстановленная форма (NADH) способна переносить их на другие вещества. Представляет собой динуклеотид, молекула которого построена из амида никотиновой кислоты и аденина, соединённых между собой цепочкой, состоящей из двух остатков D-рибозы и двух остатков фосфорной кислоты; применяется в клинической биохимии при определении активности ферментов крови. Отличие его от другого важнейшего кофермента — никотинамидадениндинуклеотидфосфата, или NADP, в том, что последний содержит в молекуле ещё один остаток фосфорной кислоты, связанной с 21-углеродным атомом рибозы. НАДН дегидрогеназа) окисляет НАД-Н, отбирая у него два электрона и перенося их на растворимый в липидах убихинон, который внутри мембраны диффундирует к комплексу III. Вместе с этим, комплекс I перекачивает 4 протона из матрикса в межмембранное пространство митохондрии.
