
- •Болезни печени
- •Стадии печёночной комы
- •Морфологические изменения в печени
- •Хронический гепатит g
- •Паразитарные поражения
- •Алкогольное поражение печени
- •Цирроз печени
- •Гемохроматоз
- •Циркуляторные расстройства в печени
- •Опухоли печени
- •Пороки развития печени
- •Поражения печени при беременности
- •Поражения печени у детей
- •Посттрансплантационные поражения печени
- •Пороки развития желчевыводящих путей
- •Болезни экзокринной части поджелудочной железы
- •Хроническая почечная недостаточность
- •Гломерулопатии
- •Классификация гломерулопатий
- •Развёрнутая классификация гломерулопатий
- •Воспалительные гломерулопатии
- •Фибромускулярная дисплазия
- •Инфаркты пoчек
- •Острый канальцевый некроз
- •Множественная миелома
- •Уратная нефропатия
- •Нефрокальциноз
- •Хронический пиелонефрит
- •Стадии хронического пиелонефрита
- •Подбор донора
- •Реакция организма реципиента
- •Отторжение трансплантата
- •Исходы и осложнения трансплантации почек
- •Почечно-клеточный рак
- •Нефробластома
- •Мезенхимальные опухоли почки
- •Кистозные болезни почек
- •Поликистозная болезнь почек взрослого типа
- •Поликистозная болезнь почек детского типа
- •Медуллярная губчатая почка
- •Нефронофтиз
- •Воспалительные заболевания
- •Опухоли лоханок и мочеточников
- •Факторы риска
- •Предопухолевые изменения
- •Пролиферативные изменения
- •Метапластические изменения
- •Опухоли мочевого пузыря
- •Доброкачественные эпителиальные опухоли
- •Злокачественные эпителиальные опухоли
- •Эндометриоз
- •Ревматизм
- •Ревматоидный артрит
- •Поражение суставов
- •Внесуставные проявления
- •Системная красная волчанка
- •Системная склеродермия
- •Поражения кожи и внутренних органов
- •Узелковый полиартериит
- •Дерматомиозит
- •Морфогенез
- •Механизмы действия возбудителей
- •Морфология инфекционных заболеваний
- •Инфекции органов дыхания
- •Парагрипп
- •Респираторно-синцитиальная инфекция
- •Аденовирусная инфекция
- •Орнитоз
- •Туберкулёз
- •Сальмонеллёз
- •Иерсиниозный энтерит
- •Кампилобактерный энтерит
- •Эшерихиозы
- •Гнойные и анаэробные инфекции
- •Скарлатина
- •Анаэробные инфекции
- •Гонорея
- •Хламидиозы
- •Паховый лимфогранулематоз
- •Трихомоноз
- •Инфекционный мононуклеоз
- •Полиомиелит
- •Ветряная оспа
- •Опоясывающий герпес
- •Болезнь лайма
- •Оппортунистические инфекции
- •Герпетическая инфекция
- •Цитомегаловирусная инфекция
- •Пневмоцистная инфекция
- •Аспергиллёз
- •Мукоромикоз
- •Кандидоз
- •Псевдомонадные инфекции
- •Амебиаз
- •Криптоспоридиоз
- •Токсоплазмоз
- •Трихинеллёз
- •Эхинококкоз
- •Цистицеркоз
- •Трахома
- •Лейшманиоз
- •Трипаносомозы
- •Шистосомоз
- •Филяриоз
- •Туляремия
- •Эпидемический возвратный тиф
- •Бруцеллёз
- •Карантинные инфекции
- •Натуральная оспа
- •Жёлтая лихорадка
- •Особенности вскрытия умерших от карантинных инфекций
- •Виды гипергликемических ком
- •Опухоли поджелудочной железы
- •Тиреоидиты
- •Опухоли щитовидной железы
- •Патология нейрогипофиза
- •Заболевания мозгового слоя надпочечников
- •Болезни шишковидной железы
- •Заболевания apud-системы
- •Множественная эндокринная неоплазия
- •Патология нейрона
- •Ноцицептивная система
- •Нейрогенные расстройства движений
- •Поражение пирамидного тракта
- •Расстройства трофической функции нервной системы
- •Алкоголизм
- •Наркомания и токсикомания
- •Объёмные внутричерепные заболевания
- •Набухание и отёк мозга
- •Гидроцефалия
- •Черепно-мозговая травма
- •Цереброваскулярные болезни
- •Инфекционные заболевания центральной нервной системы
- •Гнойные инфекции
- •Вирус ветряной оспы и опоясывающего герпеса
- •Бешенство
- •Персистирующие вирусные инфекции
- •Вирус иммунодефицита человека
- •Демиелинизирующие заболевания
- •Рассеянный склероз
- •Острый диссеминированный энцефаломиелит
- •Острый геморрагический лейкоэнцефалит
- •Витаминная недостаточность, нарушения углеводного обмена
- •Влияние злокачественных опухолей
- •Токсические и лучевые поражения
- •Алкогольные поражения
- •Нейродегенеративные процессы
- •Синдром паркинсона
- •Атаксия фридрайха
- •Врождённые аномалии развития центральной нервной системы
- •Повреждения мозга в перинатальном периоде
- •Заболевания спинного мозга
- •Опухоли центральной нервной системы
- •Нейроэпителиальные опухоли
- •Периферические невропатии
- •Опухоли периферических нервов
- •Опухоли из периферических ганглиев и параганглиев
- •Опухоли полового члена
- •Опухоли предстательной железы
- •Воспалительные заболевания
- •Опухоли
- •Заболевания оболочек яичка
- •Опухоли придатков яичек
- •Болезни шейки матки
- •Аденомиоз
- •Болезни маточных труб
- •Опухоли яичника
- •Зрелая тератома
- •Незрелая тератома
- •Дисгерминома
- •Опухоль эндодермального синуса
- •Гранулёзоклеточная опухоль взрослого типа
- •Опухоли молочной железы
- •Нарушения кровообращения
- •Плаценты близнецов
- •Поздний гестоз
- •Трофобластическая болезнь
- •Пузырный занос
- •Инвазивный пузырный занос
- •Хориокарцинома
- •Трофобластическая опухоль плацентарного ложа
- •Дисплазии
- •Хрящеобразующие опухоли
- •Костномозговые опухоли
- •Патогенез
- •Спондилоартропатии
- •Дистрофические заболевания суставов
- •Травмы костей
- •Асептический остеонекроз
- •Опухоли суставов
- •Опухолеподобные поражения суставов
- •Воспалительные и токсические миопатии
- •Псевдопаралитические миастении
- •Опухоли мягких тканей
- •Патология перинатального периода
- •Нарушения внутриутробного развития плода
- •Родовая травма
- •Инфекционные болезни плода и новорождённого
- •Гемолитическая болезнь новорождённых
- •Прочие болезни перинатального периода
- •Опухоли детского возраста
- •Классификация опухолей у детей
- •Синдром внезапной смерти младенцев
- •Нарушения пигментации кожи
- •Пигментный невус
- •Меланома
- •Предраковые заболевания кожи
- •Злокачественные эпителиальные опухоли
- •Заболевания и опухоли из придатков кожи
- •Эритема
- •Дерматиты
- •Изменения кожи при заболеваниях соединительной ткани
- •Красная волчанка
- •Грибковые инфекции
- •Паразитарные заболевания кожи
- •Патология органа зрения
- •Инфекционные заболевания глаза
- •Инфекционные заболевания роговицы и конъюнктивы
- •Инфекционные заболевания увеального тракта глазного яблока
- •Заболевания уха
- •Острая кишечная непроходимость
- •Классификация острой кишечной непроходимости
- •Септицемия
- •Хрониосепсис
- •Патоморфоз сепсиса
- •Генные болезни
- •Аутосомно-сцепленные врождённые пороки развития
- •Фенилкетонурия
- •Галактоземия
- •Хромосомные болезни
- •Синдромы, связанные с аномалиями половых хромосом
- •Мутации митохондриальных генов
- •Импринтинг генома
- •Болезни с наследственной предрасположенностью
- •Влияние генетических факторов на фармакодинамику
Воспалительные гломерулопатии
Воспалительные гломерулопатии (гломерулонефриты) — группа заболеваний с воспалительными изменениями клубочков, диффузной или очаговой пролиферацией их клеток.
Клинически для гломерулонефритов характерен нефритический синдром. Однако во многих случаях, особенно при незначительных изменениях клубочков преобладает часть нефритического синдрома (например, гематурия или протеинурия).
Патоморфология. При увеличении клеточности клубочков за счёт пролиферации мезангиальных клеток нефрит называют мезангиально-пролиферативным. Наличие пролиферации эндотелия, наряду с пролиферацией мезангиальных клеток, говорит об интракапиллярном пролиферативном гломерулонефрите. При некоторых формах гломерулонефрита, особенно у детей, возможно появление в клубочках нейтрофильных лейкоцитов. Пролиферация эпителиальных клеток (подоцитов и пристеночных, выстилающих капсулу почечного тельца) в ответ на повреждение ведёт к формированию полулуний. Это экстракапиллярный пролиферативный гломерулонефрит (гломерулонефрит с полулуниями).
Воспалительные изменения в клубочках могут быть связаны с иммунологическими механизмами, тромботическими осложнениями и др. Наиболее распространены и изучены иммунологические механизмы повреждения клубочков, представленные следующими основными типами:
отложения циркулирующих иммунных комплексов в клубочках;
образование иммунных комплексов на месте;
активация комплемента по альтернативному пути;
клеточно-опосредованные иммунные реакции.
Гломерулонефрит, связанный с отложением циркулирующих иммунных комплексов в клубочках, можно вызвать введением кролику чужеродного белка (например, бычьего альбумина). В течение 10–14 дней антитела против этого белка образуются в количестве, достаточном для связывания избытка антигена. При электронной микроскопии иммунные комплексы видны как субэпителиальные «горбы», а при иммунофлюоресцентном исследовании (с анти-IgG-и анти-С3-сыворотками) видно периферическое гранулярное свечение. Чаще иммунные комплексы не проникают сквозь базальную мембрану клубочков, оседая в субэндотелиальной зоне или мезангии. Локализация оседающих в клубочках иммунных комплексов зависит от многих факторов: размера и заряда комплексов, клубочковой гемодинамики, наличия вазоактивных веществ, функции мезангия, постоянства заряда гломерулярного барьера. Антигены могут быть экзогенного (антиген стрептококка, вируса гепатита В) и эндогенного происхождения (ДНК при развитии волчаночного нефрита). Этот механизм представлен при остром постинфекционном гломерулонефрите.
При образовании комплексов «антиген-антитело» на месте циркулирующие антитела связываются либо с собственными антигенами клубочков (аутоантитела), либо с антигенами, фиксированными в клубочках (антигены бактерий, вирусов, ДНК, сами иммуноглобулины). Наиболее известный пример нефрита этой группы — синдром Гудпасчера (антиген — глобулярный домен коллагена IV типа). При иммуногистохимическом исследовании в этих случаях выявляют линейные отложения IgG. Образование комплексов «антиген-антитело» ведёт к активации комплемента и развитию быстропрогрессирующего гломерулонефрита. Другой пример — нефрит Хеймана (аналог идиопатической мембранозной нефропатии). Альтернативный путь активации комплемента представлен в патогенезе мезангиокапиллярного гломерулонефрита и болезни Берже.
Нет прямых доказательств того, что клеточно-опосредованные реакции служат механизмом развития какой-либо формы гломерулонефрита у человека. Однако иногда обнаруживают мононуклеарную инфильтрацию клубочков при отсутствии отложений иммуноглобулина. Непрямые доказательства участия клеточно-опосредованного иммунитета получены в экспериментах, когда лимфоциты больных гломерулонефритом in vitro взаимодействуют с антигенами клубочков.
Острый постинфекционный гломерулонефрит
Острый постинфекционный (диффузный пролиферативный) гломерулонефрит — следствие различных инфекций (стафилококк, пневмококк, спирохеты, вирусы), наиболее часто его вызывает β-гемолитический стрептококк группы А. У этого заболевания клинически внезапное начало с развитием нефритического синдрома, а морфологические изменения в почках представлены диффузным увеличением количества клеток в клубочках.
Этиология и патогенез. Гломерулонефрит вызывают только определённые типы β-гемолитического стрептококка группы А (в 90% случаев это типы 12, 4 и 1). Продолжительность латентного периода обычно 9–14 дней. У большинства больных при этом повышен титр антител к одному или нескольким антигенам стрептококка. Снижение уровня комплемента в плазме говорит об участии системы комплемента. Появление гранулярных иммунных депозитов в клубочках предполагает роль в патогенезе иммунных комплексов (при электронной микроскопии электронноплотные депозиты выявляют на эпителиальной стороне базальной мембраны капилляров). Антиген стрептококка часто не удаётся идентифицировать. Это может быть связано с их быстрым выведением из повреждённых клубочков или «маскировкой» иммуноглобулинами и комплементом.
Гломерулярная базальная мембрана и иммуноглобулины, повреждённые ферментом стрептококка нейраминидазой, также способны участвовать в патогенезе острого гломерулонефрита как антигены (одновременно с антигенами стрептококка или в разное время).
Клинические признаки: острый нефритический синдром с олигурией, протеинурией, гематурией, развитием отёков и артериальной гипертензии через 9–14 дней после перенесённых фарингита, ангины или поражений кожи в виде пиодермии, импетиго, рожи. Серологически обнаруживают антитела к антигенам стрептококка, часто снижение сывороточного компонента С3 комплемента в остром периоде. У большинства больных изменения возвращаются к норме через 2–4 нед.
Патоморфология. Почки несколько увеличены в размерах, набухшие, кора серовато-коричневая с мелким красным или бледно-серым крапом на поверхности и разрезе, пирамиды тёмно-красные (большая пёстрая почка).
В течение первых 3–4 нед заболевания видны следующие изменения:
диффузное увеличение размеров клубочков и их отёчность;
пролиферация клеток эндотелия и мезангия, инфильтрация нейтрофилами и макрофагами;
облитерация просветов капилляров.
Клубочки в патологический процесс вовлечены целиком, иногда подчёркнута дольчатость клубочка или в отдельных клубочках формируются полулуния. В гломерулярной базальной мембране изменений нет. При трёхцветной окраске выявляют фуксинофильные, расположенные субэпителиально «горбы» (рис. 15-4).
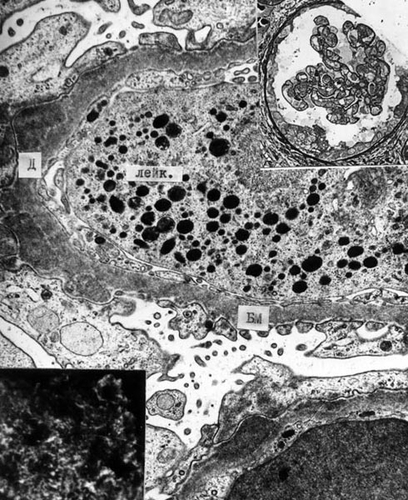
Рис. 15-4. Диффузный пролиферативный гломерулонефрит (монтаж): а) гистологическая картина пролиферативного гломерулонефрита (окраска по Джонсу–Моури, x200); б) иммунные депозиты гранулярного вида, содержащие комплемент (прямой метод Кунса, x400); в) субэпителиальные депозиты (д) на базальной мембране капилляров, нейтрофильный лейкоцит в просвете капилляра (x15 000).
Тубулоинтерстициальные изменения незначительны, очаговые изменения представлены атрофией канальцев, межуточным отёком и лимфоидной инфильтрацией. В просветах канальцев можно обнаружить эритроцитарные цилиндры. Сосуды не изменены.
Обратное развитие морфологических изменений происходит быстро, примерно к 8 нед с начала заболевания. Однако незначительное диффузное накопление мезангиального матрикса и мезангиальная пролиферация могут сохраняться годами при отсутствии клинических и лабораторных проявлений. Тяжёлое повреждение клубочков с появлением большого количества полулуний редко, у таких больных быстро прогрессирует почечная недостаточность.
Иммуногистохимически типичны гранулярные отложения IgG и С3 вдоль базальных мембран клубочков (соответственно положению фуксинофильных «горбов»), а также мезангиальные отложения. Иногда в клубочках обнаруживают отложения IgM и С4.
Характерное изменение при электронной микроскопии — субэпителиальные «горбы» из электронноплотного материала, иногда в сочетании с субэндотелиальными и мезангиальными депозитами. Количество депозитов соответствует выраженности воспалительной инфильтрации клубочков.
Прогноз благоприятный. Отложение иммунных комплексов кратковременно, почечная недостаточность развивается редко.
Мезангиокапиллярный гломерулонефрит
Мезангиокапиллярный (мембранозно-пролиферативный) гломерулонефрит характеризуют утолщение и диффузное удвоение базальной мембраны, пролиферация мезангиальных клеток. Заболевание проявляется нефротическим синдромом. Отличие от невоспалительных первичных гломерулопатий — увеличение количества гломерулярных клеток. Микроскопическая картина мембранозно-пролиферативного нефрита однотипна. Клубочки с увеличенным количеством клеток (больше за счёт пролиферации мезангиоцитов) имеют подчёркнутую дольчатость сосудистых петель.
Клинически характерен нефротический и/или нефритический синдром (острое или подострое снижение скорости клубочковой фильтрации, изменение осадка мочи, массивная протеинурия). У большинства пациентов мезангиокапиллярный гломерулонефрит прогрессирует, приводя к развитию ХПН, несмотря на проводимую терапию.
Выделяют три разновидности мезангиокапиллярного гломерулонефрита.
● Тип 1 — гломерулонефрит с субэндотелиальными депозитами. Характерны субэндотелиальные и мезангиальные отложения.
◊ Этиология и патогенез. В большинстве случаев этот тип гломерулонефрита — идиопатический, у части больных ассоциирован с вирусами гепатита В, С, Эпстайна–Барр, бактериальным эндокардитом, стрептококковой инфекцией, новообразованиями. Иногда обнаруживают циркулирующие иммунные комплексы (классический путь активации комплемента). Участие антигенов в патогенезе не доказано.
◊ Патоморфология. Почки плотные, бледные с жёлтыми пятнами в корковом веществе. При длительном течении прогрессивно уменьшаются в размерах. Клубочки диффузно увеличены, заметна мезангиальная пролиферация, особенно центролобулярная, что подчёркивает дольчатость клубочка (лобулярный гломерулонефрит), пролиферация эндотелиальных клеток (рис. 15-5). Просветы капилляров при этом резко сужены или совсем не видны. Наблюдают также инфильтрацию клубочков макрофагами, увеличение мезангиального матрикса. Выявляют субэндотелиальные и мезангиальные фуксинофильные отложения, утолщение и удвоение контуров базальной мембраны («трамвайные рельсы» при импрегнации серебром) с распространением клеток мезангия и матрикса на периферию капиллярных петель. При этом под эндотелием откладывается вещество новой базальной мембраны (интерпозиция мезангия). Иммуногистохимически в большинстве случаев обнаруживают гранулярные отложения IgG, IgM, С3 (часто с C1q и/или С4) в капиллярных петлях и мезангии. При электронной микроскопии видны интерпозиция мезангия, типичные субэндотелиальные и мезангиальные плотные депозиты, иногда субэпителиальные «горбы». Ножки подоцитов, как правило, сглажены.

Рис. 15-5. Мезангиокапиллярный гломерулонефрит (монтаж): а) гистологическая картина мезангиокапиллярного гломерулонефрита (окраска гематоксилином и эозином, x200); б) иммунные депозиты в мезангии (мезангиальный вид), содержащие IgA (прямой метод Кунса, x400); в) неравномерное утолщение базальных мембран капилляров, гипертрофия мезангиальной клетки (Мк) с образованием мембраноподобного вещества и «выселение» отростков этих клеток на периферию капиллярной петли (x13 000).
◊ Исходы и осложнения. Прогноз неблагоприятный, у большинства больных процесс прогрессирует. Исход — вторично сморщенная почка и ХПН.
● Тип 2 — болезнь плотных депозитов. Характерны лентовидные зоны повышенной плотности в центральных участках утолщённой гломерулярной базальной мембраны.
◊ Этиология и патогенез. Этот гломерулонефрит — аутоиммунное заболевание. В крови больных определяют аутоантитела (IgG-С3-нефритический фактор), ответственные за активацию системы комплемента по альтернативному пути. Эти аутоантитела связываются с С3-конвертазой, активирующей С3 с образованием С3b-компонента. Конвертаза под действием С3-нефритического фактора становится устойчивой к инактивации, поддерживаемой пропердином. Клинические проявления гломерулонефрита типа 2 аналогичны типу 1. Циркулирующие иммунные комплексы у пациентов выявляют не часто.
◊ Патоморфология. Макро- и микроскопические изменения аналогичны описанным при гломерулонефрите типа 1. Однако увеличение клеточности при гломерулонефрите типа 2 более разнообразно в разных клубочках. Интерпозиция мезангия (двухконтурность базальной мембраны при серебрении) бывает реже. Иммуногистохимически, в отличие от типа 1, выявляют только псевдолинейные, часто прерывистые отложения С3 в капиллярных петлях, очень редко иммуноглобулины и другие компоненты комплемента (C1q, C4). При электронной микроскопии патогномоничны лентовидные зоны повышенной плотности в центральных участках утолщённой гломерулярной базальной мембраны (болезнь электронноплотных депозитов). Электронноплотные отложения появляются также в мембранах капилляров вокруг канальцев, в эластических мембранах артериол.
◊ Исходы и осложнения. Прогноз неблагоприятный, у большинства больных процесс прогрессирует, несмотря на проводимое лечение. Исход — вторично сморщенная почка и ХПН.
● Тип 3 — диффузный мезангиокапиллярный гломерулонефрит. Сочетание изменений, характерных для типов 1 и 2. При электронной микроскопии часто обнаруживают субэндотелиальные, мезангиальные и субэпителиальные депозиты.
Экстракапиллярный пролиферативный гломерулонефрит
Экстракапиллярный пролиферативный гломерулонефрит (быстропрогрессирующий, подострый, злокачественный, гломерулонефрит с полулуниями) — тяжёлая форма, когда большинство клубочков окружено скоплениями клеток в капсуле почечного тельца. Полагают, что первичен разрыв стенки капилляра, после чего в полость эпителиальной капсулы проникают иммунные комплексы и моноциты, образуя полулуния. Моноциты превращаются в макрофаги и по наружному листку эпителиальной капсулы вместе с клетками последней образуют скопление эпителиоидных клеток (как при образовании гранулём). Это скопление имеет форму полулуния и постепенно сдавливает капиллярный клубочек, серьёзно затрудняя и даже прекращая образование первичной мочи с развитием олигурии и анурии. Такой гломерулонефрит обычно начинается как очаговый и сегментарный гломерулит. Происходит спадение и пропитывание фибрином капиллярных петель. При прогрессировании процесса полулуния приобретают фиброзный характер. В финале клубочек полностью облитерирован.
Образование полулуний может быть проявлением многих заболеваний, поэтому для диагностики необходимо использование и других критериев, представленных в табл. 15-1.
Таблица 15-1. Дифференциальная диагностика гломерулонефритов с полулуниями
Гломерулонефрит |
Световая микроскопия |
Электронная микроскопия |
Иммунофлюоресцентный метод |
Идиопатический (малоиммунный) гломерулонефрит с полулуниями |
Полулуния и пролиферация клеток клубочка |
Нет изменений |
Нет изменений |
Анти-ГБМ-гломерулонефрит |
Полулуния и сегментарная пролиферация клеток клубочка |
Нет изменений |
Линейные отложения IgG и C3 |
Постинфекционный гломерулонефрит |
Полулуния, пролиферация клеток клубочка, экссудативные изменения |
Интракапиллярные депозиты и субэпителиальные «горбы» |
Периферические гранулярные отложения IgG и С3 |
Мембранозно-пролиферативный гломерулонефрит |
Полулуния, подчёркнутая дольчатость клубочков, интерпозиция мезангия |
Субэндотелиальные депозиты, интерпозиция мезангия |
Периферические гранулярные отложения С3 и пропердина |
IgA-нефропатия/ пурпура Шёнляйна–Геноха |
Полулуния и пролиферация клеток клубочка |
Мезангиальные депозиты |
Мезангиальные отложения IgA, иногда в сочетании с С3, IgG, IgM |
Системная красная волчанка |
Полулуния, феномен «проволочных петель», гематоксилиновые тельца
|
Субэндотелиальные, мезангиальные, перитубулярные депозиты, депозиты в виде отпечатков пальцев, |
Мезангиальные, периферические отложения IgG, IgA, IgM, C3, C4, C1q |
Системный васкулит |
Полулуния и фокальный артериит |
Нет изменений |
Нет изменений |
Этиология и патогенез. В 40% случаев быстропрогрессирующий гломерулонефрит связан с системными заболеваниями, в 60% это первичные поражения почек (половина из них — идиопатические, треть связана с антителами к базальной мембране клубочков, остальные — с иммунными комплексами).
● Идиопатический (малоиммунный) гломерулонефрит с полулуниями. Диагноз устанавливают, если исключено участие в патогенезе иммунных комплексов и отсутствует васкулит. Иммунные комплексы в клубочках при этом обнаруживают очень редко или не обнаруживают совсем.
◊ Важный патогенетический фактор формирования полулуний — выход фибрина в просвет капсулы почечного тельца, постоянно присутствующий при этом типе гломерулонефрита. Применение антикоагулянтов для лечения экспериментального быстропрогрессирующего гломерулонефрита предотвращает накопление фибрина и пролиферацию эпителиальных клеток капсулы. Вероятно, фибрин и другие белки плазмы крови, ответственные за формирование полулуний, попадают в просвет капсулы через разрывы воспалённых капилляров клубочков (подтверждение — частая связь полулуний с полями сегментарного некроза в клубочках). Фибрин и его компоненты также стимулируют миграцию макрофагов. Макрофаги, пролиферирующие эпителиальные клетки и полиморфноядерные лейкоциты образуют клеточные, позднее фиброзно-клеточные, или фиброзно-эпителиальные полулуния (в состав последних входят фибробласты).
◊ Клиническая картина быстропрогрессирующего гломерулонефрита (почечная недостаточность, злокачественная артериальная гипертензия, отёки, протеинурия).
◊ Патоморфология. Почки увеличены, дряблые, кора широкая, жёлто-серая, тусклая с красным крапом, резко отграничена от тёмно-красных пирамид (большая пёстрая почка) или красная, сливается с пирамидами (большая красная почка). Полулуния могут занимать только часть пространства капсулы или полностью окружать клубочек (рис. 15-6). Их развитие проходит несколько стадий: от клеточных полулуний к фиброзно-клеточным, а затем фиброзным. Клетки полулуний имеют разную форму, от веретёновидных до овоидных, часто смешаны с макрофагами и фибрином. Нередко видны фигуры митозов и гигантские многоядерные клетки. В течение нескольких недель в полулуниях происходит образование соединительной ткани и матрикса, хорошо заметного при серебрении. В итоге сегментарные полулуния обнаруживают в клубочках или их капсуле (очаги сегментарного склероза). Полулуния, полностью окружающие клубочки, вызывают тотальный склероз. Также происходят отёк, инфильтрация и склероз стромы, атрофия канальцев.

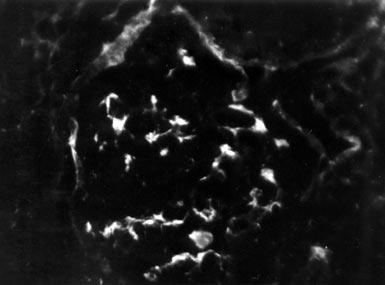
Рис. 15-6. Экстракапиллярный пролиферативный гломерулонефрит: а) пролиферация нефротелия с образованием полулуний, выраженная пролиферация эндотелиальных и мезангиальных клеток (окраска гематоксилином и эозином, x200); б) иммунные депозиты очагового линейного вида на базальных мембранах капилляров клубочка, содержащие IgG (прямой метод Кунса, x250).
◊ Исход — вторично сморщенная почка, раннее развитие почечной недостаточности.
● Анти-ГБМ-гломерулонефрит — аутоиммунное заболевание, разновидность гломерулонефрита с полулуниями.
◊ Этиология и патогенез. Анти-ГБМ-нефрит — заболевание, вызываемое антителами против компонентов клубочковой базальной мембраны (глобулярного домена коллагена типа IV). У всех пациентов с этим заболеванием в крови находят специфические антитела одного типа. Иммунная атака приводит к развитию быстропрогрессирующего гломерулонефрита с полулуниями. Среди больных анти-ГБМ-нефритом 80% мужчин, их средний возраст к началу заболевания — 29 лет. Из-за перекрёстного реагирования антител с альвеолярными базальными мембранами у многих пациентов одновременно с почечной симптоматикой развиваются лёгочные кровотечения, иногда угрожающие жизни. Одновременное поражение почек и лёгких — синдром Гудпасчера.
Ä Синдром Гудпасчера — аутоиммунное заболевание, проявляющееся лёгочным кровотечением и тяжёлым прогрессирующим гломерулонефритом. В крови циркулируют антитела к коллагену типа IV базальной мембраны почечных клубочков (антиген Гудпасчера). Поражение лёгких опережает поражение почек. Клинические признаки: повторные лёгочные кровотечения с развитием дыхательной недостаточности, быстропрогрессирующий гломерулонефрит (гематурия, протеинурия, антитела против антигена базальной мембраны клубочков), почечная недостаточность, гриппоподобный синдром (лихорадка, миалгии, артралгии, слабость).
◊ Патоморфология. Специфические для анти-ГБМ-гломерулонефрита изменения выявляют только при иммуногистохимическом исследовании (рис. 15-7). Это характерные линейные отложения IgG и С3 в базальной мембране капиллярных петель клубочков. Линейные отложения IgG иногда определяют и при других заболеваниях почек (диабетическая нефропатия). Однако при сахарном диабете линейные отложения не отражают специфическую иммунную реакцию, обычно содержат альбумины и фибриноген. Диагноз анти-ГБМ-гломерулонефрита устанавливают при обнаружении взаимодействия плазмы пациента с нормальными базальными мембранами человека.
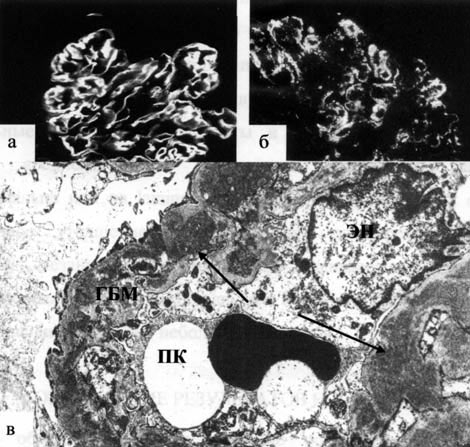
Рис. 15-7. Экстракапиллярный пролиферативный гломерулонефрит (монтаж): а) иммунные депозиты линейного вида на гломерулярной базальной мембране (ГБМ) клубочка, содержащие IgG (прямой метод Кунса, x250); б) иммунные депозиты гранулярного характера на гломерулярной базальной мембране (ГБМ) и в мезангии, содержащие IgA (прямой метод Кунса, x250); в) субэндотелиальные и интрамембранозные депозиты, интерпозиция мезангия (x6100). ПК — просвет капилляра.
◊ Исходы и осложнения аналогичны описанным выше при экстракапиллярном пролиферативном гломерулонефрите. У большинства пациентов с анти-ГБМ-нефритом ремиссия наступает при иммуносупрессивной терапии и переливании препаратов плазмы (улучшение функции почек, прекращение кровохарканья). Лечение более эффективно на ранних стадиях заболевания, до полного формирования полулуний и развития почечной недостаточности.
● IgA-нефропатия (болезнь Берже) — аутоиммунное заболевание. Как особая форма была выделена менее 30 лет назад, когда появилась возможность иммунофлюоресцентного исследования. Характерно появление IgA в мезангии, отсутствие клинических признаков поражения других органов. В некоторых странах — самая частая форма гломерулонефрита.
◊ Этиология и патогенез болезни Берже неясны. Считают, что главную роль играют иммунные комплексы, содержащие IgA, обнаруживаемые у взрослых пациентов. В 70% случаев в крови находят агрегаты из IgA и фибронектина. Кроме осаждения циркулирующих иммунных комплексов в мезангии, возможно их образование на месте. При болезни Берже также встречают аутоантитела к ядерным антигенам и компонентам клубочка. Антигенная гипотеза связывает возникновение IgA-нефропатии с вирусными, бактериальными и пищевыми антигенами. Возможность участия инфекционных агентов объясняет частоту рецидивов гематурии после перенесённых инфекций респираторных путей, желудочно-кишечного тракта. Роль пищевых антигенов подтверждают развитие нефропатии у больных с глютенчувствительной энтеропатией (целиакией) и обнаружение в мезангии некоторых белков молока. Иммунные комплексы, содержащие IgA, активируют в мезангии комплемент по альтернативному пути (в мезангии обнаруживают IgA, С3 и пропердин, тогда как C1q и С4, ответственные за классический путь активации, отсутствуют). Определённую роль в развитии IgA-нефропатии играет генетическая предрасположенность: у пациентов выявлено увеличение частоты HLA-DR4.
◊ Клиническая картина. IgA-нефропатию наиболее часто диагностируют у молодых мужчин в возрасте 15–30 лет. Формы заболевания: рецидивирующая макрогематурия (у 90% больных) и бессимптомная микрогематурия со слабой протеинурией. Иногда заболевание проявляется острой и хронической почечной недостаточностью, тяжёлой артериальной гипертензией или нефротическим синдромом (менее 20%), что ухудшает прогноз.
◊ Патоморфология. Почки бледные, плотные, с жёлтым крапом в коре. В большинстве случаев основное и единственное проявление патологии клубочков — мезангиальная пролиферация, а также расширение мезангиальных пространств и накопление матрикса. В тяжёлых случаях в клубочках видны сегментарные некрозы, полулуния и склероз. Обычен также «гиалиновый материал» в мезангии (иммунные депозиты и диффузные, иногда неправильно распределённые отложения IgA) или его набухание (может быть единственным признаком повреждения). Иммуногистохимически обнаруживают гранулярные мезангиальные отложения IgA и компонента С3 комплемента, реже IgG. Отложения IgA в стенках капилляров клубочков встречают в тяжёлых случаях. Электронная микроскопия выявляет увеличение мезангиального матрикса и мезангиальной клеточности, электронноплотные депозиты в мезангии (типично их расположение непосредственно под парамезангиальной базальной мембраной).
◊ Исходы и осложнения. Заболевание, в основном, имеет доброкачественное течение, 20-летняя выживаемость составляет около 50%. У меньшей части больных (20%) развивается почечная недостаточность, в этих случаях показана трансплантация почки. IgA часто обнаруживают в трансплантате после пересадки, однако функция трансплантата при этом не нарушена. Прогностически неблагоприятные факторы: пожилой возраст в начале заболевания, выраженная протеинурия, артериальная гипертензия, обнаружение полулуний или сегментарного склероза при биопсии почки.
Диффузный фибропластический гломерулонефрит
Диффузный фибропластический (терминальный) гломерулонефрит, или диффузный склероз почки — последняя стадия развития многих форм, её характеризуют полный склероз большинства клубочков (резкое увеличение количества мезангиального матрикса) и гиалиноз (повышение синтеза материала базальной мембраны) В меньшей степени процесс зависит от разрастания фибрилл коллагена. Также наблюдают интерстициальный фиброз. Клинические признаки: протеинурия и ХПН.
Мезангиопролиферативный гломерулонефрит
Характерна диффузная или очаговая пролиферация мезангиоцитов, очаговое утолщение и удвоение базальной мембраны капилляров. Эти морфологические изменения бывают при большом количестве заболеваний с разным патогенезом, клиническим течением и прогнозом.
Мезангиопролиферативный гломерулонефрит может быть проявлением наследственных гломерулопатий (синдром Альпорта, болезнь тонких гломерулярных мембран), остаточных явлений острого гломерулонефрита, других первичных (болезнь Берже, IgM-нефропатия) или вторичных (системная красная волчанка, болезнь Шёнляйна–Геноха) гломерулонефритов.
Клинические признаки: протеинурия, гематурия, артериальная гипертензия, изменение скорости клубочковой фильтрации. Патоморфология: пролиферация мезангиальных клеток и матрикса.
● Очаговый сегментарный мезангиопролиферативный гломерулонефрит. Клинические признаки выражены слабо или умеренно: изменение осадка мочи, снижение скорости клубочковой фильтрации различной степени. Патоморфологические изменения: сегментарные участки пролиферации и некроза занимают менее 50% клубочков, иногда с образованием полулуний.
● IgM-нефропатия. У части больных мезангиально-пролиферативным гломерулонефритом при иммунофлюоресцентном исследовании определяют отложения только IgM. Такие случаи клинически протекают более тяжело, часто с развитием нефротического синдрома, резистентного к терапии глюкокортикоидами, быстрым развитием артериальной гипертензии и почечной недостаточности. Эти особенности течения позволили выделить IgM-нефропатию как отдельную разновидность мезангиопролиферативного гломерулонефрита.
Диагностические критерии гломерулопатий с мезангиальной пролиферацией отражены в табл. 15-2.
Таблица 15-2. Дифференциальная диагностика гломерулопатий с мезангиальной пролиферацией
Заболевание |
Метод иммунофлюоресценции |
Электронная микроскопия |
Клинико-лабораторные проявления |
Болезнь тонких базальных мембран |
Иммунные депозиты не видны |
Истончение lamina densa ГБМ |
Возрастная гематурия, реже протеинурия |
Синдром Альпорта |
Иммунные депозиты не видны |
Расщепление lamina densa ГБМ |
Возрастная гематурия, реже протеинурия, ухудшение функции почек |
Бактериальный эндокардит |
Отложения IgG, C3 в мезангии |
В мезангии пролиферация и электронноплотные депозиты |
Лихорадка, выделение культур микроорганизмов из крови |
Волчаночный нефрит |
Отложения IgG, C3 в мезангии |
В мезангии пролиферация и электронноплотные депозиты |
Системные проявления, антитела к двухцепочечной ДНК |
Острый гломерулонефрит, выздоровление |
Отложения IgG, C3, реже IgM в мезангии |
Мезангиальная пролиферация |
Минимальные изменения в моче (протеинурия, микрогематурия) |
ВТОРИЧНЫЕ ГЛОМЕРУЛОПАТИИ
Вторичные гломерулопатии — группа системных заболеваний, поражающих клубочки почек.
АМИЛОИДНАЯ НЕФРОПАТИЯ
Для амилоидоза почек характерно отложение в них внеклеточных белков, обладающих общими морфологическими свойствами (специфическое окрашивание конго красным, характерное свечение в поляризованном свете). Амилоидоз развивается при многих заболеваниях. Отложение амилоида возможно в разных тканях, что вызывает их сдавление и нарушение функций. Почки, в первую очередь клубочки, почти всегда бывают поражены при системном амилоидозе. В результате возникают повышение проницаемости клубочкового фильтра и протеинурия.
Этиология и патогенез амилоидоза рассмотрены в главе 6.
Клиническое проявление амилоидоза почек — неселективная протеинурия (т.е. в моче примерно равное количество альбуминов и глобулинов). Приблизительно у 60% пациентов тяжёлая протеинурия приводит к развитию нефротического синдрома, гематурия бывает редко. Постоянно наблюдают нефрогенную артериальную гипертензию.
Патоморфология. Стадии амилоидной нефропатии: латентная, протеинурическая, нефротическая, азотемическая (уремическая).
● Протеинурическая стадия: увеличение и уплотнение почек, поверхность их бледно-cерая или жёлто-серая, на разрезе характерный сальный блеск, кора широкая, матовая, пирамиды серо-розовые (большая сальная почка).
● Нефротическая стадия: почки большие, плотные, восковидные, серо-розового цвета, граница между корковым и мозговым веществом стёрта (большая белая почка).
● Азотемическая стадия: почки обычных размеров или несколько уменьшены, очень плотные, с множеством рубцовых западений на поверхности (амилоидно-сморщенная почка).
Стадии амилоидной нефропатии по данным световой микроскопии.
● Латентная стадия. Утолщение и двухконтурность гломерулярной мембраны капилляров. Цитоплазма эпителия и просветы канальцев содержат большое количество белковых гранул, отложения белков находят в строме мозгового вещества.
● Протеинурическая стадия. Отложения амилоида в клубочках преимущественно мезангиальные, что вызывает их диффузное расширение без увеличения клеточности. Это быстро приводит к облитерации просветов капилляров. Отложение амилоида наблюдают и в артериолах. В строме мозгового вещества развивается склероз.
● Нефротическая стадия. Отложения амилоида приобретают вид узловых масс эозинофильного материала, что может напоминать диабетический гломерулосклероз. Однако амилоид можно окрасить конго красным, при этом он даёт зеленоватое свечение в поляризованном свете. Амилоид обнаруживают в капиллярных петлях большинства клубочков, артериолах, артериях, мембранах канальцев. Просвет канальцев расширен, забит цилиндрами, в их эпителии много липидов. Диффузный склероз стромы мозгового вещества (рис. 15-8).
● Конечная стадия амилоидоза. Структуры клубочков облитерированы, клубочки выглядят, как крупные аморфные эозинофильные шарики. Склероз стромы охватывает и корковое, и мозговое вещество.
Антитела против К- и Х-цепей, и сывороточного белка SAA позволяют иммуногистохимически отличать формы амилоидоза. Часто в клубочках обнаруживают неспецифические отложения иммуноглобулинов и других белков плазмы крови.
Электронная микроскопия — надёжный метод выявления амилоида, имеющего вид линейных фибрилл (рис. 15-8). Впервые фибриллы можно увидеть в мезангиальных полях, при этом малые ножки подоцитов отделены от базальной мембраны и сглажены. Эпителиальные клетки отодвинуты фибриллами амилоида, часто направленными перпендикулярно к базальной мембране. Тяжесть повреждения эпителиальных клеток соответствует уровню протеинурии.
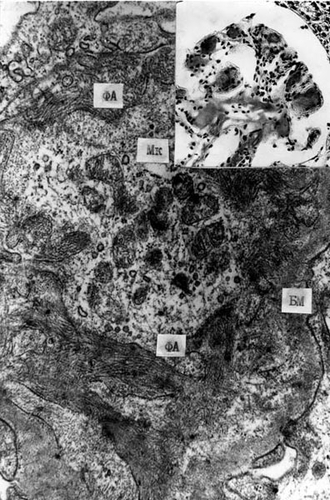
Рис. 15-8. Амилоидоз почек. Фибриллы амилоида (ФА) в мезангии и базальной мембране (БМ) капилляров клубочка (x20 000). На врезке: амилоидные массы в капиллярах клубочка и приносящей артериоле (окраска Конго красным, x360). Мк — мезангиальная клетка.
Исходы и осложнения: острая или хроническая почечная недостаточность, инфекции (пневмония, рожа, паротит), инфаркты, кровоизлияния, сердечная недостаточность. Прогноз неблагоприятный.
РЕНОВАСКУЛЯРНАЯ ГИПЕРТЕНЗИЯ
Этот синдром, связанный со стенозом или полной облитерацией просвета почечных артерий, приводит к возникновению артериальной гипертензии, излечимой при восстановлении проходимости сосудов. В большинстве случаев (90–95%) причина реноваскулярной гипертензии — атеросклероз. С этим связана наибольшая частота развития синдрома у мужчин старше 55 лет.
Патогенез артериальной гипертензии при стенозе почечных артерий связан с гиперплазией юкстагломерулярного аппарата, что вызывает усиление продукции ренина, ангиотензина II и альдостерона, задержку натрия и воды, и, в результате, основной клинический симптом — повышение АД.
Патоморфология. Если стеноз почечной артерии возникает вследствие атеросклероза, атеросклеротическая бляшка располагается обычно в области устья, приводя к сужению проксимальной части сосуда. Левая артерия бывает поражена чаще, чем правая. Иногда развитие стеноза почечных артерий связано с формированием аневризмы брюшного отдела аорты.
Размеры почки уменьшены незначительно. Клубочки, артериолы и артерии выглядят нормальными. Часто наблюдают очаги канальцевой атрофии, гиперплазию, повышенную зернистость и удлинение юкстагломерулярного аппарата. При длительной реноваскулярной гипертензии в артериях почек могут возникнуть изменения, вызванные повышенным АД.
Исходы и осложнения. Остро наступающая ренальная гипертензия обратима при восстановлении кровотока в ишемизированной почке. Более чем в половине случаев эффективны хирургическая реваскуляризация, ангиопластика или нефрэктомия. При длительном течении развиваются цирроз почек и ХПН.
