Химия Бакал / Методические указания по выполнению эссе, рефератов, индивидуальных домашних заданий, контрольных
.pdfИндивидуальные задания по химии
1.Получить все возможные соли, включая средние, основные, кислые и комплексные из полученных соединений. Написать уравнения реакции в молекулярной, полной ионной и сокращенной ионной формах.
2.Для каждой полученной в задании № 1 соли рассчитать относительную молекулярную массу, молярную массу и молярную массу эквивалента. Определить количество вещества, количество вещества эквивалента, а также число молекул в 10 граммах каждой соли.
3.Написать электронные формулы элементов, входящих в состав веществ задания № 1.
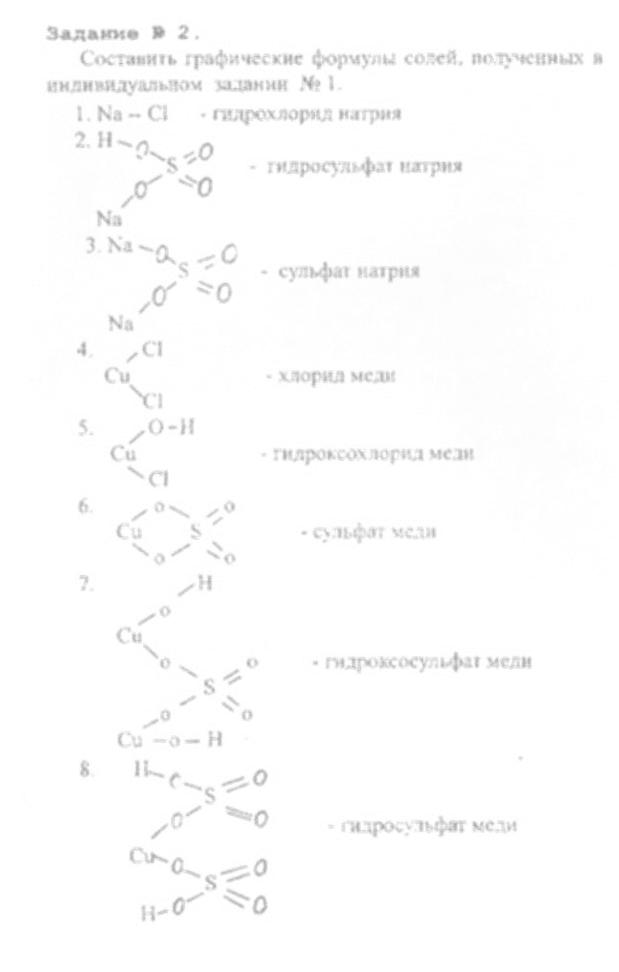
4.Составить графические формулы солей, полученных в задании № 1.
5.Записать 5 уравнений окислительно-восстановительных реакции с участием элементов, входящих в состав веществ задания № 1. Подобрать коэффициенты методом полуреакций.
6.Из задания № 1 выбрать соль для приготовления раствора со следующими параметрами: m (соли)=20 г, V (раствора)= 250 мл, ρ (раствора)= 1,02 г/см3.
Рассчитать молярную концентрацию соли, молярную концентрацию
эквивалента соли, моляльную концентрацию соли, титр и массовую долю
соли.
7.Написать уравнения реакции гидролиза солей, полученных в задании № 1. Указать рН среды.
8.Записать 3 формулы комплексных солей, в состав которых входят элементы из задания № 1. Назвать комплексные соединения. Указать внутреннюю и внешнюю сферы, комплексообразователь, координационное число. Записать константу устойчивости комплексного иона.
9.Составить гальванические цепи из металлов, входящих в состав заданий №
1.Написать все возможные варианты электролиза средних солей.
(Номер индивидуального задания выбирается в соответствии с номером зачетной книжки студента)
Индивидуальные задания по химии
1. HCI LiOH H3IO5 Co(OH)2 |
2. |
HBrO LiOH H3IO5 Fe(OH)2 |
3. HF NaOH H3BO3 Fe(OH)2 |
4. |
HBrO3 NaOH H3BO3 Co(OH)2 |
5. HBr KOH H3AsO4 Mn(OH)2 |
6. |
HIO KOH H3AsO4 Cr(OH)2 |
7. HI RbOH H3AsO3 Cr(OH)2 |
8. |
HNO2 RbOH H3AsO3 Mn(OH)2 |
9. HNO3 CsOH H3PO4 Cd(OH)2 |
10. |
HNO3 FrOH H2MnO4 Cd(OH)2 |
11. HCIO FrOH H2MnO4 Zn(OH)2 |
12. |
HPO3 CsOH H3PO4 Zn(OH)2 |
13. HCIO2 Mg(OH)2 H2SiO3 Cu(OH)2 |
14. |
HAsO3 Mg(OH)2 H2SiO3 Cu(OH)2 |
15. HCIO3 Ca(OH)2 H2SeO3 Ba(OH)2 |
16. |
HBO2 Ca(OH)2 H2SeO3 Ba(OH)2 |
17. HCIO4 Sr(OH)2 H2SeO4 Mg(OH)2 |
18. |
HAsO2 Sr(OH)2 H2SeO4 Sr(OH)2 |
19. HBrO Ba(OH)2 H2CO3 Ca(OH)2 |
20. |
HIO Ba(OH)2 H2CO3 LiOH |
21. HBrO3 Cu(OH)2 H2SO3 Sr(OH)2 |
22. |
HIO4 Cu(OH)2 H2SO3 NaOH |
23. HIO Zn(OH)2 H2SO4 LiOH |
24. |
HMnO4 Zn(OH)2 H2SO4 KOH |
25. HNO2 Cd(OH)2 H2S NaOH |
26. |
H2S Cr(OH)2 HCI RbOH |
27. HNO3 Cr(OH)2 HCI KOH |
28. |
H2SO4 Mn(OH)2 HF CsOH |
29. HPO3 Mn(OH)2 HF RbOH |
30. |
H2SO3 Cd(OH)2 H2S FrOH |
31. HAsO3 Fe(OH)2 HBr CsOH |
32. |
H2CO3 Fe(OH)2 HBr Sr(OH)2 |
33. HBO2 Co(OH)2 HI FrOH |
34. |
H2SeO4 Co(OH)2 HI Mg(OH)2 |
35. HAsO2 Cr(OH)3 HNO3 Sr(OH)2 |
36. |
H2SeO3 Cr(OH)3 HNO3 Ca(OH)2 |
37. HIO AI(OH)3 HCIO Ba(OH)2 |
38. |
H2SiO3 AI(OH)3 HCIO Sr(OH)2 |
39. HIO4 Fe(OH)3 HCIO2 Cu(OH)2 |
40. |
H2MnO4 Fe(OH)3 HCIO2 Ba(OH)2 |
41. HMnO4 Co(OH)3 HCIO3 Zn(OH)2 |
42. |
H3PO4 Co(OH)3 HCIO3 Cu(OH)2 |
43. HCI Cd(OH)2 H2S LiOH |
44. |
H3AsO3 Cd(OH)2 H2S Zn(OH)2 |
45. HF Cr(OH)2 H2SO4 NaOH |
46. |
H3AsO4 Cr(OH)2 H2SO4 LiOH |
47. HBr Mn(OH)2 H2SO3 KOH |
48. |
H3BO3 Mn(OH)2 H2SO3 NaOH |
49. HI Fe(OH)2 H2CO3 RbOH |
50. |
H3IO5 Fe(OH)2 H2CO3 KOH |
51. HNO3 Co(OH)2 H2SeO4 CsOH |
52. |
HCI Co(OH)2 H2SeO4 NaOH |
53. HCIO Cr(OH)3 H2SeO3 FrOH |
54. |
HF Cr(OH)3 H2SeO3 RbOH |
55. HCIO2 AI(OH)3 H2SiO3 Mg(OH)2 |
56. |
HBr AI(OH)3 H2SiO3 CsOH |
57. HCIO3 Fe(OH)3 H2MnO4 Ca(OH)2 |
58. |
HI Fe(OH)3 H2MnO4 FrOH |
59. HCIO4 Co(OH)3 H3PO4 Sr(OH)2 |
60. |
HNO3 Co(OH)3 H3PO4 Ba(OH)2 |