
- •Белки, их строение и биологическая роль
- •Строение белков. Первичная структура.
- •Вторичная структура
- •Третичная структура
- •Понятие о нативном белке
- •Классификация. Биологические и химические свойства белков
- •Физико-химические свойства белков
- •Биохимия сложных белков
- •Некоторые особенности строения миоглобина и гемоглобина
- •Гемаглобинопатии
- •Ферменты
- •Механизм действия ферментов. Основные черты ферментативного катализа, его этапы.
- •1. Частичный протеолиз (Трипсиноген------ Трипсин)
- •Факторы, оказывающие влияние на активность ферментов.
- •Конкурентное ингибирование.
- •Неконкурентное ингибирование.
- •Биохимия нуклеотидов и нуклеиновых кислот. Матричные биосинтезы.
- •Характеристика репликации.
- •Транскрипция. Трансляция.
- •1).Инициация
- •1. Обмен веществ включает в себя 3 этапа:
- •Организация цпэ (по рис.1)
- •Функции дыхательной цепи:
- •Дыхательный контроль.
- •Токсичное действие кислорода. Защита от токсичного действия кислорода.
- •Обмен углеводов.
- •Функции углеводов.
- •Всасывание углеводов в кишечнике.
- •Метаболизм глюкозы.
- •Гликолиз (дихотомический процесс).
- •Биомедицинское значение ферментативных реакций гликолиза.
- •Суммарная реакция и выход энергии при гликолизе.
- •Пентофозофосфатный путь ( пфп).
- •Биомедицинское значение.
- •Общая схема биохимических реакций пфп.
- •Медицинское значение.
- •Глюконеогенез.
- •Биомедицинское значение.
- •Биомедицинское значение.
- •Биосинтез гликогена.
- •Обмен фруктозы и галактозы.
- •Обмен липидов.
- •Функции липидов в организме.
- •Переваривание и всасывание жиров.
- •Желчные кислоты.
- •Всасывание продуктов гидролиза.
- •Биосинтез кетоновых тел.
- •Распад кетоновых тел.
- •Биосинтез высших жк.
- •Синтез жиров (таг).
- •Отличие действия инсулина в жировой ткани и печени:
- •Синтез холестерина.
- •Биосинтез Хс.
- •Ферменты.
- •Регуляция синтеза нуклеотидов.
- •Синтез пиримидиновых нуклеотидов.
- •Регуляция.
- •Катаболизм.
- •Катаболизм пуриновых нуклеотидов.
- •Регуляция обмена веществ. Гормоны (химические посредники).
- •1. По химической структуре:
- •2. По механизму действия;
- •3. По влиянию на организм:
- •Синтез и секреция гормонов.
- •Механизм действия гормонов белково-пептидной природы через вторичных посредников.
- •Эффекты, осуществляемые через ц амф.
- •Кальций как вторичный посредник.
- •Биохимия печени
- •Обезвреживающая функция печени
- •Обезвреживание веществ
- •Отличие этих цепей от цпэ
- •Удф-глюкуронилтрансферазы
- •Биохимия крови
- •Белки плазмы крови
- •Сывороточный альбумин
- •Глобулины
- •Конверсия метгемоглобина
- •Биосинтез тема и его регуляция
- •Гемостаз
- •1 Фаза: первичный гемостаз.
- •2 Фаза: гемокоагуляция
- •Фибрина
- •Противосвертывающая система
- •Биохимический_анализ
- •Гормоны
- •Липотропины
Некоторые особенности строения миоглобина и гемоглобина
НЬ состоит из простого белка глобина и 4 молекул гема. При объединении глобина и тема получается сложное соединение, которое выполняет в организме исключительно важную дыхательную функцию. Другое важное свойство - поддержание постоянства рН крови. НЬ обеспечивает до 50% буферной ёмкости крови. НЬ - аллостерический белок, присоединение какого-либо вещества к нему меняет его сродство к другим. Он обладает способностью легко взаимодействовать с рядом газов: ОА, СОА, СО, NO, NQ. Кинетика связывания кислорода миоглобином и гемоглобином
В отличие от НЬ миоглобин имеет 1 ППЦ, которая связана с гемом. Миоглобин не способен переносить кислород от лёгких к периферическим тканям по своей химической природе. Он преобладает в мышцах и является веществом, которое эффективно запасает кислород. % или степень насыщения миоглобина Од, зависит от концентрации О2 в среде, окружающей молекулы белка. [О2] обозначается как парциальное давление в мм рт.ст. Зависимость между (О2) в среде и насыщенностью миоглобина О2, описывается в виде прямоугольной гиперболы. Кривая насыщения миоглобина и гемоглобина кислородом.
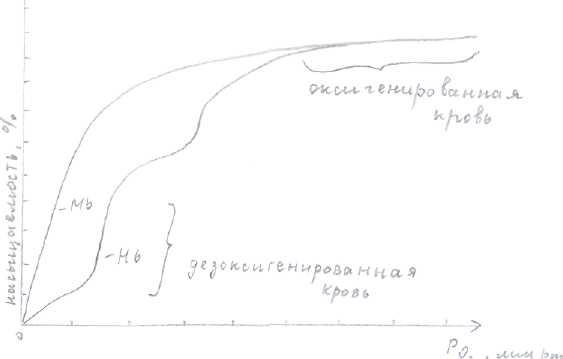
Для выяснения кинетики насыщения О2 миоглобина и НЬ необходимо принимать во внимание, что Р О2(в лёгких) = 100мм рт.ст., поэтому миоглобин в лёгких мог бы весьма эффективно насыщаться О2, . В венозной крови Р О2 составляет 40мм рт.ст., а в активно работающей мышце - 20мм рт.ст. Даже при таких параметрах миоглобин будет в значительной степени насыщаться О2 , поэтому МЬО2 не может являться средством доставки O2 от лёгких к периферическим тканям. При тяжёлой мышечной работе Ро2 может понизиться до 5, при этих условиях МЬО2 легко отдаёт О2, который используется для окислительного биосинтеза АТФ в митохондриях мышечных клеток.
НЬ связывает 4 молекулы О2, на 1 тетрамер (по одной молекуле на гем в каждой субъединице). Кривая насыщения носит сигмоидный характер. Т.о. способность НЬ связывать О2 зависит от того содержатся ли в данном тетрамере другие молекулы О2,. Как видно из изотермы адсорбции связывание первой молекулы О2, протекает медленно, другой - с большей скоростью и т.д. Такой характер кинетики объясняется так называемым кооперативным связыванием, благодаря которому НЪ легко насыщается О2 в легких (при Ро2 = 100мм рт.ст.) и очень легко отдает О2, в периферических тканях (Р50 ~20мм рт.ст.). Для характеристики кинетики действия НЬ введён показатель P50 (значение РО2 , при котором происходит 50%-ное насыщение, у теплокровных Р50 может значительно варьировать, однако оно всегда выше значения \ в периферических тканях). Оксигенирование НЬ сопровождается значительными изменениями конформации молекул:
разрыв солевых связей, образованных концевыми карбоксилами субъединиц, что облегчает присоединение О2,
разрыв связи обуславливает изменение вторичных, третичных, четвертичных структур, при этом происходит компактизация тетрамеров и увеличивается сродство к О2
четвертичная структура НЬ описывается как Т - состояние для частично оксигенированного НЬ и как R-состояние для полностью оксигенированного НЬ.
« Т- и R-состояние» используют для характеристики четвертичной структуры многих аллостерических ферментов, в Т-состоянии отмечается наименьшее сродство к субстрату. НЬ ускоряет транспорт СО2 от ткани к лёгким =15% СО2 крови переносится НЬ.
