
- •3) Основные понятия химии. Закон постоянства состава. Закон эквивалентов. Молярная масса эквивалентов. Молярный объем эквивалентов.
- •4) Квантово-механическая модель атома. Строение ядер и электронных оболочек.
- •5)Квантовые числа. Электронные конфигурации атомов.
- •6) Принцип наименьшей энергии. Принцип Паули. Правило Хунга.
- •7)Периодический закон д. И. Менделеева. Структура псхэ : периоды, ряды, семейства, s-, p-, d-, f-классификация элементов.
- •8) Химическая связь и ее характеристики. Типы хим. Связей.
- •9) Ионная связь.
- •10) Ковалентная связь.
- •11)Метод валентных связей.
- •12) Метод молекулярных орбиталей.
- •13) Межмолекулярные взаимодействия.
- •14) Водородная связь.
- •Межмолекулярная и внутримолекулярная водородная связь
- •15) Металлическая связь.
- •16) Основные понятия термодинамики.
- •17)Энтальпия. Теплота. Работа. Первый закон термодинамики.
- •Следствия из закона Гесса
- •19) Энтропия и второй закон термодинамики. Энергия Гиббса.
- •100% Энергии не может быть преобразовано в работу
- •20) Основные положения химической кинетики. Скорость хим. Реакции. Порядок и молекулярность хим. Реакции.
- •21) Зависимость скорости хим. Реакции от температуры.
- •22)Принцип Ле-Шателье.
- •24) Растворы: понятие, классификация. Способы выражения концентрации.
- •26) Осмотический закон Вант-Гоффа.
- •28) Ионное произведение воды. PH водных растворов.
- •Ионное произведение воды
- •29) Качественный анализ. Классификация методов. Требования, предъявляемые к реакциям в качественном анализе. Примеры.
- •30) Классификация методов количественного анализа. Сущность титриметрического метода анализа, основные приемы титрования. Индикаторы кистно-основного титрования.
- •31) Обратимость химических реакций.
17)Энтальпия. Теплота. Работа. Первый закон термодинамики.
- Энтальпи́я, такжетепловая функцияитеплосодержание— термодинамический потенциал, характеризующий состояние системы в термодинамическом равновесии при выборе в качестве независимых переменных давления, энтропии и числа частиц.
Проще говоря, энтальпия — это та энергия, которая доступна для преобразования в теплоту при определенном постоянном давлении.
Если термомеханическую систему рассматривать как состоящую из макротела (газа) и поршня площадью Sс грузом весомР = pS, уравновешивающего давление газарвнутри сосуда, то такая система называетсярасширенной.
Энтальпия или энергия расширенной системы Еравна сумме внутренней энергии газаUи потенциальной энергии поршня с грузомEпот=pSx=pV
![]()
Таким образом, энтальпия в данном состоянии представляет собой сумму внутренней энергии тела и работы, которую необходимо затратить, чтобы тело объёмом Vввести в окружающую среду, имеющую давлениери находящуюся с телом в равновесном состоянии. Энтальпия системыH— аналогично внутренней энергии и другим термодинамическим потенциалам — имеет вполне определенное значение для каждого состояния, т. е. является функцией состояния. Следовательно, в процессе изменения состояния
![]()
Изменение
энтальпии (или Тепловой эффект химической
реакции) не зависит от пути процесса,
определяясь только начальным и конечным
состоянием системы. Если система
каким-либо путём возвращается в исходное
состояние (круговой процесс), то изменение
любого её параметра, являющегося функцией
состояния, равно нулю, отсюда
![]() ,
или же
,
или же
![]()
Дифференциал энтальпии, выраженный в собственных переменных — через энтропию S и давление p:
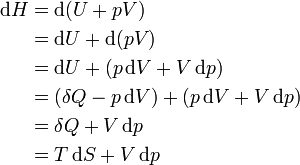
Поскольку
в квазиравновесных процессах
![]() —
количество теплоты, подведенной к
системе, отсюда вытекает физический
смысл введения понятия энтальпии: ее
изменение — это тепло, подведенное
к системе в изобарическом процессе (при
постоянном давлении). Практическое
применение этой функции основано на
том, что множество химических процессов
в реальных или лабораторных условиях
реализуются именно при постоянном
(атмосферном) давлении, когда резервуар
открыт. Так, энтальпия образования —
количество энергии, которое выделяется
или поглощается при образовании сложного
вещества из простых веществ.
—
количество теплоты, подведенной к
системе, отсюда вытекает физический
смысл введения понятия энтальпии: ее
изменение — это тепло, подведенное
к системе в изобарическом процессе (при
постоянном давлении). Практическое
применение этой функции основано на
том, что множество химических процессов
в реальных или лабораторных условиях
реализуются именно при постоянном
(атмосферном) давлении, когда резервуар
открыт. Так, энтальпия образования —
количество энергии, которое выделяется
или поглощается при образовании сложного
вещества из простых веществ.
Все химические реакции сопровождаются выделением (экзотермические) или поглощением (эндотермические) тепла. Мерой теплоты реакции служит изменение энтальпии ΔН, которая соответствует теплообмену при постоянном давлении. В случае экзотермических реакций система теряет тепло и ΔН — величина отрицательная. В случае эндотермических реакций система поглощает тепло и ΔН — величина положительная.
Энтальпией системы удобно пользоваться в тех случаях, когда в качестве независимых переменных, определяющих состояние системы, выбирают давление ри температуруТ
![]()
В
этом случае изменение энтальпии в
изобарическом процессе практически
удобно рассчитывать, зная теплоемкость
при постоянном давлении
![]() (термохимический
закон Кирхгофа):
(термохимический
закон Кирхгофа):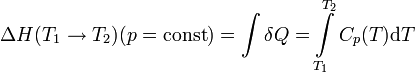
При этом используется эмпирическое разложение теплоёмкости в ряд по степеням Т:
![]()
Энтальпия —
величина аддитивная (экстенсивная),
т. е. для сложной системы равна сумме
энтальпий её независимых частей![]() .
Подобно другим термодинамическим
потенциалам, энтальпия определяется с
точностью до постоянного слагаемого,
которому в термодинамике часто придают
произвольные значения (например, при
расчете и построении тепловых диаграмм).
При наличии немеханических сил величина
энтальпии системы равна
.
Подобно другим термодинамическим
потенциалам, энтальпия определяется с
точностью до постоянного слагаемого,
которому в термодинамике часто придают
произвольные значения (например, при
расчете и построении тепловых диаграмм).
При наличии немеханических сил величина
энтальпии системы равна
![]()
где
![]() —
обобщённая сила;
—
обобщённая сила;![]() —
обобщённая координата.
—
обобщённая координата.
Первый закон термодинамики гласит, (4 разные формулировки) что :
Энергия не может быть создана или уничтожена (закон сохранения энергии), она лишь переходит из одного вида в другой в различных физических процессах. Отсюда следует, что внутренняя энергия изолированной системы остается неизменной.
Количество теплоты, полученное системой, идет на изменение ее внутренней энергии и совершение работы против внешних сил.
Изменение внутренней энергии системы при переходе ее из одного состояния в другое равно сумме работы внешних сил и количества теплоты, переданной системе и не зависит от способа, которым осуществляется этот переход.
Изменение внутренней энергии неизолированной термодинамической системы равно разности между количеством теплоты, переданной системе, и работой, совершенной системой над внешними силами.
Первый закон термодинами гласит, что энергия не может быть создана или уничтожена. Таким образом, энергия системы (замкнутой) - постоянна. Тем не менее, энергия может быть передана от одного элемента системы другому. Рассмотрим замкнутую систему, изолированную от остальных.
Передача энергии между различными подсистемами в ней может быть описана как :
E1 = E2
где
E1 = начальная энергия
E2 = конечная энергия
Внутрення энергия включает :
Кинетическую энергию движения атомов
Потенциальную энергию хранящуюся в химических связях
Гравитационную энергию системы
Первый закон является основой для термодинамической науки и инженерного анализа.
Базируется на возможных типах обмена (энергии), ниже приведены 3 типа систем:
пред - изолированные системы (isolated systems): отсутствует обмен элементами системы или энергией
закрытые системы (closed systems): отсутствует обмен элементами системы, но присутствует некоторый обмен энергией
открытые системы (open systems): возможен обмен как элементами системы, так и энергией
Первый закон термодинамики помогает использовать ключевые концепции внутренней энергии (internal energy), тепла (heat), и работы системы (system work). которые широко используются в описании тепловых систем (heat engines).
Внутренняя энергия ( Internal Energy) - Внутренняя энергия определяется как энергия случайных, находящихся в неупорядченном движении молекул. Энергия молекул находится в диапазоне от высокой, необходимой для движения, до заметной лишь с помощью микроскопа энергии на молекулярном или атомном уровне. Например, у стакана с водой комнатной температы, стоящего на столе нет, на первый взгляд, никакой энергии: ни кинетической, ни потенциальной относительно стола. Но, с помощью микроскопа становится заметна "бурлящая" масса быстро двигающихся молекул. Если выплеснуть воду из стакана, эта микроскопическая энергия не обязательно заметно изменится, когда мы усредним добавленную кинетическую энергию на все молекулы воды.
Тепло - Тепло может быть определено, как энергия, передаваемая от объекта с более высокой температурой к объекту с менее высокой температурой. Сам по себе объект не обладает "теплом"; соответствующий термин для микроскопической энергии объекта - внутренняя энергия. Внутренняя энергия может увеличиваться путем переноса энергии к объекту от объекта, имеющего температуру выше - этот процесс называется нагревом.
Работа - Когда работа совершается термодинамической системой (чаще всего это газ, который совершает работу), то работа совершенная газом при постоянном давлении определяется как : W = p dV, где W - работа, p - давление, а dV -изменение объема. В случаях когда давление не является постоянным, работа может быть представлена интегральным образом, как площадь поверхности под кривой в координатах давление, объем, которые представляют происходящий процесс.
Изменение внутренней энергии системы равно теплу (добавленному системе) минус работа, совершенная системой
dE = Q - W
где dE = изменение внутренней энергии Q = добавленное тепло W =работа системы
18) Закон Гессе. Следования их закона Гессе. Термохимические расчеты. - Закон Гесса— основной законтермохимии, который формулируется следующим образом:
Тепловой эффект химической реакции, проводимой в изобарно-изотермических или изохорно-изотермических условиях, зависит только от вида и состояния исходных веществ и продуктов реакции и не зависит от пути её протекания.
Иными словами, количество теплоты, выделяющееся или поглощающееся при каком-либо процессе, всегда одно и то же, независимо от того, протекает ли данноехимическое превращениев одну или в несколько стадий (при условии, чтотемпература,давлениеиагрегатные состояниявеществ одинаковы). Например, окислениеглюкозыв организме осуществляется по очень сложному многостадийному механизму, однако суммарный тепловой эффект всех стадий данного процесса равен теплоте сгорания глюкозы.
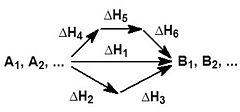
На рисунке приведено схематическое изображение некоторого обобщенного химического процесса превращения исходных веществ А1, А2… в продукты реакции В1, В2…, который может быть осуществлен различными путями в одну, две или три стадии, каждая из которых сопровождается тепловым эффектомΔHi. Согласно закону Гесса, тепловые эффекты всех этих реакций связаны следующим соотношением:
![]()
Закон открыт русским химиком Г. И. Гессомв1840г.; он является частным случаемпервого начала термодинамикиприменительно к химическим реакциям. Практическое значение закона Гесса состоит в том, что он позволяет рассчитывать тепловые эффекты самых разнообразных химических процессов; для этого обычно используют ряд следствий из него.
