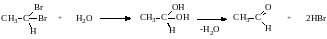- •Примеры решения задач
- •Задачи и упражнения для самостоятельного решения
- •Получение алканов
- •2. Каталитическое гидрирование (Ni, Pd, Pt) ненасыщенных углеводородов при нагревании:
- •4. Гидролиз карбидов
- •5. Декарбоксилирование солей низших карбоновых кислот
- •Химические свойства алканов
- •2. Нитрование (реакция Коновалова)- реакция радикального замещения sr.
- •3. Реакции дегидрирования
- •5. Реакции горения
- •Примеры решения задач
- •Задачи и упражнения для самостоятельного решения
- •1. Крекинг и пиролиз нефтепродуктов.
- •2. Каталитическое (Ni, Pt, Pd) дегидрирование алканов при нагревании :
- •Химические свойства алкенов.
- •2. Реакции полимеризации:
- •3. Реакции окисления
- •Решение:
- •1) Условию задачи отвечает следующее строение:
- •Задачи и упражнения для самостоятельного решения
- •97. Смесь этена с бутаном, с плотность по водороду 21,5, сожгли. Продукты сгорания 20 л этой смеси пропустили через избыток раствора гидроксида кальция. Определите массу выпавшего осадка.
- •Диеновые углеводороды
- •1. Галогенирование
- •4. Полимеризация.
- •Примеры решения задач
- •Задачи и упражнения для самостоятельного решения
- •Алкины.
- •2. Взаимодействие карбидов металлов с водой
- •4. Дегидрогалогенирование дигалогеналканов:
- •5. Из галогеналканов под действием цинка:
- •Химические свойства алкинов
- •1. Галогенирование
- •3. Гидратация.
- •4. Гидрирование.
- •6. Кислотные свойства алкинов
- •8. Горение
- •Примеры решения задач
- •Задачи и упражнения для самостоятельного решения
- •Циклоалканы
- •Получение циклоалканов
- •2. Циклогексан и его производные получают гидрированием бензола:
- •Химические свойства циклоалканов
- •Примеры решения задач Пример 18.
- •Решение:
- •Пример 19.
- •Решение:
- •Пример 20.
- •Задачи и упражнения для самостоятельного решения
- •Получение аренов
- •Химические свойства аренов
- •1. Электрофильное замещение в бензольном кольце
- •Примеры решения задач
- •Задачи и упражнения для самостоятельного решения
- •2. Гидролиз алкилгалогенидов в кислой или щелочной среде:
- •3. Гидролиз сложных эфиров:
- •4. Восстановление более высокоокисленных соединений
- •5. Биохимические методы.
- •1. Кислотные свойства.
- •3. Дегидратация(отщепление воды).
- •5. Окисление спиртов
- •1. Многие из химических свойств двухатомных и трёхатомных спиртов походят на таковые одноатомных спиртов. Отличия:
- •Задачи и упражнения для самостоятельного решения
- •1. Кислотные свойства
- •2. Реакции электрофильного замещения в бензольном кольце
- •3. Окислительно-восстановительные реакции
- •4. Реакции комплексообразования
- •Задачи и упражнения для самостоятельного решения
- •Карбонильные соединения
- •Получение карбонильных соединений
- •1. Окисление спиртов
- •4. Гидратация алкинов(реакция Кучерова).
- •5. Получение ацетона в промышленности
- •Химические свойства карбонильных соединений
- •1. Окисление
- •2. Восстановление.
- •Примеры решения задач
- •Задачи и упражнения для самостоятельного решения
- •Карбоновые кислоты
- •1. Растворимые кислоты диссоциируют в воде:
- •2. Карбоновые кислоты (особенно растворимые в воде)
- •9. Окисление
- •11. Реакции в бензольном ядре ароматических кислот
- •12. Реакции ненасыщенных кислот
- •Примеры решения задач
- •Задачи и упражнения для самостоятельного решения
- •Сложные эфиры. Жиры.
- •2. Взаимодействие ангидрида карбоновой кислоты со спиртом
- •3. Взаимодействие хлорангидрида карбоновой кислоты со спиртом
- •Углеводы
- •1. Окисление
- •3. Алкилирование аминов:
- •4. Взаимодействие с ангидридами и хлорангидридами
- •7. Особенности ароматических аминов(анилина)
- •8. Окисление анилина
- •2. Обработка галогенсодержащих карбоновых кислот избытком аммиака:
- •3. Реакции, обусловленные наличием двух функциональных групп в
Карбонильные соединения
К карбонильным соединениям относятся соединения, содержащие карбонильную группу( альдегиды, кетоны)
 -альдегиды
-альдегиды
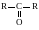 -кетоны.
-кетоны.
Номенклатура
Для альдегидов к названию главной цепи добавляется окончание «аль» или «ал».
Для кетонов «он»
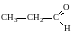
- пропаналь
-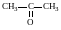 пропанон-2
пропанон-2
Также альдегиды называются по названию тех кислот, в которые они переходят при окислении.
- пропионовый альдегид
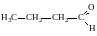
- масляный альдегид
Изомерия.
Изомерия альдегидов зависит от изомерии радикалов, соединений с карбонильной группой.
- бутаналь (масляный альдегид)

- 2-метилпропаналь(изомасляный альдегид)
Строение карбонильной группы
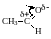
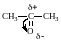
В альдегидах и кетонах карбонильный атом углерода находится в sp2 – гибридном состоянии и образует 3 σ-связи, которые располагаются в плоскости под углом 120о друг к другу. Вследствие большей электроотрицательности атома кислорода электронная плотность π–связи смещена в его направлении. В результате этого у атома кислорода карбонильной группы создаётся повышенная электронная плотность и он приобретает частичный отрицательный заряд δ- а на атоме углерода возникает частичный положительный заряд δ+. Атом углерода приобретает электрофильные свойства и активно взаимодействует с нуклеофильными реагентами (реакции присоединения), а атом кислорода становится нуклеофильным и поэтому способен взаимодействовать с электрофильными реагентами.
*Большая реакционная способность карбонильной группы объясняется сильной поляризацией этой группы. С одной стороны, атом кислорода оказывает влияние на атом водорода, соединенный с карбонильной группой и он легко окисляется, а с другой стороны, так как есть двойная связь, то для карбонильной группы характерны реакции присоединения по карбонильному углеродному атому, на котором частичный положительный заряд (
Физические свойства.
Карбонильные соединения бывают газообразные (формальдегиды); жидкие(уксусный альдегид); твердые(параформ). Также у них нет водородных связей, то температура кипения ниже, чем у спиртов. Имеют характерный запах.
Получение карбонильных соединений
1. Окисление спиртов
В качестве окислителей обычно используется CuO(1 стадия окисления), кислород воздуха в присутствии катализаторов(Cu и др.), подкисленный раствор KMnO4 или K2Cr2O7 .
При окислении первичных спиртов на первой стадии образуются альдегиды которые далее могут окисляться до карбоновых кислот. Вторичные спирты в этих условиях окисляются до кетонов.
Например:
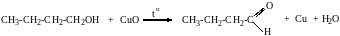
бутаналь
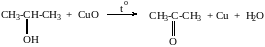
пропанон
Каталитическое дегидрирование спиртов.
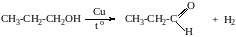
пропаналь
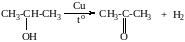
пропанон

циклогексанол циклогексанон
3. Гидролиз дигалогенидов.