
- •Оглавление
- •Горение газов
- •Общие закономерности кинетического режима горения
- •Влияние различных факторов на скорость распространения пламени
- •Диффузионное горение газов
- •Особенности горения газовых струй.
- •Условия стабилизации и срыва пламени
- •Оценка расхода горящих газовых фонтанов
- •Методы тушения газовых фонтанов
- •Расчет основных параметров горения газового фонтана
- •Определим число молей и продуктов горения
- •Зависимость изменения мощности излучения факела пламени от расстояния до устья скважины.
- •6. Определение теоретического расхода воды на тушение газового фонтана производится по формуле:
- •Литература.
Горение газов
Как правило, горение возникает от какого-либо источника зажигания. По существу это только начальная стадия процесса горения, т.е. ее инициирование. Безусловно, указанная стадия важна с точки зрения профилактики пожаров и взрывов, но предотвратить их не всегда удается. Поэтому для практических работников пожарной охраны большое значение имеет возможность прогнозирования динамики развития горения, а именно, в каком режиме и с какими параметрами будет развиваться пожар или взрыв на реальных объектах. Кроме того, в практической деятельности приходится сталкиваться с необходимостью реставрации картины развития уже происшедших пожаров и взрывов. Для этого необходимо знать основные закономерности процессов распространения, развития горения. Эти сведения необходимы также для правильного выбора наиболее эффективного вида и способа применения огнетушащего средства в конкретных условиях.
При изучении дисциплины «Теория горения и взрыва» вы познакомились с различными режимами горения газов: кинетическим и диффузионным, ламинарным и турбулентным. Кинетическое горение возможно только в предварительно перемешанных смесях горючего и окислителя. Во всех остальных случаях горение будет протекать в диффузионном режиме.
Общие закономерности кинетического режима горения
Если
с помощью оптического прибора рассмотреть
кинетическое пламя
в неподвижной горючей смеси, то можно
увидеть следующую картину (рис.
1). Справа находятся нагретые до высокой
температуры продукты горения
(Тпг),
слева — холодная с температурой (То)
исходная горючая смесь, а между ними -
ярко светящаяся полоска - фронт пламени
с толщиной (![]() ).
Горючий
компонент во фронте пламени сгорает, и
в продуктах горения его концентрация
практически равна нулю. Естественно,
температура продуктов горения,
равная температуре горения (Тг),
больше
температуры исходной смеси
(То) (Тпг
= Тг
).
Горючий
компонент во фронте пламени сгорает, и
в продуктах горения его концентрация
практически равна нулю. Естественно,
температура продуктов горения,
равная температуре горения (Тг),
больше
температуры исходной смеси
(То) (Тпг
= Тг![]() То). Поскольку теплота передается от
горячего к холодному,
в сторону исходной смеси будет идти
тепловой поток (
То). Поскольку теплота передается от
горячего к холодному,
в сторону исходной смеси будет идти
тепловой поток (![]() ),
нагревая
прилегающий
к ней слой, так называемую зону подогрева.
Передача теплоты от
нее осуществляется теплопроводностью.
),
нагревая
прилегающий
к ней слой, так называемую зону подогрева.
Передача теплоты от
нее осуществляется теплопроводностью.

Рис. 1. Схема фонтана.
Нормальное или дефлаграционное горение — это распространение пламени по однородной горючей среде, при котором фронт пламени движется вследствие ее послойного разогрева по механизму теплопроводности от продуктов горения.
Толщина
фронта пламени![]() ,
как правило, не превышает десятых долей
миллиметра. Поэтому его обычно принимают
за поверхность, отделяющую
исходную смесь от продуктов горения.
Как показали исследования, своим
свечением фронт пламени обязан
многоатомным радикалам: С=С
,
как правило, не превышает десятых долей
миллиметра. Поэтому его обычно принимают
за поверхность, отделяющую
исходную смесь от продуктов горения.
Как показали исследования, своим
свечением фронт пламени обязан
многоатомным радикалам: С=С![]() ,
СН
,
СН![]() ,
НСО и др. Есть в пламени и ионы, концентрация
которых достигает 10 - 101
м-3.
Возникновение ионов в пламени имеет
химическую и термическую
природу.
,
НСО и др. Есть в пламени и ионы, концентрация
которых достигает 10 - 101
м-3.
Возникновение ионов в пламени имеет
химическую и термическую
природу.
Влияние различных факторов на скорость распространения пламени
Нормальная скорость распространения пламени (uн) зависит от теплофизических свойств газопаровоздушной смеси. Но в еще большей степени скорость распространения зависит от ее физико-химических свойств -скорости и температуры реакции горения:
![]()
т.е. ![]() пропорциональна скорости реакции
окисления (
пропорциональна скорости реакции
окисления (![]() )
и обратно пропорциональна температуре
горения (
)
и обратно пропорциональна температуре
горения (![]() ).
Определяющим параметром, безусловно,
будет скорость реакции.
).
Определяющим параметром, безусловно,
будет скорость реакции.
Запишем уравнение скорости химической реакции горения:
![]()
Рассмотрим, как будет меняться скорость реакций окисления для смесей с разным соотношением горючего и воздуха (рис. 2).
Из
графика видно, что для смеси
стехиометрического состава (коэффициент
избытка воздуха ![]() =
1)
скорость реакции окисления максимальна:
=
1)
скорость реакции окисления максимальна:
![]()
При увеличении концентрации горючего в смеси, когда а становится < 1, воздух находится в недостатке, и горючее сгорает не полностью, а частично. Поэтому меньше выделится теплоты Qгор, а значит Тг снизится.
Скорость
реакций окисления по сравнению со
стехиометрической уменьшится,
причем сразу из-за снижения и концентрации
окислителя ![]() ,
и температуры
горения. То есть при последовательном
снижении а (что эквивалентно
увеличению концентрации Сгор
в смеси) скорость реакций окисления
w
и
температуры горения Тг
будет последовательно снижаться. На
графике при Сгор
> Сг.стех
кривая
становится нисходящей. Значит, при
> 1 скорость реакций окисления также
снижается, и в целом на графике получается
парабола.
,
и температуры
горения. То есть при последовательном
снижении а (что эквивалентно
увеличению концентрации Сгор
в смеси) скорость реакций окисления
w
и
температуры горения Тг
будет последовательно снижаться. На
графике при Сгор
> Сг.стех
кривая
становится нисходящей. Значит, при
> 1 скорость реакций окисления также
снижается, и в целом на графике получается
парабола.
Именно такая зависимость скорости реакции горения от концентрации горючего компонента в исходной смеси предопределяет параболический вид зависимости многих параметров процесса горения от состава смеси: температуры самовоспламенения и минимальной энергии зажигания, концентрационных пределов распространения пламени. Вид параболы имеет также и зависимость нормальной скорости распространения пламени ин от концентрации горючего Сг (рис. 2).
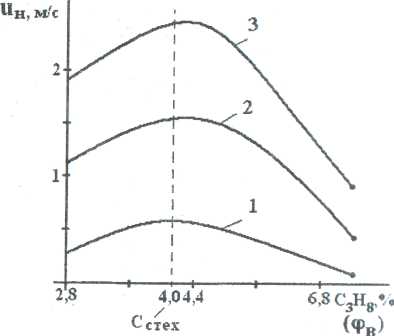
Рис.2. Зависимость скорости распространения пламени от концентрации пропана в воздухе при температурах 311 К (1); 644 К (2); 811 К (3).
Согласно теории максимальная скорость распространения пламени (uмах) должна соответствовать стехиометрической концентрации. Однако экспериментальные ее значения несколько сдвинуты в сторону богатых по содержанию горючих смесей (а< 1). С увеличением начальной температуры смеси скорость распространения пламени должна повышаться, что и дается на практике.
Для различных веществ uн зависит от их химического строения и колеблется в довольно широких пределах (табл. 1). Для большинства смесей углеводородных топлив с воздухом uн < 1 м/с. При введении в горючую смесь балласта — избыточного воздуха или азота заметно снижается температура горения.
Таблица 1. Нормальная скорость распространения пламени для некоторых горючих смесей
Горючая смесь |
Формула |
uн,м/с |
Водород + воздух |
Н2 + 0,5(О2 + 3,76N2) |
1.60 |
Ацетилен + воздух |
СH=СН+2,5(О2+ 3,76N2 |
1.50 |
Ацетилен + кислород |
СН=СН + 2,5О2 |
8.00 |
Этилен + воздух |
СН2=СН2+3(О2 + 3,76N2) |
0.60 |
Бутан + воздух |
С4Н10 + 6,5(О2 + 3,76N2) |
0.40 |
Метан + воздух |
CH4 + 3(О2 + 3,76N2) |
0.34 |
40
Рис.5.
Влияние флегматизаторов на скорость
распространения пламени
по пропану
С3Н8
(
= 1.15).
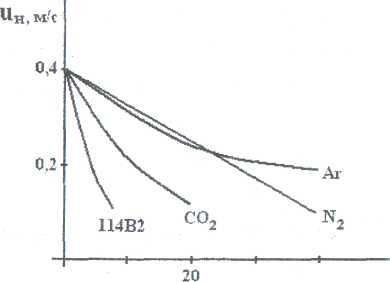
Данные рис. 5. иллюстрируют эти факты.
