
- •Методы решения научно-технических задач методические указания по выполнению лабораторных работ
- •Содержание
- •Введение
- •Лабораторная работа №1 обработка результатов химического эксперимента
- •Лабораторная работа №2 метод наименьших квадратов. Линейная зависимость
- •Лабораторная работа №3 мнк нелинейная функциональная зависимость
- •Лабораторная работа №4 расчет смесей сложного состава
- •Лабораторная работа №5 оду в химической кинетике
- •Лабораторная работа №6 простая перегонка
- •Приложения
- •Список литературы
Лабораторная работа №2 метод наименьших квадратов. Линейная зависимость
Очень часто исследуемая величина меняется с изменением условий опыта, а задача измерений состоит в нахождении функциональной зависимости, которая наилучшим образом описывает закон изменения интересующей на величины (например, зависимость объема газа от давления, вязкости жидкости от температуры и т.д.)
Положим, мы определяем некоторую величину y, зависящую только от величины x. Для каждого значения xi проводим одно или несколько измерений и получаем соответствующие значения yi. Чаще всего yi известна не точно, а с определенной погрешностью ∆yi. Также часто может быть неизвестно и точное значение xi. Этот массив данных позволяет с некоторой степенью вероятности определить ту функциональную зависимость, которой связаны x и y, y = f(x). Однако таких функций можно брать бесчисленное множество. Для выбора единственной используем принцип простоты и монотонности зависимости.
Эта задача может быть решена с помощью метода наименьших квадратов. Суть метода состоит в нахождении таких значений параметров, входящих в искомую функциональную зависимость, при которых сумма квадратов отклонений значений функции от экспериментальных данных будет минимальной.
Рассмотрим особенности метода наименьших
квадратов на примере линейной зависимости
в случае одной переменной. Пусть искомая
функция является линейной, т.е.
![]() ,
где a и b
неизвестны, а x и y
заданы некоторыми значениями (xi,
yi),
полученными в результате некоторого
эксперимента. При подстановке значений
в уравнение
получаем
,
где a и b
неизвестны, а x и y
заданы некоторыми значениями (xi,
yi),
полученными в результате некоторого
эксперимента. При подстановке значений
в уравнение
получаем
![]() .
Разность
.
Разность
![]() называется невязкой и возникает в
результате в результате ошибок
эксперимента, ошибок вычислений, неточной
линейной зависимости и т.п. Тогда
требуется подобрать a
и b так, чтобы сумма
квадратов невязок, т.е
называется невязкой и возникает в
результате в результате ошибок
эксперимента, ошибок вычислений, неточной
линейной зависимости и т.п. Тогда
требуется подобрать a
и b так, чтобы сумма
квадратов невязок, т.е
![]() была
минимальной. Итак,
была
минимальной. Итак,
![]() – функция двух переменных и требуется
найти ее минимум. Минимум этой суммы
находится по правилам дифференциального
исчисления. Это соответствует равенству
нулю производных функции по a
и b.
– функция двух переменных и требуется
найти ее минимум. Минимум этой суммы
находится по правилам дифференциального
исчисления. Это соответствует равенству
нулю производных функции по a
и b.


Отсюда,
![]() и
и
![]() .
Эта система уравнений легко решается
относительно a и b:
.
Эта система уравнений легко решается
относительно a и b:

 (2.1)
(2.1)
Теория дает возможность определить
также дисперсию уклонения (количественно
охарактеризовать степень разброса
точек) и дисперсию коэффициентов a
и b. Результаты расчета
могут быть записаны в виде ![]() ,
,
![]() ;
;
![]() ,
,
![]() tα
– коэффициент Стьюдента, Sa
и Sb
– дисперсии коэффициентов. Степень
приближения экспериментальной зависимости
к прямой характеризуется коэффициентов
r. Чем ближе значение
r к единице, тем лучше
экспериментальные данные описываются
уравнением прямой, тем надежней интер-
и экстраполяция.
tα
– коэффициент Стьюдента, Sa
и Sb
– дисперсии коэффициентов. Степень
приближения экспериментальной зависимости
к прямой характеризуется коэффициентов
r. Чем ближе значение
r к единице, тем лучше
экспериментальные данные описываются
уравнением прямой, тем надежней интер-
и экстраполяция.
В результате математических выкладок получаем систему, состоящую из двух уравнений с двумя неизвестными m и b.
 и далее
и далее
![]() ,
,
где
,
![]() ,
,
![]() ,
,
![]() – соответственно средние арифметические
значения xi,
yi,
– соответственно средние арифметические
значения xi,
yi,
![]() и xiyi
[1].
и xiyi
[1].
Например, классическая задача для экспериментальной химии определение Аррениусовских параметров. Известно, что зависимость константы скорости реакции от абсолютной температуры, как правило, хорошо описывается при помощи эмпирического уравнения Аррениуса.
![]() (2.2)
(2.2)
где k0 – множитель (предэкспонента), который в простейших случаях может быть вычислен исходя из молекулярных представлений о механизме элементарного акта; Ea – энергия активации реакции; R – универсальная газовая постоянная; T – абсолютная температура. Значения k0 и Ea, входящие в уравнение Аррениуса, находят из экспериментальных значений констант скорости реакции, измеренных при различных температурах.
Задача: Пользуясь экспериментальными данными о величине константы скорости химической реакции при различных температурах, найти значения предэкпоненциального множителя и энергии активации по формулам (2.1). Построить график и подобрать аппроксимирующую функцию с помощью встроенных функций программы Excel.
t, o |
550 |
560 |
570 |
580 |
590 |
600 |
610 |
620 |
630 |
k105, c-1 |
2,5 |
4,7 |
8,2 |
12,3 |
23,1 |
35,3 |
57,6 |
92,4 |
141,3 |
Прологарифмируем уравнение (2.2) чтобы получить линейную функцию:
![]()
Положим равными:
![]()
Составим в программе Excel таблицу (рис.9):
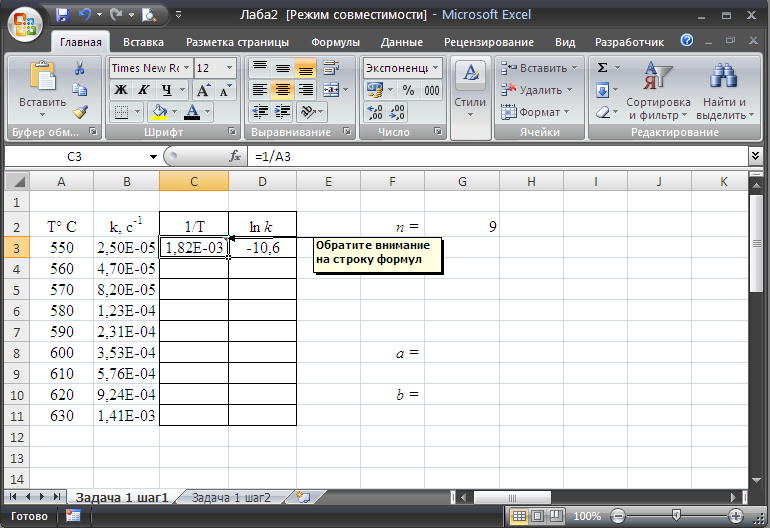
Рис. 9
Рассчитываем значения переменных для расчета a и b по формуле (2.1)

Рассчитываем значение постоянных параметров:

Строим график:

используя встроенные функции программы Excel:
Задача 1. Определение Аррениусовских параметров. Для реакции термического разложения этана получены следующие значения констант скоростей реакции первого порядка при разных температурах:
t, o |
420 |
430 |
440 |
450 |
460 |
470 |
490 |
500 |
510 |
k105, c-1 |
2,5 |
4,7 |
8,2 |
12,3 |
23,1 |
35,3 |
57,6 |
92,4 |
141,3 |
Постройте график зависимости lg k от 1/T. Рассчитайте энергию активации и предэкспоненциальный множитель, используя метод наименьших квадратов.
Задача 2. Определение гидратного числа для карбоновой кислоты. При изучении процесса экстракции карбоновой кислоты RCOOH из водного раствора с помощью органического растворителя обнаружилось, что в неводную фазу наряду с кислотой переходит некоторое количество воды, причем увеличение концентрации кислоты в неводной фазе сопровождается увеличением концентрации воды. Это дает возможность предположить, что при экстракции происходит образование гидросольвата вида RCOOH x1Н2О x2Z, где Z — обозначение молекулы экстрагирующего вещества. Образование гидросольвата, протекающее по реакции:
RCOOH + х1Н2О + x2Z = RCOOH х1Н2О x2Z
предполагает наличие линейной зависимости
между величинами концентрации
карбоновой кислоты х и воды у в
органическом растворителе после
экстракции:
![]() ,
где величины m и b
представляют собой соответственно
гидратное число карбоновой кислоты
(число молекул воды на одну молекулу
кислоты) и фоновую растворимость
воды в используемом растворителе.
,
где величины m и b
представляют собой соответственно
гидратное число карбоновой кислоты
(число молекул воды на одну молекулу
кислоты) и фоновую растворимость
воды в используемом растворителе.
На основании результатов анализа органической фазы после экстракции из водного раствора, содержащего различное количество карбоновой кислоты определить гидратное число карбоновой кислоты.
мМRCOOH |
4,0 |
7,0 |
9,4 |
10,8 |
13,0 |
16,0 |
18,4 |
20,0 |
мМH2O |
11,2 |
14,6 |
16,6 |
17,6 |
19,6 |
22,4 |
24,6 |
26,6 |
