
- •Коллоидная химия
- •Печатается по рекомендации Методического совета и по решению Редакционно-издательского совета Хакасского государственного университета им. Н. Ф. Катанова
- •Оглавление
- •Введение
- •Лекция 1. Дисперсные системы
- •1.1. Предмет коллоидной химии
- •1.2. Количественные характеристики дисперсных систем
- •1.3. Классификация дисперсных систем
- •Классификация по дисперсности
- •Классификация по агрегатному состоянию фаз
- •Классификация по взаимодействию дисперсной фазы и дисперсионной среды (по межфазному взаимодействию)
- •Классификация по межчастичному взаимодействию
- •1.4. Краткий исторический очерк
- •Лекция 2. Поверхностные явления
- •2.1. Природа поверхностной энергии
- •2.2. Поверхностное натяжение
- •2.3. Самопроизвольные процессы в поверхностном слое
- •2.4. Адсорбция. Общие положения, классификация
- •Лекция 3. Виды адсорбции
- •3.1. Адсорбция на границе «жидкий раствор – газ». Поверхностно-активные вещества
- •3.2. Адсорбция газов и паров на поверхности твердых тел. Капиллярная конденсация
- •3.3. Адсорбция растворенного в жидкости вещества на твердом адсорбенте. Смачивание. Адгезия
- •Лекция 4. Лиофобные золи (коллоидные растворы)
- •4.1. Методы получения лиофобных золей
- •4.1.1. Диспергационные методы
- •4.1.2. Конденсационные методы
- •4.1.3. Пептизация
- •4.2. Методы очистки коллоидных растворов
- •4.2.1. Диализ
- •4.2.2. Электродиализ
- •4.2.3. Ультрафильтрация
- •4.2.4. Обратный осмос
- •Лекция 5. Оптические и молекулярно-кинетические свойства коллоидных растворов
- •5.1. Оптические свойства коллоидных растворов
- •5.1.1. Рассеяние света
- •5.1.2. Поглощение света и окраска золей
- •5.1.3. Оптические методы исследования коллоидных растворов
- •5.2. Молекулярно-кинетические свойства коллоидных растворов
- •5.2.1. Броуновское движение
- •5.2.2. Диффузия
- •5.2.3. Осмотическое давление
- •Лекция 6. Электрические свойства коллоидных растворов
- •6.1. Электрокинетические явления в гидрофобных золях
- •6.2. Пути образования двойного электрического слоя
- •6.3. Строение двойного электрического слоя
- •6.4. Факторы, от которых зависит дзета-потенциал
- •Лекция 7. Устойчивость коллоидных растворов. Коагуляция
- •7.1. Седиментационная устойчивость дисперсных систем
- •7.2. Агрегативная устойчивость коллоидных растворов. Коагуляция
- •7.3. Факторы устойчивости лиофобных золей
- •7.4. Теория устойчивости лиофобных золей
- •7.4.1. Электростатические силы отталкивания
- •7.4.2. Ван-дер-Ваальсовы силы притяжения
- •7.5. Виды коагуляции электролитами
- •7.6. Гетерокоагуляция и гетероадагуляция
- •Лекция 8. Лиофильные системы. Микрогетерогенные системы
- •8.1. Лиофильные системы
- •8.1.1. Растворы коллоидных поверхностно-активных веществ
- •8.1.2. Растворы высокомолекулярных соединений
- •8.2. Микрогетерогенные системы
- •8.2.1. Суспензии
- •8.2.2. Эмульсии
- •8.2.3. Пены
- •8.2.4. Аэрозоли
- •Заключение
- •Библиографический список
- •Горенкова Галина Алексеевна
- •Коллоидная химия
- •655017, Г. Абакан, пр. Ленина, 94
1.2. Количественные характеристики дисперсных систем
Для характеристики ДС используются три величины:
1. Поперечный размер частиц – d. [d] = см; м. Для сферических частиц это диаметр сферы, для кубических частиц – ребро куба.
2. Дисперсность (раздробленность) – Д – величина, обратная поперечному размеру частиц:
![]() ;
;
![]() .
.
3. Удельная
поверхность (![]() )
– это межфазная поверхность (
)
– это межфазная поверхность (![]() ),
приходящаяся на единицу объема дисперсной
фазы (V) или ее массы (m).
),
приходящаяся на единицу объема дисперсной
фазы (V) или ее массы (m).
![]() ;
;
![]() ,
,
где
![]() – коэффициент формы частиц (для
сферических и кубических частиц
– коэффициент формы частиц (для
сферических и кубических частиц![]() ).
).
1.3. Классификация дисперсных систем
Классификация ДС может быть проведена на основе различных свойств.
Классификация по дисперсности
Рис. 1.2.
Зависимость
величины удельной поверхности от
размеров частиц

![]() графически выражается равносторонней
гиперболой (рис.1.2).
графически выражается равносторонней
гиперболой (рис.1.2).
Из графика видно,
что с уменьшением поперечных размеров
частиц величина удельной поверхности
существенно возрастает. Если кубик
с размером ребра 1 см измельчить до
кубических частиц с размерами
![]() см,
величина общей межфазной поверхности
возрастет с 6 см2
до 600 м2.
см,
величина общей межфазной поверхности
возрастет с 6 см2
до 600 м2.
При
![]() см
гипербола обрывается, так как частицы
уменьшаются до размеров отдельных
молекул, и гетерогенная система
становится гомогенной, в которой
межфазная поверхность отсутствует. По
степени дисперсности ДС делятся на:
см
гипербола обрывается, так как частицы
уменьшаются до размеров отдельных
молекул, и гетерогенная система
становится гомогенной, в которой
межфазная поверхность отсутствует. По
степени дисперсности ДС делятся на:
грубодисперсные системы,
 см;
см;микрогетерогенные системы,
 см;
см;коллоидно-дисперсные системы или коллоидные растворы,
 см;
см;истинные растворы,
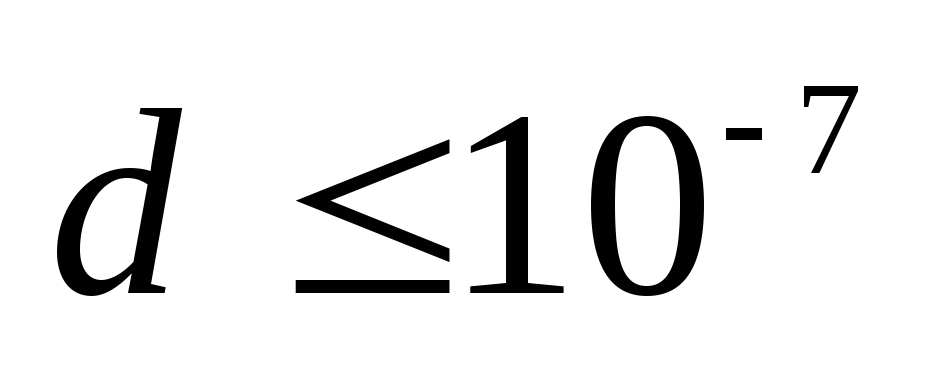 см.
см.
Необходимо подчеркнуть, что самую большую удельную поверхность имеют частицы дисперсной фазы в коллоидных растворах.
Классификация по агрегатному состоянию фаз
Классификация по агрегатному состоянию фаз была предложена Вольфгангом Оствальдом. В принципе возможно 9 комбинаций.
|
Агрегатное состояние дисперсной фазы |
Агрегатное состояние дисперсионной среды |
Название системы |
Примеры |
|
г |
г |
Аэрозоли |
Атмосфера Земли |
|
ж |
г |
Туман, слоистые облака | |
|
тв |
г |
Дымы, пыли, перистые облака | |
|
г |
ж |
Газовые эмульсии, пены |
Газированная вода, мыльная пена, лечебный кислородный коктейль, пивная пена |
|
ж |
ж |
Эмульсии |
Молоко, масло сливочное, маргарин, кремы и т.д. |
|
тв |
ж |
Лиозоли, суспензии |
Лиофобные коллоидные растворы, суспензии, пасты, краски и т.д. |
|
г |
тв |
Твердые пены |
Пемза, твердые пены, пенопласт, активированный уголь, пенобетон, хлеб, пористые тела в газе и т.д. |
|
ж |
тв |
Твердые эмульсии |
Вода в парафине, природные минералы с жидкими включениями, пористые тела в жидкости |
|
тв |
тв |
Твердые золи |
Сталь, чугун, цветные стекла, драгоценные камни, золь золота в стекле (рубиновое стекло) |
Классификация по взаимодействию дисперсной фазы и дисперсионной среды (по межфазному взаимодействию)
Эта классификация пригодна только для систем с жидкой дисперсионной средой. Г. Фрейндлих предложил подразделить ДС на два вида:
1) лиофобные, в них дисперсная фаза не способна взаимодействовать с дисперсионной средой, а следовательно, и растворяться в ней, к ним относятся коллоидные растворы, микрогетерогенные системы;
2) лиофильные, в них дисперсная фаза взаимодействует с дисперсионной средой и при определенных условиях способна в ней растворяться, к ним относятся растворы коллоидных ПАВ и растворы ВМС.
