
- •Физико-химические процессы в гидросфере Учебное пособие
- •Физико-химические процессы в гидросфере
- •1. Аномальные свойства воды и состав природных вод
- •Примеры решения задач
- •2. Способы классификации природных вод
- •Примеры решения задач
- •3. Основные процессы формирования химического состава природных вод
- •3.1. Процессы растворения газов в природных водах
- •3.2. Процессы растворения твердых веществ в природных водах
- •3.3. Жесткость природных вод
- •Примеры решения задач
- •4. Кислотно-основное равновесие в природных водоемах
- •4.1. Карбонатная система и рН атмосферных осадков
- •4.2. Растворимость карбонатов и рН подземных и поверхностных природных вод
- •4.3. Карбонатное равновесие в океане
- •4.4. Щелочность природных вод
- •4.5. Процессы закисления поверхностных водоемов
- •Примеры решения задач
- •5. Окислительно-восстановительные процессы в гидросфере
- •2.5.1. Окислительно-восстановительное равновесие
- •5.2. Взаимосвязь между окислительно-восстановительными и кислотно-основными характеристиками природных вод
- •5.3. Редокс-буферность природных вод
- •5.4. Особенности окислительно-восстановительных процессов в озерах
- •5.5. Особенности окислительно-восстановительных процессов в океане
- •5.6. Особенности окислительно-восстановительных процессов в подземных водах
- •5.7. Окислительно-восстановительные условия и миграция элементов
- •Примеры решения задач
- •Контрольные вопросы
- •Модуль № 2. Физико-химические процессы в гидросфере
- •Задачи ко второму учебному модулю
- •Ответы на задачи для самостоятельного решения
- •Литература
- •Приложение
- •Оглавление
4.3. Карбонатное равновесие в океане
Неорганические
соединения углерода в морской воде
представлены, как и в случае пресных
поверхностных и глубинных вод, диоксидом
углерода
и ионами НСО![]() и СО
и СО![]() .
Химические превращения, связывающие
между собой отдельные компоненты
карбонатной системы, едины для воды
океана и пресноводных водоемов. Однако
в отличие от пресных водных систем вода
океанов представляет собой
многокомпонентный раствор электролитов
средней концентрации, который
характеризуется высокими значениями
ионной силы
.
Химические превращения, связывающие
между собой отдельные компоненты
карбонатной системы, едины для воды
океана и пресноводных водоемов. Однако
в отличие от пресных водных систем вода
океанов представляет собой
многокомпонентный раствор электролитов
средней концентрации, который
характеризуется высокими значениями
ионной силы
Таблица 5. Коэффициенты
активности ионов НСО![]() и СО
и СО![]() в морской воде, вычисленные по константам
диссоциации угольной кислоты при
различных значениях хлорности
в морской воде, вычисленные по константам
диссоциации угольной кислоты при
различных значениях хлорности
|
Ионы |
Значение при хлорности (%о) | |||||
|
2 |
6 |
10 |
14 |
18 |
20 | |
|
НСО |
0,833 |
0,647
|
0,519 |
0,460 |
0,428 |
0,412 |
|
СО |
0,292 |
0,085 |
0,042 |
0,027 |
0,020 |
0,017 |
Для воды океана величина ионной силы может быть определена как функция хлорности:
I = 0,0147 + 0,03592 . С1%о + 0,000068 . (С1%о)2, (45)
где I – ионная сила раствора;
Cl%o – величина хлорности воды в промилле.
При расчетах
карбонатных равновесий для морской
воды следует использовать данные об
активности ионов. Коэффициенты активности
ионов НСО![]() и СО
и СО![]() резко уменьшаются при росте хлорности
воды (таблица 5). Их расчет по теории
Дебая—Хюккеля позволяет получитьудовлетворительные
результаты
лишь при малых значениях ионной силы
раствора (для морской поды — до хлорности
2%о). Экспериментальное определение
коэффициентов активности представляет
определенные трудности. В связи с этим
при расчете равновесий в морской
воде наиболее часто используют значения
концентрационных кажущихся, или
смешанных, констант. Так, для констант
диссоциации угольной кислоты по первой
и второй ступеням смешанные константы
диссоциации имеют вид:
резко уменьшаются при росте хлорности
воды (таблица 5). Их расчет по теории
Дебая—Хюккеля позволяет получитьудовлетворительные
результаты
лишь при малых значениях ионной силы
раствора (для морской поды — до хлорности
2%о). Экспериментальное определение
коэффициентов активности представляет
определенные трудности. В связи с этим
при расчете равновесий в морской
воде наиболее часто используют значения
концентрационных кажущихся, или
смешанных, констант. Так, для констант
диссоциации угольной кислоты по первой
и второй ступеням смешанные константы
диссоциации имеют вид:
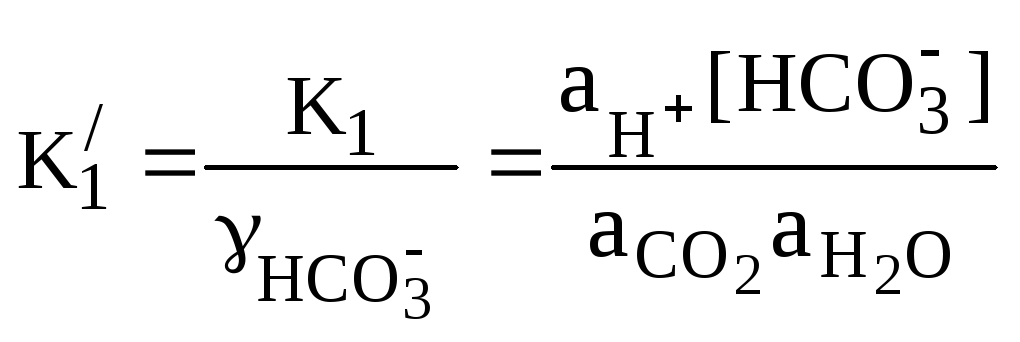 ;
(46)
;
(46)
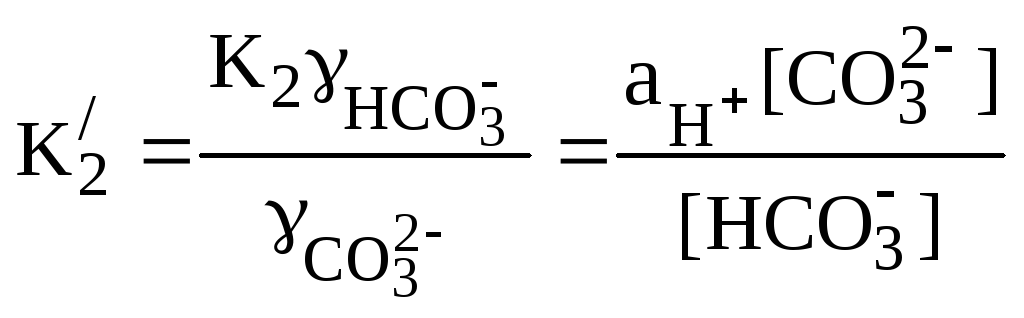 ,
(47)
,
(47)
где
![]() и
и
![]() – смешанные константы диссоциации;
– смешанные константы диссоциации;
К1 и К2 – термодинамические константы диссоциации.
В отличие от термодинамических констант, смешанные константы диссоциации угольной кислоты зависят от солености и хлорности морской воды. Их использование позволяет избежать необходимости введения коэффициентов активности, так как они уже учтены при экспериментальном определении констант. При различных хлорности и температуре воды значения констант диссоциации угольной кислоты по первой и второй ступеням могут быть найдены, например, по уравнениям:
![]() = 6,3784
– 0,01137 .
Сl%0
– 0,010765Т+ 1,563 .
10–4T2;
(48)
= 6,3784
– 0,01137 .
Сl%0
– 0,010765Т+ 1,563 .
10–4T2;
(48)
![]() = 9,8227 – 0,2719 .
С1%о
– 0,015215T
+ 1,3232 .
10–4T2.
(49)
= 9,8227 – 0,2719 .
С1%о
– 0,015215T
+ 1,3232 .
10–4T2.
(49)
Протекание процессом растворения или осаждения СаСО3 в рассматриваемой карбонатной системе океана зависит, помимо парциального давления СO2 и температуры, от солености воды и величины гидростатического давления. В океанах создается весьма неоднородное распределение насыщенности воды карбонатом кальция; по глубине обычно выделяют четыре зоны с различной степенью насыщения воды карбонатами.
Первая зона – поверхностный слой воды до глубины 300-800 м – значительно пересыщена. Этому способствуют сравнительно высокие температуры и низкие парциальные давления диоксида углерода.
Вторая зона охватывает слой глубиной до 1500-2000 м. В связи с интенсификацией процесса окисления органического вещества в этой зоне происходит увеличение Рсо2 и может возникнуть недонасыщение карбонатом кальция.
Третья зона (до 3500-4500 м) отличается состоянием, близким к равновесному.
Четвертая зона (от 3500-4500 м до дна) характеризуется ярко выраженным недонасыщением воды карбонатом кальция, связанным с ростом гидростатического давления.
