
- •Міністерство охорони здоров’я україни
- •Передмова
- •Тематичний план лекцій спеціальність “фармація” і “клінічна фармація”
- •Тематичний план практичних занять спеціальність “фармація”
- •Тематичний план практичних занять спеціальність “клінічна фармація”
- •Тематичний план самостійної роботи студентів спеціальність “фармація”
- •Тематичний план самостійної роботи студентів спеціальність “клінічна фармація”
- •Модуль 2. Кількісний аналіз Змістовий модуль 4
- •5. Завдання для закріплення матеріалу (виконати в робочому зошиті):
- •Тема 2 Введення в титриметричний аналіз
- •1. Значення теми для вивчення наступних дисциплін та практичної діяльності:
- •2. Основні питання теми:
- •3. Література:
- •4. Тестовий контроль та еталони відповідей:
- •5. Завдання для закріплення матеріалу (виконати в робочому зошиті):
- •Тема 3 Кислотно–основне титрування. Суть методу та його можливості
- •1. Значення теми для вивчення наступних дисциплін та практичної діяльності:
- •2. Основні питання теми:
- •3. Література:
- •4. Тестовий контроль та еталони відповідей:
- •5. Завдання для закріплення матеріалу (виконати в робочому зошиті):
- •5. Завдання для закріплення матеріалу (виконати в робочому зошиті):
- •6. Лабораторні роботи Лабораторна робота 4.1. Приготування робочого розчину хлоридної кислоти
- •Лабораторна робота 4.2. Приготування первинного стандартного (вихідного) розчину бури
- •Лабораторна робота 4.3. Встановлення молярної концентрації еквіваленту робочого розчину хлоридної кислоти
- •Лабораторна робота 4.4. Приготування робочого розчину натрію гідроксиду
- •Лабораторна робота 4.5. Приготування вихідного розчину оксалатної кислоти
- •Лабораторна робота 4.6. Встановлення молярної концентрації еквіваленту розчину NaOh
- •Лабораторна робота 4.7. Визначення оцтової кислоти
- •Тема 5 Кислотно-основне титрування Титрування багатоосновних кислот, солей, сумішей кислот, основ і солей
- •1. Значення теми для вивчення наступних дисциплін та практичної діяльності:
- •2. Основні питання теми:
- •3. Література:
- •4. Тестовий контроль та еталони відповідей:
- •5. Завдання для закріплення матеріалу (виконати в робочому зошиті):
- •6. Лабораторні роботи Лабораторна робота 5.1. Встановлення молярної концентрації еквіваленту робочого розчину соляної кислоти
- •Лабораторна робота 5.2. Визначення натрію гідроксиду і натрію карбонату в суміші
- •Тема 6 Кислотно-основне титрування у неводних середовищах
- •1. Значення теми для вивчення наступних дисциплін та практичної діяльності:
- •2. Основні питання теми:
- •3. Література:
- •4. Тестовий контроль та еталони відповідей:
- •5. Завдання для закріплення матеріалу (виконати в робочому зошиті):
- •Тема 7 Контроль засвоєння змістового модулю 4
- •Приклади тестових завдань по темам:
- •Тема 2. Введення в титриметричний аналіз
- •Тема 3. Кислотно–основне титрування. Суть методу та його можливості
- •Тема 4. Титрування кислот та основ
- •Тема 5. Титрування багатоосновних кислот, основ, сумішей кислот, основ
- •Тема 6. Кислотно-основне титрування у неводних середовищах
- •Тема 8 Семінарське заняття з розділу "Титриметричні методи аналізу. Кислотно-основне титрування" Змістовий модуль 5
- •Тема 9 Методи окислювально–відновного титрування Перманганатометрія
- •1. Значення теми для вивчення наступних дисциплін та практичної діяльності:
- •2. Основні питання теми:
- •3. Література:
- •4. Тестовий контроль та еталони відповідей:
- •5. Завдання для закріплення матеріалу (виконати в робочому зошиті):
- •6. Лабораторні роботи Лабораторна робота 9.1. Приготування робочого розчину перманганату калію
- •Лабораторна робота 9.2. Встановлення молярної концентрації еквіваленту вихідного розчину перманганату калію
- •Лабораторна робота 9.3. Визначення масової частки заліза в солі Мора
- •Тема 10 Йодометрія та йодиметрія
- •1. Значення теми для вивчення наступних дисциплін та практичної діяльності:
- •2. Основні питання теми:
- •3. Література:
- •4. Тестовий контроль та еталони відповідей:
- •5. Завдання для закріплення матеріалу (виконати в робочому зошиті):
- •6. Лабораторні роботи Лабораторна робота 10.1. Приготування робочого розчину тіосульфату натрію
- •Лабораторна робота 10.2. Приготування вихідного розчину дихромату калію
- •Лабораторна робота 10.3. Встановлення молярної концентрації еквіваленту розчину тіосульфату натрію
- •Лабораторна робота 10.4. Визначення аскорбінової кислоти
- •Тема 11 Бромато- та бромометричне титрування
- •1. Значення теми для вивчення наступних дисциплін та практичної діяльності:
- •2. Основні питання теми:
- •3. Література:
- •4. Тестовий контроль та еталони відповідей:
- •5. Завдання для закріплення матеріалу (виконати в робочому зошиті):
- •6. Лабораторні роботи
- •Лабораторна робота 11.3 Визначення масової частки стрептоциду в препараті
- •Тема 12 Нітритометричне титрування
- •1. Значення теми для вивчення наступних дисциплін та практичної діяльності:
- •2. Основні питання теми:
- •3. Література:
- •4. Тестовий контроль та еталони відповідей:
- •5. Завдання для закріплення матеріалу (виконати в робочому зошиті):
- •Лабораторна робота 12.3 Визначення масової частки стрептоциду в препараті
- •Тема 13 Контроль засвоєння змістового модулю 5
- •Приклади тестових завдань по темам:
- •Тема 9. Методи окислювально–відновного титрування. Перманганатометрія
- •Тема 10. Йодометрія та йодиметрія
- •Тема 11. Бромато- та бромометричне титрування
- •Тема 12. Нітритометричне титрування
- •Тема 14 Семінарське заняття з розділу "Окисно-відновне титрування" Змістовий модуль 6
- •Тема 15 Методи осаджувального титрування
- •1. Значення теми для вивчення наступних дисциплін та практичної діяльності:
- •2. Основні питання теми:
- •3. Література:
- •4. Тестовий контроль та еталони відповідей:
- •5. Завдання для закріплення матеріалу (виконати в робочому зошиті):
- •6. Лабораторні роботи: Лабораторна робота 15.1. Приготування 0,1 м розчину нітрату срібла
- •Лабораторна робота 15.2. Стандартизація 0,1 м розчину срібла нітрату за натрію хлоридом
- •Лабораторна робота 15.3. Визначення масової частки калію броміду за методом Мора
- •Тема 16 Методи комплексиметричного титрування
- •1. Значення теми для вивчення наступних дисциплін та практичної діяльності:
- •2. Основні питання теми:
- •3 Література:
- •4. Тестовий контроль та еталони відповідей:
- •5. Завдання для закріплення матеріалу (виконати в робочому зошиті):
- •6. Лабораторні роботи Лабораторна робота 16.1. Трилонометричне визначення магнію
- •Лабораторна робота 16.2. Визначення загальної твердості води комплексонометричним методом
- •Тема 17 Гравіметричний (ваговий) аналіз
- •1. Значення теми для вивчення наступних дисциплін та практичної діяльності:
- •2. Основні питання теми:
- •3. Література:
- •4. Тестовий контроль та еталони відповідей:
- •5. Завдання для закріплення матеріалу (виконати в робочому зошиті):
- •6. Лабораторні роботи Лабораторна робота 17.1 Визначення масової частки кристалізаційної води в мідному купоросі СuSo4·5h2o
- •Тема 18
- •Тема 19
- •Додаток
- •Цифрові значення критерія Ст’юдента t (p, f)
- •Числові значення контрольного критерію q (p, n)
- •Тема 1. Статистична обробка результатів аналізу 9
6. Лабораторні роботи
Лабораторна робота 11.1
Приготування робочого розчину бромату калію
Мета роботи: приготувати 1000 мл 0,1 Н розчину бромату калію.
Методика виконання роботи: 2,8 г калію бромату зважують на технічних терезах, розчиняють у воді і доводять об'єм розчину водою до 1 дм3.
Лабораторна робота 11.2
Встановлення молярної концентрації еквіваленту вихідного розчину бромату калію
Мета роботи: встановити молярну концентрацію еквіваленту розчину бромату калію.
Стандартизацію проводять йодометричним методом за способом заміщення. При цьому відбувається реакція:
|
BrO3–
+ 6H+
+
6 |
1 E0 = 1,45 B |
|
3I-
-
2 |
3 E0 = 0,545 B |
|
BrO3– + 9I- + 6H+ → Br- + 3[I3]- + 3H2O |
|
Йод , який вивільняється, відтитровують розчином тіосульфату натрію.
Методика
виконання роботи:
Аліквотний об’єм приготовленого розчину
калію бромату піпеткою переносять в
колбу з притертою пробкою, додають
приблизно 100 см3
води, 5 см3
хлороводневої кислоти (![]() ),
10 см3
розчину калію йодиду (
),
10 см3
розчину калію йодиду (![]() ),
закривають пробкою, збовтують і залишають
на 5 хвилин в захищеному від світла
місці. Йод, який виділився, титрують
0,1 Н стандартним розчином натрію
тіосульфату до світло-жовтого
забарвлення, потім додають 2-3 см3
розчину крохмалю і синій розчин титрують
до знебарвлення. Титрування повторюють
до одержання відтворюваних результатів.
Обчислюють молярну концентрацію розчину
калію бромату і поправковий коефіцієнт
(К).
),
закривають пробкою, збовтують і залишають
на 5 хвилин в захищеному від світла
місці. Йод, який виділився, титрують
0,1 Н стандартним розчином натрію
тіосульфату до світло-жовтого
забарвлення, потім додають 2-3 см3
розчину крохмалю і синій розчин титрують
до знебарвлення. Титрування повторюють
до одержання відтворюваних результатів.
Обчислюють молярну концентрацію розчину
калію бромату і поправковий коефіцієнт
(К).
Результати досліджень і розрахунків вносимо в таблицю 11.1.
Таблиця 11.1.
|
№ п/п |
Об’єм розчину калію бромату, см3 |
Об’єм розчину Na2S2O3 , витрачений на титрування, см3 |
Середнє значення об’єму розчину Na2S2O3, см3 |
Молярна концентрація еквіваленту розчину KBrO3 , моль/л |
|
|
|
|
|
|
|
|
|
| ||
|
|
|
| ||
|
|
|
|
Висновок: ______________________________________________________________________
________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
„Зараховано” „_____”_____________ ___________
Лабораторна робота 11.3 Визначення масової частки стрептоциду в препараті
Мета роботи: визначити масову частку стрептоциду в препараті.
Визначення основане на реакціях 1) і 2), що перебігають послідовно:
1) ВrО3 – + 5Вr – + 6Н+ 3Вr2 + 3Н2О
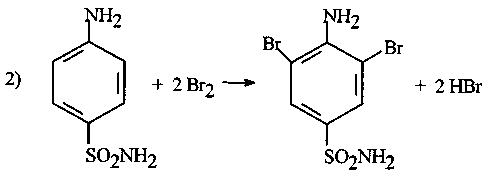
![]() ;
;
![]()
Методика виконання роботи: розраховану точну наважку стрептоциду переносять в колбу для титрування і розчиняють в 60 см3 2М розчину сірчаної кислоти. До приготовленої суміші додають 15 см3 розчину калію броміду, 5 крапель розчину метилового оранжевого і повільно, при енергійному помішуванні, титрують стандартним розчином калію бромату до знебарвлення розчину рожевого кольору. Титрування повторюють до одержання відтворюваних результатів і проводять розрахунки.
Результати дослідження і розрахунків заносять в таблицю 11.2.
Таблиця 11.2.
|
№ п/п |
Маса наважки стрептоциду, г |
Об’єм титранту KBrO3, см3 |
Масова частка стрептоциду, % |
Середнє значення масової частки стрептоциду, % |
Абсо-лютна помилка % |
Віднос-на помилка, % |
|
|
|
|
|
|
|
|
|
|
|
|
| |||
|
|
|
|
| |||
|
|
|
|
|
Висновок:_______________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
„Зараховано” „_____”_____________ ___________
Заняття № 10
