
V_N_Kovalev_Praktikum_po_farmakognozii
.pdf
Анализ ЛРС, содержащего хромоны |
1 1 1 |
|
|
|
|
|
|
|
кий, распадающийся на два полуплодика (мерикарпия), с брюшной стороны плоский, со спинной — выпуклый, с одного конца заостренный, с 5 продольными нитевидными ребрами. Длина зрелого полуплодика около 2 мм, толщина — около 1 мм. Цвет зрелых плодов — светло-коричневый или коричневатый, ребра более светлые, недозрелые плоды зеленоватые. Запах слабый. Вкус горьковатый, слегка жгучий.
П р и м е ч а н и е. Плоды |
виснаги |
|
морковевидной (амми зубной) можно |
|
|
отличить от плодов амми большой толь- |
|
|
ко при микроскопическом, химическом |
|
|
и хроматографическом исследовании. |
|
|
Зрелые плоды амми зубной не содер- |
|
|
жат в экзокарпии друзы кальция окса- |
|
|
лата; имеют крупные реберные и мел- |
|
|
кие ложбиночные секреторные каналы, |
|
|
темно-бурую окраску семенной оболоч- |
|
|
ки и «зубчатые клетки» на |
границе |
Рис. 6.2. Амми зубная: цветущий побег и плод |
с эндокарпием. У незрелых плодов два |
|
|
последних признака отсутствуют.
Задание 3. Сравните диагностические признаки плодов амми зубной с осо бенностями плодов других растений сем. зонтичных (стр. 104).
Задание 4. Изучите (цв. вкл. IV, рис. 2) хроматограмму экстрактов амми большой и амми зубной (виснаги морковевидной). Обратите внимание на отли чие в качественном составе. Зарисуйте схему хроматограммы в лаборатор ном журнале и расчитайте Rf виснадина. Напишите формулы виснадина и вис нагина.
Задание 5. Изучите числовые показатели, характеризующие доброкачествен ность плодов виснаги морковевидной. Обратите внимание, что стандартизация сырья проводится по сумме хромонов.
Числовые показатели. Суммы хромонов — не менее 0,8 %; влаги — не более 12 %; золы общей — не более 10 %; частиц, проходящих сквозь сито с отверстиями диаметром 0,2 мм,— не более 1,0 %; других частей растения — не более 6 %; посторонних примесей: органической — не более 2 %; минеральной — не более 1,5 %.
Задание 6. Определите количество хромонов в плодах виснаги морковевид ной. Сделайте заключение о соответствии исследуемого образца сырья следующе му требованию АНД: «не менее 0,8 % суммы хромонов в пересчете на келлин».
Методика. Аналитическую пробу сырья измельчают до размера частиц, проходящих сквозь сито с отверстиями диамером 0,2 мм. Около 0,25 г сырья (точная навеска) помещают в колбу вместимостью 150 мл, добавляют 50 мл дистиллированной воды и кипятят с обратным холодильником в течение 30 мин. К кипящей смеси добавляют 2 мл 10 %-ного раствора свинца ацетата
1 1 2 |
|
Фенольные соединения. Тема 6. Хромоны |
|
|
|
|
|
|
ипродолжают кипятить еще 3 мин. Горячую смесь фильтруют на воронке Бюхнера под вакуумом. Колбу и сырье на фильтре промывают кипящей водой три раза по 30 мл. Фильтрат количественно переносят в колбу вместимостью 200 мл, добавляют 1 г однозамещенного натрия фосфата и кипятят еще 3 мин. Горячее извлечение фильтруют непосредственно в делительную воронку вместимостью 500 мл; колбу и фильтр промывают кипящей водой три раза по 30 мл и охлаждают фильтрат до комнатной температуры. К водному извлечению в делительной воронке прибавляют 25 мл хлороформа, встряхивают и дают отстояться до полного разделения фаз. Нижний слой сливают в колбу вместимостью 200 мл. Водный слой обрабатывают еще 3 раза по 25 мл хлороформа как описано выше. Объединенные хлороформные извлечения промывают 5 мл дистиллированной воды и обезвоживают, фильтруя через бумажный фильтр с 2 г безводного натрия сульфата, предварительно смоченные хлороформом, в колбу вместимостью 200 мл; фильтр промывают три раза по 10 мл хлороформа и промывную жидкость сливают в ту же колбу. Объединенное хлороформное извлечение упаривают досуха. Остаток растворяют в 80 мл раствора 20 моль/л кислоты серной при осторожном подогревании. Охлажденный раствор количественно переносят в мерную колбу вместимостью 100 мл, объем раствора доводят водой до метки, перемешивают
иоставляют на 5—10 мин.
25 мл раствора фильтруют и измеряют оптическую плотность на фотоэлектроколориметре в кювете с толщиной слоя 10 мм при длине волны 465 нм. В качестве раствора сравнения применяют воду. По градуировочному графику* находят содержание суммы хромонов в пересчете на келлин.
Содержание суммы хромонов Х (%) в пересчете на абсолютно сухое сырье вычисляют по формуле
а. 100 . 100 . 100
Х= ———————————— , m . (100 – W) . 1000
где а — содержание суммы хромонов в 1 мл испытуемого раствора, мг; m — масса сырья, г;
W — потеря в массе при высушивании сырья, %.
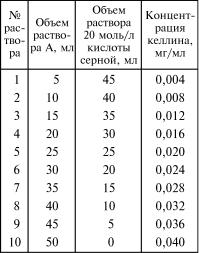
П р и м е ч а н и е. Построение градуировочного |
|
графика*. 0,02 г келлина помещают в мерную кол- |
Приготовление рабочих растворов |
бу вместимостью 500 мл и растворяют в раство- |
|
ре 20 моль/л кислоты серной. Доводят объем ра- |
|
створа тем же растворителем до метки и переме- |
|
шивают (раствор А). Затем готовят ряд рабочих |
|
растворов, смешивая определенные объемы рас- |
|
твора А с раствором 20 моль/л кислоты серной |
|
(см. табл.). |
|
Измеряют оптическую плотность рабочих рас- |
|
творов, как указано выше, и строят градуиро- |
|
вочный график, откладывая на оси абсцисс кон- |
|
центрацию вещества, а на оси ординат — опти- |
|
ческие плотности растворов. |
|
Задание 7. Известно, что плоды виснаги морковевидной перерабатывают на фармацев тических предприятиях. Напишите в лабора торном журнале название препаратов и их применение.

Анализ ЛРС, содержащего хромоны |
1 1 3 |
|
|
|
|
|
|
|
? |
КОНТРОЛЬНЫЕ ВОПРОСЫ К ТЕМАМ «КУМАРИНЫ И ХРОМОНЫ»
1. Дайте определение понятия «кумарины» и «хромоны».
2.Охарактеризуйте химическое строение и перечислите классы кумаринов и хромонов.
3.Охарактеризуйте физико-химические свойства кумаринов и хромонов.
4.Напишите формулы кислоты кумариновой, кумарина, псоралена, ангелицина, пиранокумарина, хромона, фуранохромона, келлина.
5.Охарактеризуйте методы выделения кумаринов и хромонов из ЛРС, а также очистки экстракта от сопутствующих веществ.
6.Перечислите методы обнаружения кумаринов и хромонов в ЛРС.
7.Что происходит при взаимодействии кумаринов со щелочью? Почему исчезает желтая окраска при подкислении?
8.Как провести реакцию азосочетания? Является ли она специфической для кумаринов и хромонов?
9.Напишите химизм лактонной пробы и реакции азосочетания.
10.Как флюоресцируют кумарины в УФ-свете?
11.Назовите основные методы количественного определения кумаринов и хромонов в ЛРС.
12.Перечислите основные этапы количественного определения кумаринов в листьях инжира и келлина в амми зубной.
13.Идентифицируйте по гербарному образцу одно из лекарственных растений: донник лекарственный, каштан конский, амми большая, пастернак посевной, смоковница обыкновенная, псоралея костянковая, дягиль лекарственный, рута душистая, амми зубная, укроп огородный, морковь дикая. Напишите латинское название растения и семейства.
14.Идентифицируйте по внешнему виду один из образцов ЛРС: трава донника, семена каштана, плоды амми большой, плоды пастернака, листья смоковницы, плоды псоралеи, корни дягиля, трава руты душистой, плоды амми зубной, плоды укропа, плоды моркови. Напишите латинское название сырья, лекарственного растения и семейства.
15.Укажите сроки заготовки и меры предосторожности при сборе сырья: донника лекарственного, каштана конского, амми большой, пастернака посевного, смоковницы обыкновенной, псоралеи костянковой, дягиля лекарственного, руты душистой.
16.Расскажите об особенностях сушки сырья: донника лекарственного, каштана конского, амми большой, пастернака посевного, смоковницы обыкновенной, псоралеи костянковой, дягиля лекарственного, руты душистой, амми зубной, укропа огородного, моркови дикой.
17.На основании каких морфологических признаков амми большую, амми зубную, укроп огородный, морковь дикую, пастернак посевной и дягиль лекарственный можно отнести к семейству зонтичных?
18.Как отличить донник лекарственный от близких видов?
19.Расскажите о путях и способах использования сырья: донника лекарственного, каштана конского, амми большой, пастернака посевного, смоковницы обыкновенной, псоралеи костянковой, дягиля лекарственного, руты душистой.
ТЕМА
7Ксантоны и лигнаны
Ксантоны — группа биологически активных веществ фенольной |
природы |
с общей формулой С6—С1—С6, в основе которых лежит дибензо-γ |
-пирон. |
ксантон (дибензо-γ-пирон) |
гентизин |
мангиферин |
Первый представитель этой группы был выделен Генри в 1821 г. из корней Gentiana lutea и назван гентизином.
Наиболее распространен в природе ксантоновый С-гликозид мангиферин, впервые выделенный из плодов манго — Mangifera indica. В настоящее время из растений семейств горечавковых, зверобойных, тутовых идентифицировано более 300 ксантонов.
Ксантоны в зависимости от структуры разделяют на пять групп. Собственно ксантоны — это дибензо-γ-пироны, которые имеют в качестве
заместителей окси-, алкокси-, алкильные группы и их О- и С-гликозиды. Фураноксантоны накапливаются как у высших, так и у низших растений.
Пирано- и дигидропираноксантоны линейные и ангулярные; дипираноксантоны.
Ксантолигнаны, у которых фрагмент фенилпропана связан с ксантоном. Ксантоны — кристаллические вещества желтого цвета (от греческого «xanthos» или «xanthus», что означает «желтый»). В растениях находятся в свободном виде и в форме гликозидов. Агликоны ксантонов растворяются в хлороформе, ацетоне, метаноле, этаноле, не растворяются в воде; гликозиды хорошо растворимы в воде, низших спиртах и не растворяются в хлороформе. В УФ-свете ксантоны флюоресцируют желтым или желто-зеленым цветом. УФ-спектры ксантонов характеризуются четырьмя полосами поглощения
в области: 230—260, 260—290, 285—300 и 325—395 нм.
Ксантоны с замещением в положениях 1, 3, 5, 8 имеют антивирусную активность; в 1, 3, 7, 8 — противотуберкулезную; в 1, 6 и 1, 3 — являются ингибиторами саркомы; в 1, 3, 8 — проявляют противогрибковый эффект. Мангиферин стимулирует ЦНС, в больших дозах оказывает кардиотоническое, диуретическое, антибактериальное и противовоспалительное действие.
Лигнаны — это димерные фенольные соединения, производные фенилпропана (С6—С3)2, фрагменты которых соединены С—С-связями между средними атомами углерода боковых цепей (между Сβ).

Анализ ЛРС, содержащего ксантоны и лигнаны |
1 1 5 |
|
|
|
|
|
|
|
Термин «лигнан» был введен в 1936 г. Впервые эти соединения были получены из древесины (лат. «lignum» — древесина, дерево), на основании чего они и получили свое название.
Разнообразие лигнанов обусловлено расположением фенильных ядер, степенью насыщенности боковых цепей и окисленности γ-углеродных атомов.
Лигнаны в зависимости от расположения ароматических ядер делятся на три группы: собственно лигнаны, неолигнаны и лигноиды.
Собственно лигнаны — соединения, в молекулах которых арилпропановые (С6—С3)-фрагменты соединены по типу «хвост к хвосту». Известно шесть типов структур этой группы: диарилбутановый, дигидронафталиновый, диарилтетрагидрофурановый, тетрагидронафталиновый, диоксабициклооктановый (сезаминовый) и диарилоктановый.
Неолигнаны — соединения, в молекулах которых арилпропановые фрагменты соединены между собой по типу «голова к хвосту». В положении Сβ—Сγ часто бывает двойная связь.
Лигноиды — соединения, в которых фрагмент фенилпропана (С6—С3) связан с другими группами фенольных соединений (флаволигнаны, ксантолигнаны, кумаринолигнаны).
Лигнаны — бесцветные кристаллические вещества. В растениях находятся в свободном состоянии и в виде гликозидов, часто растворенных в жирных или эфирных маслах, смолах. Лигнаны растворяются в бензоле, эфире, низших спиртах; не растворяются в воде. В УФ-свете флюоресцируют голубым или желтым цветом. Лигноиды проявляют свойства тех соединений, которые входят в их состав.
Лигнаны оказывают стимулирующее и адаптогенное (схизандрин и производные сирингорезинола), противоопухолевое (подофиллотоксин), антигеморрагическое (сезамин), противомикробное (арктиин), гепатозащитное (флаволигнан силибин) действие.
Анализ ЛРС, содержащего ксантоны и лигнаны
Объекты для лабораторного исследования: трава золототысячника, семена расторопши, корневища и корни элеутерококка, плоды и семена лимонника китайского, корневища с корнями подофилла.
Объекты для самостоятельного изучения: корни горечавки (см. тему «Горечи»), перец кубеба, кунжут индийский.
ТРАВА ЗОЛОТОТЫСЯЧНИКА — Herba Centaurii

1 1 6 |
|
Фенольные соединения. Тема 7. Ксантоны и лигнаны |
|
|
|
|
|
|
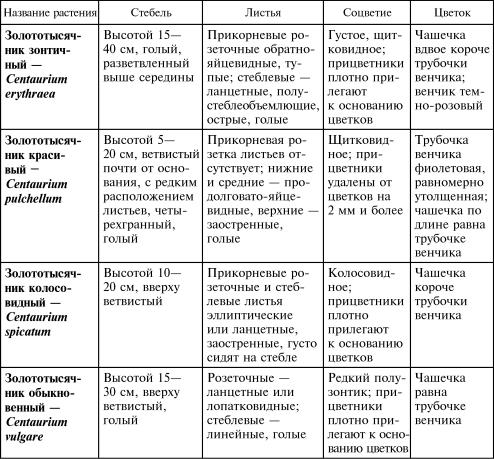
Задание 1. Сравните по гербарным образцам, рис. 7.1 и описанию, данному в табл. 7.1, золототысячник обыкновенный и другие виды золототысячника. Об ратите внимание на синонимы лекарственного растения. Запишите в лаборатор ный журнал название сырья, лекарственного растения и семейства на русском и латинском языках.
Рис. 7.1. Золототысячник зонтичный — а; золототысячник красивый — б; золототысячник обыкновенный — в
Задание 2. Проведите анализ травы золототысячника в сравнении со стан дартным образцом сырья (цв. вкл. XIII, рис. 3). Запишите, используя схему 10, основные внешние признаки исследуемого сырья.
Напишите русские и латинские названия возможных примесей. Внешние признаки по ст. 48 ГФ XI. Стебли голые, простые или разветв-
ленные, четырехгранные, иногда с крылатыми ребрами. Листья сидячие, супротивные, с 5 жилками, средние — продолговато-яйцевидные, голые, цельнокрайние, с 5 жилками, верхние — продолговатоили линейно-лан- цетные. Соцветия верхушечные, щитковидные. Цветки правильные. Чашечка сростнолистная с 5 долями. Венчик с длинной цилиндрической трубкой и пятираздельным отгибом. Тычинок пять. Цвет стеблей, листьев и чашечки — желтовато-зеленый, венчика — розовато-фиолетовый, желтовато-розо- вый и желтый. Запах слабый. Вкус горький.
Задание 3. Проведите количественное определение суммы ксантонов в траве золототысячника. Запишите расчеты в лабораторный журнал. Сравните получен
Анализ ЛРС, содержащего ксантоны и лигнаны |
1 1 7 |
|
|
|
|
|
|
|
Т а б л и ц а 7.1
Отличительные признаки видов золототысячника
ные результаты с числовыми показателями ЛРС и сделайте заключение о соот ветствии исследуемого образца требованиям АНД по количеству ксантонов. По думайте, к каким природным соединениям фенольной природы приближаются ксантоны по физико химическим свойствам?
П р и м е ч а н и е. Ксантоны извлекают из образца ЛРС спирто-водной смесью с добавлением кислоты хлористоводородной для разрушения межмолекулярных связей и лучшей экстракции действующих веществ. Сопутствующие водорастворимые вещества удаляют элюацией водой на колонке с полиамидным сорбентом. Сумму ксантонов отделяют от других веществ фенольной природы элюированием спиртом. Продвижение окрашенной зоны ксантонов контролируют визуально в видимом и УФ-свете. Собственно количественное определение ксантонов проводят спектрофотометрически при длине волны, соответствующей максимуму поглощения спектра алпизарина, после проведения реакции со спиртовым раствором алюминия хлорида.
Методика. Аналитическую пробу сырья измельчают до размера частиц, проходящих сквозь сито с отверстиями диаметром 2 мм. Около 5 г (точная навеска) измельченного сырья помещают в колбу вместимостью 250—300 мл, прибавляют 150 мл 60 %-ного спирта, содержащего 5 % кислоты хлористоводородной, взвешивают, присоединяют к обратному холодильнику и нагревают на кипящей водяной бане в течение 3 ч.
1 1 8 |
|
Фенольные соединения. Тема 7. Ксантоны и лигнаны |
|
|
|
|
|
|
После охлаждения до комнатной температуры колбу вновь взвешивают
идоводят до первоначальной массы тем же спиртом. Содержимое колбы фильтруют через воронку диаметром 70 мм с бумажным фильтром в колбу вместимостью 250 мл, отбрасывая первые 5 мл фильтрата. 2 мл фильтрата вносят в колонку с полиамидным сорбентом. Колонку промывают 50 мл воды со скоростью 3,5—4 мл в минуту. Водный элюат отбрасывают. Сумму ксантонов элюируют 50 мл 95 %-ного спирта, контролируя их продвижение в видимом
иУФ-свете по желтой зоне. При достижении зоной нижней части сорбента элюат этой зоны собирают в мерную колбу вместимостью 50 мл. Объем элюата доводят до метки 95 %-ным спиртом и тщательно перемешивают.
К5 мл элюата прибавляют 5 мл спиртового раствора алюминия хлорида (0,05 моль/л) и через 15—20 мин измеряют оптическую плотность на спектрофотометре при длине волны 410 нм в кювете с толщиной слоя 10 мм на фоне контрольного опыта.
Параллельно измеряют оптическую плотность раствора стандартного образца (ФСО) алпизарина в смеси со спиртовым раствором алюминия хлорида (0,05 моль/л).
Содержание суммы ксантонов в пересчете на алпизарин в абсолютно сухом сырье X, %, вычисляют по формуле
D · 5 · 100 · 150 · m0 · 100 · 100 |
300 · D · m0 · 100 |
Х = ———————————————————= ———————————, |
|
m · D0 · 2 · 100 · 25 · 5 · (100 – W ) |
D0 · m · (100 – W ) |
где D — оптическая плотность исследуемого раствора;
D0 — оптическая плотность раствора ФСО алпизарина;
m0 — масса ФСО алпизарина, г;
m— масса сырья, г;
W — потеря в массе при высушивании сырья, %.
П р и м е ч а н и е. 1. Приготовление колонки: 1,5 г полиамидного сорбента помешают в стаканчик вместимостью 50 мл, прибавляют 30 мл воды, перемешивают и переносят взвесь в колонку диаметром 2 см, высотой 28 см с пористым стеклянным фильтром и помещенным на него ватным тампоном, предварительно смоченным водой.
Колонку заполняют при открытом спускном кране, сливают воду, оставив столб воды 1 см над сорбентом.
2. Приготовление раствора стандартного образца (ФСО) алпизарина: около 0,05 г (точная навеска) стандартного образца алпизарина (в пересчете на 100 %-ное вещество) растворяют в смеси ацетон—вода (1:1) в мерной колбе вместимостью 100 мл; 1 мл полученного раствора переносят в мерную колбу вместимостью 25 мл и доводят объем раствора 95 %-ным спиртом до метки.
Срок хранения 1 мес.
3. Проведение контрольного опыта: колонку с полиамидом, подготовленную, как указано выше, промывают 50 мл воды со скоростью 3,5—4 мл в минуту. Водный элюат отбрасывают и колонку промывают 50 мл 95 %-ного спирта, который собирают в мерную колбу вместимостью 50 мл, затем доводят объем элюата спиртом до метки и перемешивают.
4. Приготовление спиртового раствора алюминия хлорида (0,5 моль/л): 12,5 г алюминия хлорида помещают в мерную колбу вместимостью 1 л, растворяют в 95 %-ном спирте и доводят объем раствора тем же спиртом до метки.
Задание 4. Изучите числовые показатели, характеризующие доброкачествен ность травы золототысячника в сравнении с PhEur. Обратите внимание на коли чество действующих веществ.
Числовые показатели. Суммы ксантонов в пересчете на алпизарин — не менее 0,9 %; влажность — не более 14 %; золы общей — не более 7 %;
Анализ ЛРС, содержащего ксантоны и лигнаны |
1 1 9 |
|
|
|
|
|
|
|
золы, нерастворимой в 10 %-ном растворе кислоты хлористоводородной,— не более 1,5 %; корней, в том числе отделенных при анализе,— не более 2 %; органической примеси — не более 1 %; минеральной примеси — не более 1 %.
Числовые показатели по PhEur. Показатель горечи — не менее 2000; влажность — не более 10 %; золы общей — не более 6,0 %; золы, нерастворимой в 10 %-ном растворе кислоты хлористоводородной,— не более 1,5 %; корней, в том числе отделенных при анализе,— не более 2 %; органической примеси — не более 1 %; минеральной примеси — не более 1 %.
Задание 5. Известно, что траву золототысячника применяют для возбужде ния аппетита. Запишите в лабораторном журнале препараты золототысячника. Отметьте, что применение ЛРС зависит от содержания горечей, которые относят ся к классу монотерпеновых гликозидов.
ПЛОДЫ РАСТОРОПШИ — Fructus Silybi
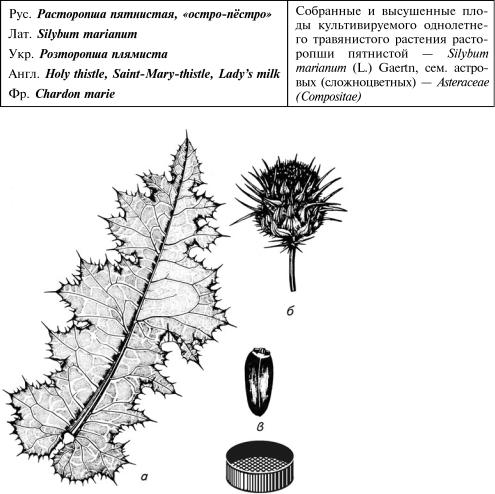
Рис. 7.2. Расторопша пятнистая:
а — лист; б — соцветие; в — плод
Задание 1. Изу чите по гербарному образцу и рис. 7.2 расторопшу пятнис тую. Запишите в ла бораторный журнал название сырья, ле карственного расте ния и семейства на русском и латинском языках. Обратите внимание, что народ ное название «ост ро пёстро» растение получило по морфо логическим особен ностям листьев, ко торые по краю снабжены острыми колючками и имеют белые пятна по всей листовой пластинке.
Задание 2. Про ведите анализ семян расторопши в срав нении со стандарт

1 2 0 |
|
Фенольные соединения. Тема 7. Ксантоны и лигнаны |
|
|
|
|
|
|
ным образцом сырья (цв. вкл. VI, рис. 3). Запишите, используя схему 9, основные внешние признаки исследуемого сырья.
Внешние признаки по ТУ 64-4-30—81. Плоды — семянки яйцевидной формы, слегка сплюснутые с боков, длиной от 5 до 8 мм, шириной от 2 до 4 мм, толщиной от 1 до 3 мм. Верхушка косо усеченная с выступающим тупым толстым остатком столбика или без него. Основание семянки тупое; плодовый рубчик щелевидный или округлый, слегка смещенный в бок. Поверхность гладкая, иногда продольно-морщинистая, блестящая или матовая. Цвет — от черного до светло-коричневого, иногда с сиреневым оттенком, часто плоды пятнистые, валик более светлый. Запах отсутствует. Вкус слегка горьковатый.
Задание 3. Изучите хроматограмму метанольного экстракта обезжиренных плодов расторопши (цв. вкл. VI, рис. 2). Обратите внимание на стабильность хи мического состава различных образцов сырья.
Задание 4. Изучите числовые показатели, характеризующие доброкачествен ность плодов расторопши. Объясните, можно ли использовать сырье с содержа нием флаволигнанов менее 2,7 %?
Числовые показатели. Содержание флаволигнанов — не менее 2,7 %; влажность — не более 12 %; зола общая — не более 6 %; содержание других частей расторопши — не более 2 %; органической примеси — не более 2 %; минеральной примеси — не более 1 %.
Задание 5. Известно, что плоды расторопши пятнистой применяют как гепа топротекторное средство. Запишите в лабораторном журнале препараты расто ропши пятнистой отечественного и зарубежного производства.
КОРНЕВИЩА И КОРНИ ЭЛЕУТЕРОКОККА —
Rhizomata et radices Eleutherococci
Задание 1. Изучите элеутерококк колючий по гербарному образцу и рис. 7.3. Запишите в лабораторный журнал название сырья, лекарственного растения и семейства на русском и латинском языках.
Задание 2. Проведите анализ корневищ и корней элеутерококка в сравне нии со стандартным образцом сырья. Запишите, используя схему 12, основные внешние признаки исследуемого сырья.
Внешние признаки по ФС 42-2725—90. Куски корневищ и корней цельные или расщепленные вдоль, длиной до 8 см, толщиной не более 4 см, деревянистые, твердые, прямые или изогнутые, иногда разветвленные. Кора тонкая, плотно прилегает к древесине. Корневища с поверхности гладкие или слабо продольно-морщинистые, местами со следами отломанных корней, почками и рубцами (следы отмерших листьев и стеблей). Поверхность корней
