
- •Биохимия: предмет, задачи. Липиды, углеводы, белки: структура, химические и физико-химические свойства, классификация, биологическая роль.
- •1. Структура белков.
- •Ферменты: структура, свойства, механизм действия
- •Ферменты: номенклатура, классификация, применение в сельском хозяйстве
- •Цикл трикарбоновых кислот: реакции, биологическая роль. Нарушение энергетического обмена.
- •Гидролиз белков в органах пищеварительной системы. Метаболизм аминокислот в клетках.
- •Биосинтез белков.
- •Образование конечных продуктов белкового обмена. Патология белкового обмена.
- •Аэробный гликолиз. Глюконеогенез. Пентозный цикл. Патология углеводного обмена.
- •Гидролиз липидов в органах пищеварительной системы. Окисление глицерола и жирных кислот. Кетоновые тела
- •Биосинтез глицерола, жирных кислот, ацилглицеролов, фосфоглицеридов и холестерола. Патология липидного обмена.
- •Водно-солевой обмен: роль в организме, регуляция
- •Регуляция обмена веществ. Эндокринная система
- •Биохимический состав биологических жидкостей: крови, мочи,
- •Биохимический состав нервной и мышечной ткани
- •Молоко: биохимический состав, механизм образования. Биохимический состав яйца.
Лекции по биологической химии
Лекция №1
Биохимия: предмет, задачи. Липиды, углеводы, белки: структура, химические и физико-химические свойства, классификация, биологическая роль.
План.
1. Структура белков.
2. Стрктура углеводов.
3. Структура липидов.
1. Структура белков.
Белки - органические соединения, состоящие из аминокислот, связанных между собой пептидной связью. Аминокислоты - кабоновые кислоты, содержащие аминную и карбоксильную групп, находящиеся у одного и того же углеродного атома.В состав белков входят 22 аминокислоты, которые по свойствам боковой цепи делят на 4 группы: гидрофобные,
гидрофильные неионные, гидрофильные с отрицательным зарядом и гидрофильные с положительным зарядом.
I. гидрофобные аминокислоты.




Глицин. Аланин Валин Лейцин




Изолейцин Метионин Цистин Фенилаланин


Триптофан Пролин
II.гидрофильные неионные аминокислоты.




Серин Треонин Аспарагин Глутамин

Оксипролин
III. гидрофильные аминокислоты с состоящая из остатковα-Д-глюкопиранозы.
.




Аспарагиновая Глутаминовая Цистеин Тирозин
кислота кислота
IV. гидрофильные аминокислоты с положительно заряженным радикалом.



Лизин Аргинин Гистидин
Физико-химические свойства белков.
Находящиеся на поверхности белковой молекулы радикалы аспарагиной, глутаминовой кислот, тирозина и цистина, диссоциируя на ион водорода, придают ей отрицательный заряд. Радикалы лизина, аргинина и гистидина, диссоциирующие на ион гидроксила, наоборот придают молекуле белка положительный заряд. У большинства белков отрицательных зарядов на молекуле больше. Благодаря заряду они отталкиваются друг от друга и не слипаются в конгломераты. Слипанию препятствует также наличие вокруг молекулы белка водной оболочки.
В слабокислой среде тормозится диссоциация части отрицательно заряженных радикалов аминокислот, количество положительных и отрицательных зарядов сравнивается, молекулы белков становятся электронейтральными и слипаются в конгломераты и выпадабт в осадок. Слипанию их способствует и нагревание, приводящее к потере водной оболочки. Значение рН, при котором молекула белка становится электронейтральной, называется изоэлектрической точкой белка.
Классификация белков. Белки делятся на простые, состоящие только из аминокислот (альбумины, глобулины, проламины, глютелины, протамины, гистоны и пртеиноиды) и сложные, состоящие из белковой и небелковой части. У хромопротеинов небелковой частью может быть окрашенное вещество (например гем у гемоглобина), у липопротеинов - липидная часть, у гликопротеинов - гетерополисахарид, у фосфопротеинов - фосфорная кислота, у нуклеопротеинов - ДНК или РНК. Нуклеиновые кислоты состоят из нуклеотидов. Последние состоят из азотистого основания, пуринового (аденин и гуанин) или пиримидинового [цитозин, тимин (у ДНК) или урацил (у РНК)], дезоксирибозы (у ДНК) или рибозы (у РНК) и фосфорной кислоты. Сборка нуклеотида из аденина, дезоксирибозы и фосфорной кислоы показана ниже.

Молекула ДНК состоит из четырех разновидностей нуклеотидов6 дезоксиаденозинмонофосфата (дАМФ), дезоксигуанозинмонофосфата (дГМФ), дезоксицитидинмонофосфата (дЦМФ) и дезокситимидинмонофосфата (дТМФ). Нуклеотиды связаны между собой посредством фосфодиэфирной связи межде вторым углеродным атомом дезоксирибозы и фосфорной кислотой соседнего нуклеотида, как показано в фформуле фрагмента ДНК, состоящего из дАМФ, дГМФ, дЦМФ и дТМФ.

Структура и биологическая роль углеводов.
Углеводы – полиоксикарбонильные соединения, являющиеся по своей природе альдо- или кетоспиртами или их производными. По химической структуре различают: 1) моносахариды (рибоза, дезоксирибоза, глюкоза, галактоза, фруктоза и др.); 2) олигосхариды (сахароза, мальтоза, лактоза и др.); 3) гомопосахариды (гликоген, крахмал, клетчатка и др.) и гетероплсахариды (гиалуроновая, хондроитинсерная кислоты, кератансульфат и др.).
1. Моносахариды.

Превращение Д-дезоксирибозы в α-Д-дезоксирибофуранозу.
Превращение
Д-глюкозы в α-Д-глюкопиранозу
Превращение Д-глюкозы в α-Д-глюкопиранозу

Превращение Д-глюкозы в β-Д-глюкопиранозу

Превращение Д-глюкозы в β-Д-глюкопиранозу

Превращение Д-фруктозыозы в β-Д-фруктофуранозу
2. Олигисахариды

Мальтоза
Лактоза

Сахароза.
3. Гомоолисахариды

Клетчатка, состоящая из остатков β-Д-глюкопиранозы.

Крахмал, состоящий из остатков α-Д-глюкопиранозы.


Гиалуроновая и хондроитинсерная кислоты, компоненты гетерополисахаридов.
Биологическая роль углеводов.
Углеводы являются основным энергетическим материалом в организме. При окислении 1 г глюкозы высвобождается 4,1 ккал. Углеводы необходимы для окисления липидов. Гликоген и крахмал являются запасным энергетическим материалом.
Рибоза входит в состав нуклеотидов РНК, АТФ, НАД, ФАД, витамина В12 и других веществ, а дезоксирибоза - в состав ДНК.
Углеводы являются источником пластического материала для биосинтеза триглицеридов, холестерина, заменимых аминокислот и других веществ.
Гетерополисахариды являются небелковой частью гликопротеинов, участвующих в многих процессах: формировании соединительной ткани, развитии иммунной реакции, свертывании крови и др.
Лекция №2
Витамины: номенклатура, классификация, биологическая роль.
План
1. Классификация витаминов.
2. Гиповитаминозы
3. Жирорастворимые витамины.
4. Водорастворимые витамины.
5. Витаминоподобные вещества.
Витамины – низкомолекулярные органические соединения, необходимые для жизнедеятельности организма, но не синтезирующиеся в нем или синтезирующиеся в недостаточных количествах и поэтому поступающие в малых количествах с пищей или от микроорганизмов, базирующихся в органах пищеварительной системы.
Еще в 1880 г. Н.И. Лунин доказал, что, кроме белков, углеводов, липидов, воды и минеральных веществ, организму необходимы дополнительные вещества. К. Функ выделил из рисовых отрубей одно из таких веществ, витамин В1, содержащий аминогруппу. Поэтому он предложил называть эти вещества витаминами (vita– жизнь). Потом оказалось, что не все витамины содержат аминогруппу.
Классификация витаминов. Из делят на 2 группы: жиро- и водорастворимые. У каждого витамина имеется 3 названия: буквенное, клиническое и химическое. Существуют еще ряд витаминоподобных веществ, не подходящих по какому-то из признаков к понятию «витамины». При отсутствии поступления витаминов развиваются авитаминозы, при сниженном поступлении – гиповитаминозы. При чрезмерном поступлении некоторых витамино (А, Д и др.) возможны гипервитаминозы.
Причины гиповитаминозов.
А. Экзогенныегиповитаминозы развиваются при:
1) отсутствии определенных продуктов питания: свежих овощей, мяса, жиров и т.д.;
2) потери витаминов при хранении, обработке продуктов, приготовлении пищи и т.д.
Б. Эндогенныегиповитаминозы развиваются при:
1) недостаточно эффективном поступлении витаминов из кишечника при воспалении его, а также из-за нарушения поступление в него желчных кислот при патологии печени и перекрытии желчевыводящих путей, приводящего к снижению гидролиза и всасывания липидов с растворенными в них витаминами;
2) гибели микроорганизмов пищеварительного тракта при кормлении высоко концентратными кормами, лечении антибиотиками и от других причин;
3) нарушении транспорта витаминов кровью при снижении содержания в ней некоторых белков;
4) нарушении превращения провитаминов в витамины при недостаточном ультрафиолетовом облучении, отсутствии ферментов, осуществляющих это превращение;
5) поступлении в организм антивитаминов.
Жирорастворимые витамины.
Витамин А (антиксерофтальмический); ретинол.

Биологическая роль витамина А:
1. Является компонентом биологических мембран, способствует биосинтезу их углевод-белковых комплексов, стабилизирует структуру клеток, особенно эпителиальных, поддерживает барьерную функцию их.
2. Обладает антиоксидантными свойствами.
3. Регулирует рост, дифференциацию тканей, развитие организма в целом, особенно организма молодняка.
4. Поддерживает функцию иммунной системы.
5. Входит в состав родопсина (зрительного пурпура) колбочек и палочек сетчатки глаза. Под действием света родопсин расщепляется на белок опсин и ретинальдегид (производное витамина А), что приводит к генерации светового импульса.
Суточная потребность(для человека) – 2,3 мг.
Продукты, богатые витамином А: рыбий жир, печень, молочные продукты, яичный желток и др. Каротин (предшественник витамина А, состоящий из двух остатков его) содержится в моркови и других коренеплодах, зеленых листьях, сочных кормах и т.д. В организме животного каротин расщепляется до витамина А каротиназой.
Проявления гиповитаминоза А:
Первые проявления его – ухудшение зрения в темноте (куриная слепота). Замедляется рост и развитие организма. Снижается иммунитет. Из-за нарушения барьерной функции эпителия поражаются слезные протоки, слеза не проходит к роговице глаза и она размягчается (ксерофтальмия). Поражается также эпителий дыхательных, мочеполовых путей, кожи и других структур, что приводит к их воспалению.
Витамины группы Д(антирахитические); кальциферолы (эргокальциферол и холекальциферол) Предшественником первого из них является эргостерин, который после облучения ультрафиолетовыми лучами превращается в эргокальциферол (витамин Д2). В коже содержится второй провитамин Д, который также после облучения ультрафиолетовыми лучами превращается в холекальциферол (витамин Д3). Обо витамина поступают в печень, где у них 25-й атом углерода подвергается гидроксилированию под действием 25-гидроксилазы, а затем – в почки. В последней под действием 1-гидроксилазы гидроксилируется еще и первый атом углерода и образуются 1,25-дигидрокальциферолы, обладающие биологической активностью. При недостаточной активности 25- и 1- гидроксилазы развивается Д-резистентный рахит.

Суточная потребность(у человека)- 10-25 мкг.
Биологическая роль витаминов Д:
1) являются компонентом Са++-связывающего белка стенки тонкого кишечника, участвующего в всасывании этого иона;
2) способствуют обратному всасыванию (реабсорбции) ионов кальция и фосфата из почечных канальцев;
3) активируют щелочную фосфатазу.
Благодаря этому, они поддерживают постоянство концентрации ионов кальция и фосфата в крови, способствуя минерализации костной ткани.
Продукты, богатые витаминами Д: рыбий жир, печень, растительные масла, молочные продукты, дрожжи, желток и др.
Проявление гиповитаминоза Д у молодняка – рахит. Из-за снижения концентрации ионов кальция и фосфата в крови нарушается снабжение ими костной ткани. Кости размягчаются (остеопороз) и под тяжестью тела искривляются конечности. С опозданием зарастают роднички, прорезываются зубы, нарушается рост и развитие организма.
Витамины группы Е (антистерильные); токоферолы. Отличаются друг от друга расположение метильных групп в бензольном цикле. Синтезирован водорастворимый аналог витаминов К викасол. Антивитамин К – дикумарин- применяют при повышенной свертываемости крови.

Биологическая роль.
1. Являются антиоксидантами (предотвращают образование перекисей в мембранных структурах клетки). Встраиваясь в мембраны клетки и ее органелл, токоферолы своей гидрофобной боковой цепью прикрывают двойные связи ненасыщенных жирных кислот фосфолипидов мембран от активных форм кислорода. При этом последние инактивируются, реагируя с хроманоловым циклом токоферола. Образовавшаяся окисленная форма витамина Е восстанавливается аскорбиновой кислотой. Образовавшийся при этом дегидроаскорбат обратно восстанавливается в аскорбат глутатионом, трипертидом состоящим из глутаминовой кислоты, цистеина и глицина. Донором ионов водорода являютя SH-группы цистеина.
2. Участвуют в окислительно-восстановительных процессах, протекающих в дыхательной цепи митохондрий, во время превращения креатина в креатинфосфат, в генах в процессе транскрипции и др.
Благодаря этим свойствам, токоферолы поддерживают структуру и функцию клеток различных органов, но особенно органов репродуктивной системы, весьма чувствительных к повреждению. Они поддерживают сперматогенез, образование яйцеклетки, способствуют ее оплодотворению, развитию беременности, ее течению. Поэтому витамины Е называют антистерильными.
Суточная потребность(у человека) - 5 мг.
Продукты, богатые витаминами Е: семена облепихи, злаков, сливочное и растительные масла, печень, мясо, капуста, сочные корма и т.д.
Проявления гиповитаминоза
У самцов развиваются дегенеративные изменения в семенниках, нарушается сперматогенез, вырабатываются сперматозоиды, не способные оплодотворить клетку. В тяжелых случаях развивается атрофия семенников с последующей деградацией половых признаков.
У самок нарушается образование яйцеклетки. Если оплодотворение ее, эмбриогенез происходят, то плод может не вынашиваться, появляются выкидыши.
Из-за нарушения окислительно-восстановительных процессов в мышечных волокнах наступает дегенерация миофибрилл. Из-за неэффективного превращения креатина в креатинфосфат он поступает из мышечных волокон в кровь (гиперкреатинемия) и появляется в моче (кретинурия). Это наблюдается при мышечнойц дистрофии у лошадей и крупного рогатого скота.
Витамины группы К(антигеморрагические): филлохинон (витамин К1) и менахинон (витамин К2). В основе структуры их цикл 1,4-нафтохинона и боковая изопреноавя цепь.

Биологическая роль
Участвуют в процессах свертывания крови, являясь коферментами энзимов, превращающих неактивные факторы свертывания крови в активные: протромбина в тромбин, проконвертина – в конвертин, фибриногена – в фибрин. В процессе активации этих факторов происходит превращение содержащейся в их составе глутаминовой кислоты в γ-карбоксиглутаминовую кислоту.
Суточная потребность(у человека) - 10-15 мг.
Продукты, богатые витаминами К:крапива, печень, капуста, коренеплоды, сочные корма и др. Образуют витамины К микроорганизмы пищеварительного тракта.
Проявления гиповитаминоза К – желудочные, кишечные, маточные и другие кровотечения.
Водорастворимые витамины
Витамин В1 (антиневритный); тиамин содержит в своем составе пиримидиновый и тиозоловый циклы. Является предшественником в биосинтезе тиаминдифосфата (ТДФ): Тиамин + АТФТиаминкиназаТДФ + АМФ.

Биологическая роль
ТДФ является одним из пяти коферментов, входящих в состав полиферментных комплексов, осуществляющий одновременное отщепление ионов водорода и углекислого газа от пировиноградной кислоты (пируватдегидрогеназа; реакция аэробного гликолиза) и α-кетоглутаровой кислоты (α-кетоглутаратдегидрогеназа; реакция цикла Кребса). ТДФ также является коферментом транскетолазы.
Суточная потребность(у человека) - 1,5- 2 мг.
Продукты, богатые витаминами В1: зерно злаков, гречихи, бобовые культуры, печень, мясо и др.
Проявления гиповитаминоза В1 :
1. Торможение пируватдегидрогеназной реакции, ведущее к накоплению в нервной ткани пировиноградной кислоты. Она повреждает нервные стволы, развивается их воспалении - полиневриты. Снижается также выработка ацетил-КоА, что приводит к дефициту энергетического и пластического материала;
2. Недостатку последнего способствует и торможение активности транскетолазы, ключевого фермента окислительной ветви пентозного цикла;
3. Возможно развитие тиамин-зависимой анемии, поскольку ТДФ участвует в кроветворении;
Витамин В2(фактор роста); рибофлавин имеет в основе своей структуры
изоаллоксаззиновый цикл. Является предшественником в биосинтезе коферментов флавинмононуклеотида (ФМН) и флавинадениндинуклеотида (ФАД).

Биологическая роль:
1. ФМН является коферментом одного из энзимов дыхательной цепи митохондрий.
2. ФАД, как и ТДФ, является одним из пяти коферментов, входящих в состав пируватдегидрогеназного и α-кетоглутаратдегидрогеназного полиферментных комплексов, осуществляющий одновременное отщепление ионов водорода и углекислого газа соответственно от пировиноградной (реакция аэробного гликолиза) и α-кетоглутаровой кислот (реакция цикла Кребса).
3. ФАД является коферментом ацил-КоА-дегидрогеназы (фермент β-окисления жирных кислот), глутатионредуктазы, восстанавливающей глутатиондисульфид, и других энзимов.
Суточная потребность(у человека) - 1,7 мг.
Продукты, богатые витамином В2: зерна злаков, яйца, печень, мясо, овощи, сочные корма и др.
Проявления гиповитаминоза В2:
1. Торможение реакций гликолиза, цикла Кребса, функции дыхательной цепи митохондрий приводит к снижению эффективности выработки АТФ, процессов биосинтеза с последующим нарушением роста и развития молодняка, снижению резистентности организма к патогенным факторам. 2. Из-за недостатка пластического материала нередко нарушается биосинтез гемоглобина, развивается малокровие.
3. Нередко развиваются васкуляризация, воспаление глазного яблока, роговой оболочки (кератит), помутнение хрусталика (катаракта).
Витамин В3 (антидерматитный); пантотеновая кислота состоит из 2,4-дигидрокси-3,3-диметилмасляной кислоты и β-аланина, соединенных между собой через пептидную связь. Является предшественником в биосинтезе коферментаHS-коэнзима А (КоА).
СН3 ОН
! !
НО - СН2 - С----СН – СО –NH - СН2 -СН2 - COOH
!
СН3
2,4-диокси-3,3-диметил- β - а л а н и н
масляная кислота
Биологическая роль
1. КоА, как и ФАД и ТДФ, является одним из пяти коферментов, входящих в состав пируватдегидрогеназного и α-кетоглутаратдегидрогеназного полиферментных комплексов, осуществляющий одновременное отщепление ионов водорода и углекислого газа соответственно от пировиноградной (реакция аэробного гликолиза) и α-кетоглутаровой кислот (реакция цикла Кребса).
2. Будучи компонентом активированных жирных и других кислот (ацил-КоА), КоА участвует в реакциях их окисления.
3. В составе ацетил-КоА и других активированных органических кислот КоА принимает участие в биосинтезе многих веществ (жирных кислот, ацилглицеролов, холестерола, стероидных гормонов, гемма и др.).
Суточная потребность(у человека) - 3-5 мг.
Продукты, богатые витамином В3: печень, дрожжи и многие другие пищевые продукты.
Проявления гиповитаминоза В3:
Воспаление кожных покровов (дерматит) и выпадение шерсти
(аллопеция);
Поражение сердца, почек, желудка, надпочечников и других
внутренних органов;
Повреждение тканей головного мозга, выражающееся в нарушении
координации движений.
Витамин В5 (РР; антипеллагрический); никотиновая кислота и никотинамид имеет в своей основе цикл пиридина. Является предшественником в биосинтезе коферментов НАД и НАДФ.
Биологическая роль
НАД и НАДФ являются коферментами более чем 50 дегидрогеназ гликолиза, β-окисления жирных кислот, окислительного дезаминирования глутамата, цикла Кребса, дыхательной цепи митохондрий, пентозного цикла и др.
Суточная потребность(у человека) - 18 мг.
Продукты, богатые витамином В2: печень, мясо, зерна злаков, картофель, корнеплоды, сочные корма, дрожжи и другие пищевые продукты.
Проявление гиповитаминоза В5– пеллагра. Признаки ее:
1) Воспаление в форме бабочки на открытых участках кожных покровов (дерматит);
2) Поражение тканей пищеварительной системы: гастрит со сниженной кислотностью, поражение кишечника, кровавый понос (диарея);
3) Повреждение нервных клеток и нарушение функции головного мозга.
Витамин В6 (антидерматитный); пиридоксин, пиридоксамин и пиридоксаль имеет в своей основе также цикл пиридина. Является предшественником в биосинтезе кофермента пиридоксальфосфат (ПФ).

Биологическая роль:
ПФ является коферментом энзимов метаболизма аминокислот: аминотрансфераз (аспартатаминотрансферазы, аланинаминотрансферазы и др.), декарбоксилаз ( глутаматдекарбоксилазы, гистидиндекарбоксилазы и др.). Велика его роль в метаболизме серосодержащих аминокислот, синтезе гемма из аминолевулиновой кислоты, пиридоксина из триптофана и др.
Суточная потребность(у человека) - 2 мг.
Продукты, богатые витамином В6: печень, зерна злаков, дрожжи и др.
Проявление гиповитаминоза В5:
1) поражение эпителиальной ткани: пеллагроподобный дерматиты, воспаление слизистых оболочек глаз, полости рта, глотки и др.;
2) нарушение функции центральной нервной системы – эпилептоподобные припадки;
3) возможно появление в моче промежуточных продуктов обмена серосодержащих аминокислот: гомоцистеина и цистатиона.
Витамин В12 (антианемический); кобаламин содержит в своем составе кобальт, соединенный с атомами азота четырех пиррольных колец, остатки рибозы, фосфорной кислоты и другие радикалы. Кобаламин является предшественником в биосинтезе двух коферментов:метилкобаламина (СНз-витамин В12) идезоксиаденозилкобаламина (дезоксиаденозил- витамин В12).

Биологическая роль витамина В12
1. Метилкобаламин является коферментом энзимов, катализирующих реакции переноса групп –СН3 и других одноуглеродных радикалов от одного вещества к другому, например от метил-тетрагидрофолиевой кислоты (СН3-ТГФК) к гомоцистеину (рекция биосинтеза метионина):
СН3-ТГФК + ГомоцистеинТетрагидроптероилглутамат- Метионин + ТГФК
метилтрансфераза
Кобаламин
2. Дезоксиаденозилкобаламин входит в состав ферментов, катализирующих реакции изомеризации. Так при метаболизме аминокислот валина, изолейцина и треонина, а также пропионовой кислоты, образовавшейся в преджелудках жвачных при расщеплении микроорганизмами клетчатки, образуется одинаковый конечный продукт- метилмалонил-КоА. Последний вступает в реакцию изомеризации, катализируемую S-метилмалонил-КоА-мутазой, коферментом которой является дезоксиаденозилкобаламин:
Метилмалонил-КоА S-метилмалонил-КоА-мутаза Сукцинил-КоА
Дезоксиаденозилкобаламин
3. Производные кобаламина способствуют биосинтезу нуклеиновых кислот, участвуя в реакциях образования дезоксирибозы, тиминовых нуклеотидов и других веществ, особенно в кроветворных органах.
Суточная потребность(у человека) - 3 мкг. У жвачных она удовлетворяется за счет деятельности микрофлоры пищеварительного тракта.
Продукты, богатые витамином В12: говяжья печень, мясо, рыба, яйца. Для того, чтоб всосаться в кишечнике, кобаламин должен вступить в комплекс с гастромукопротеином, вырабатываемым в желудке. У жвачных полностью, а у других животных - частично потребность в витамине витамин В12 удовлетворяется за счет деятельности микрофлоры пищеварительного тракта.
Проявление гиповитаминоза В12:
1. При высоко концентратном кормлении жвачных животных нарушается деятельность микрофлоры, вырабатывающей витамина В12, что приводит не только к торможению превращения метилмалонил-КоА в сукцинил-КоА с последующим развитием кетоацидоза, но и к дефициту метионина и других липотропных веществ, способствующему накоплению в печени ацилглицеролов..
2. При патологии желудка нарушается выработка гастромукопротеина, что приводит к нарушению всасывания витамина В12, последующим торможением биосинтеза нуклеиновых кислот в кроветворных органах и развитием малокровия.
3. Накопление в тканях головного мозга метилмалонил-КоА приводит к вовлечению его вместо малонил-КоА в реакции биосинтеза жирных кислот. Это приводит к образованию жирных кислот с разветвленной цепью, способствующему нарушению структуры миэлиновых оболочек нервных волокон.
Витамин Вс(антианемический); фолиевая кислота содержит в своем составе птеридиновый цикл (1), связанный с п-аминобензойной (2) и глутаминовой кислотами (3).
1 2 3

Биологическая роль:
Фолиевая кислота является предшественницей в биосинтезе коферментов трансфераз, участвующих в переносе метильной (–СН3), метиленовой (-СН2-), метенильной (-СН=), формильной (-СОН) и формиминовых групп
(-СН=NH). Данные энзимы участвуют в биосинтезе пуриновых нуклеотидов, холина, аминокислот серина, метионина, глицина и других веществ.
Суточная потребность(у человека) – 0,1 мг.
Продукты, богатые витамином В12: листья растений, дрожжи, люцерновая мука, соевый шрот, картофель и др.
Гиповитаминоз Всразвивается при дефиците фолиевой кислоты в кормах, нарушении всасывания в кишечнике при патологии его. Проявляется он в малокровии, сниженном содержание лейкоцитов в крови, нарушении роста, развития, снижении продуктивности животного. В тяжелых случаях возможны паралич шеи и конечностей.
Витамин С (антицинготный); аскорбиновая кислота.Является витамином лишь для человека, африканских обезьян и морских свинок. У других животных способна синтезироваться, но ее может недоставать при патологических состояниях. Структурно аскорбиновая кислота представляет собой производное спирта сорбита - лактон 2,3-диенол-гулоновой кислоты.
отдает два иона водорода, связанные со вторым и третьим углеродными атомами, превращаясь в дегидроаскорбат.
Биологическая роль:аскорбиновой кислоты
1. Является антиоксидантом. В водной фазе клеток взаимодействует с активными кислородными метаболитами, инактивируя их. В липидной фазе клеток восстанавливает глутатиондисульфид, образовавшийся в реакции восстановления токоферилхинона глутатионом или при взаимодействии последнего с активными кислородными метаболитами.
2. Поддерживает функцию дыхательной цепи митохондрий, передавая ионы водорода цитохромам или молекуле кислорода.
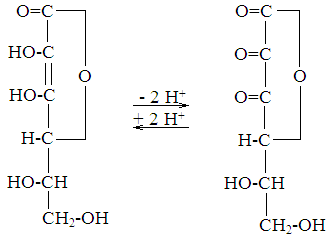
Аскорбиновая Дегидроаскорбино-
кислота ваяя кислота
3. Способствует созреванию соединительной ткани, участвуя в реакциях гидроксилирования пролина в оксипролин и лизина в оксилизин.
4. Участвует в других реакциях гидроксилирования, сопряженных с катаболизмом тирозина до тироксина, меланина, дофамина, норадреналина и адреналина, биосинтезом гликопротеинов межклеточного вещества соединительной ткани, стероидных гормонов, желчных кислот и других веществ.
Суточная потребность(у человека) – 100 мг.
Продукты, богатые витамином В12: фрукты, ягоды, свежие овощи, шиповник и др.
Проявление недостатка аскорбиновой кислоты в организме
Из-за нарушения биосинтеза межклеточного вещества соединительной
ткани изменяется структура базальной мембраны кровеносных сосудов, что приводит к повышенной кровоточивости, появлению множественных точечных кровоизлияний (петехий).
Нарушение синтеза органического матрикса костной ткани приводит к
ее хрупкости, частым переломам, ослаблению структуры альвеол челюстей, выпадению из них зубов.
3. Торможение функции антиоксидантной системы приводит к сниженной сопротивляемости организма к патогенным факторам, уменьшению продуктивности животных, сокращению времени их эксплуатации.
Витамин Р(капилляроукрепляющий); биофлавоноиды (флавонол, рутин, кверцетин, эриодиктин, гесперидин и др.) - группа веществ, построенных на основе дифенилпропанового цикла хромона или флавана.

Биологическая роль:
1. В состав межклеточного вещества соединительной ткани входит гетерополисахарид гиалуроновая кислота. Рутин ингибирует гиалуронидазу, ее расщепляющую, стабилизируя структуры, построенные из соединительной ткани.
2. Вместе с аскорбиновой кислотой, с которой тесно функционально связан, рутин регулирует окислительно-восстановительные процессы, является антиоксидантом.
Продукты, богатые витамином Р:свежие овощи, фрукты, чай.
Проявление гиповитаминоза Р:
1) повышение проницаемости кровеносных сосудов, кровоизлияния в ткани, кровотечения;
2) Снижение резистентности организма к патогенным факторам, общая слабость, боль в конечностях.
Витаминоподобные вещества также необходимы для жизнедеятельности организма, но не соответствуют по какому-то из признаков понятию «витамины».
Холинпо своей структуре является аминоэтиловым спиртом, содержащим у атома азота три метильные группы: НО-СН2 -СН2–N≡(CH3)3
+
Биологическая роль холина.
1. Входит в состав фосфатидилхолина (лецитина), компонента мембранных структур клетки. Участвуя в биосинтезе этого фосфоглицерида, холин способствует выходу из печени ацилглицеролов, предотвращая жировую инфильтрацию этого органа.
2. В качестве донора метильных групп участвует в биосинтезе метионина, адреналина, креатина, и других веществ.
3. Входит в состав ацетилхолина, передающего импульс от нервной клетки.
Источники холина в клетках.
Частично животные получают холин с животной и растительной пищей, а частично - за счет эндогенного синтеза: декарбоксилированием аминокислоты серин с последующим метилированием образовавшегося этаноламина. Донорами метильных групп могут быть метионие, фолиевая кислота и витамин В12.
Проявление недостатка холина в организме:жировая инфильтрация печени, геморрагическая дистрофия почек, нарушение свертывания крови вследствие недостаточно эффективного синтеза акцелерина и др.
Инозитол(инозит) является по своей структуре циклическим шестичленным спиртом.

Биологическая роль:
1. Является компонентом фосфоглицерида фосфатидилинозитола.. От последнего в результате реакции, катализируемой фосфолипазой Д, отщепляется инозитол-1,4,5-трифосфат, являющийся вторичным посредником при воздействие на клетки инсулина, паратгормона, тиреокальцитонина и других биологически активных веществ;
2. Обладает липотропным эффектом, предотвращает жировую инфильтрацию печени;
3. регулирует перестальтику кишечника, осмотическое давление в сперматозоидах, окисление жирных кислот, активность амилазы и др.
Продукты, богатые инозитолом:зародыши пшеницы, апельсины, зеленый горошек. Много его и в продуктах животного происхождения: печени, мясе, молоке.
Проявление недостатка инозитола наиболее выражено у мышей и крыс. Оно выражается в остановке роста и развития, жировой инфильтрации печени с отложением в нее холестерина.
Коэнзим Q(убихинон) похимической структуре представляет собой 2,3-диметокси-5-метил-1,4-бензохинон с изопреновой цепью в шестом положении.

Биологическая роль убихинона: является обязательным компонентом дыхательной цепи митохондрий, осуществляя перенос электронов от мембранных дегидрогеназ на цитохромы.
Источники убихинона в клетках.
Организм животного получает это вещество с различными кормами, а частично – в результате эндогенного биосинтеза из мевалоновой кислоты и продуктов метаболизма фенилаланина и тирозина.
Проявление недостатка убихинона в организме. Это состояние развивается при поступлении в организм недостаточного количества пищи, богатой белками. Это приводит к развитию анемии, не поддающейся лечению обычными средствами, но поддающейся лечению убихиноном. Недостаток последнего может привести и к мышечной дистрофии и сердечно-сосудистой недостаточности.
Витамин Н(антидерматитный); биотин.
Молекула его состоит из имидазольного и тиофенового циклов. К последнему присоединяется остаток валерьяновой кислоты.
О
||
C
/ \
HNNH
| |
HC------ CH
| |
H2C CH - (CH2)4 – COOH
\ /
S
Биотин
Биологическая рольбиотина:
Из этого вещества путем связывания его с ε-аминогруппой аминокислоты лизинобразуется коферментная форма витамина Н. Последняя входит в состав карбоксилаз, катализирующих две группы реакций: а) протекающих с участием АТФ (ацетил-КоА-, пропионил-КоА- и пируваткарбоксилаза); б) протекающих без участия АТФ (метилмалонил-КоА-карбоксилаза и др.). Поэтому биотин принимает активное участие в биосинтезе жирных кислот, пуриновых нуклеотидов и других веществ.
Суточная потребность(у человека) – 0,25 мг.
Источники биотина в клетках: растительные (картофель, бобовые растения, шпинат, томаты и др.) и животные продукты (печень, почки, желток яйца, молоко и др.). У животных биотин способен вырабатываться микрофлорой пищеварительного тракта.
Проявление недостатка биотина в организме:сниженный аппетит сонливость, малокровие, боли в мышцах, дерматиты, сопровождающиеся усиленной функцией сальных желез, выпадение шерсти и др.
Липоевая кислота; 1,2-дитиолан-3-валериановая кислота. Существует в окисленной (-S-S-) и восстановленной (-SH) формах, что позволяет ей выполнять коферментную функцию.
СН2
/ \
H2 CCH– (СН2)4- СООН
! !
S-------S
Липоевая кислота
Биологическая роль липоевой кислоты: входит в состав мультиферментных комплексов, осуществляющих одновременное отщепление ионов водорода и углекислого газа (окислительное декарбоксилирование) от пировиноградной и α-кетоглутаровой кислот.
Проявление недостатка липоевой кислоты в организме – «пирувизм», проявляющийся в повышенной концентрации пировиноградной и других кетокислот в крови, метаболическом ацидозе, мышечных спазмах, а в тяжелых случаях – в полиневрите.
Витамин U(противоязвенный фактор); метилметионин
NH2СН3
| |
HOOC- CH - CH2 - CH2 - S+
|
СН3
Биологическая рольметилметионина:
1) обладает положительным эффектом при язвах желудка и кишечника, стимулируя регенерацию эпителия этих органов;
2) метилируя биогенный амин гистамин в метилгистамин, способствует выведению его из организма;
3) как и метионин, является донором метильных групп при биосинтезе холина, креатина и других веществ;
4) способствует удалению из организма избытка холестерина.
Продукты, богатые метилметионином: свежая капуста, зелень петрушки и репы, зеленый чай, бананы, помидоры и др.
Проявление недостатка метилметионина в организме – развитие язв желудка и тонкого кишечника.
Витамин В15(пангамовая кислота) является эфиромглюконовой кислотыи диметилглицина:СООН
!
(Н-С-ОН)4 CH3
!!
СН2-О-СО- СН2-N
!
CH3
Биологическая роль пангамовая кислоты:
1) участвует в биосинтезе холина, метионина и креатина в качестве источника метильных групп и поэтому обладает липотропными свойствами.;
2) принимает участие в процессах тканевого дыхания, биосинтеза белка, в функционировании надпочесников.
Продукты, богатые пангамовой кислотой: семена растений, дрожжи, печень и др.
Проявление недостатка пангамовой кислоты:
1) жировая инфильтрация печени;
2) кислородное голодание.
п-Аминобензойная кислота необходима для жизнедеятельности микроорганизмов и животных.

Биологическая роль п-аминобензойной кислоты:
1) входя в состав витамина фолиевой кислоты, принимает участие в реакциях, в которых участвует синтезирующийся из нее кофермент тетрагидрофолиевая кислота: синтез нуклеиновых кислот и др.
2) участвуя в биосинтезе из тирозина пигмента меланин, способствует пигментации кожи, шерсти, перьев и др.
Продукты, богатые п-аминобензойной кислотой: зародыши пшеницы, картофель, дрожжи, мясо, печень, почки животных и др.
В медицине и ветеринарии применяются аналоги п-аминобензойной кислоты сульфаниламиды. Последние вследствие структурного сходства конкурентно замещают п-аминобензойную кислоту в ферментах микроорганизмов с последущей остановкой из размножения.
Витамин F; ненасыщенные жирные кислоты. Свойствами витаминаFобладают олеиновая (С17 Н33–СООН), линолевая (С17 Н31–СООН), линоленовая (С17 Н29–СООН) и арахидоновая (С19 Н31-СООН) кислоты.
Биологическая роль ненасыщенных жирных кислот:
1) входят в состав фосфолипидов биологических мембран клеток. Поэтому необходимы для образования и репарации клеток, особенно клеток репродуктивных органов, кожи и эндотелия кровеносных сосудов. 2) из ненасыщенных жирных кислот синтезируются простогландины, тромбоксаны, лейкотриены и другие сигнальные молекулы.
Продукты, богатые витамином F: олеиновая, линолевая и линоленовая кислоты содержатся в составе растительных и в меньшей степени – животных жиров. Арахидоновая кислот содержится только в составе животных жиров.
При дефицитененасыщенных жирных кислотнарушается функция репродуктивных органов, развиваются заболевания кожи, увеличение концентрации холестерина в крови, склероз кровеносных сосудов.
Лекция № 2
