
Лабы ОБХ
.pdfМинистерство образования и науки РФ
Уральский Федеральный Университет имени первого президента России Б.Н. Ельцина
ОБЩАЯ ХИМИЯ: ПРАКТИКУМ
Учебно-методическое пособие для студентов 1 курса департамента Химии Института естественных наук
направление 020100 «Химия»
Екатеринбург
2013
1
Подготовлено кафедрой неорганической химии
Составители:
А.Ф. Гусева, С.С. Нохрин,
И.Н. Атманских, Н.А. Кочетова,
Л.И. Балдина, И.Е. Анимица
2
ПРЕДИСЛОВИЕ
Настоящее учебно-методическое пособие предназначено студентам первого года обучения департамента «Химический факультет» для проведения лабора-
торно-практических занятий по курсу «Общая химия». Целью пособия является формирование у студентов навыков научно-исследовательской деятельности в ходе экспериментального раскрытия теоретических положений общей химии.
Для того чтобы студенты могли успешно овладеть основными способами организации самостоятельной работы, в первом разделе «Этапы проведения эксперимента» предлагается схема последовательности действий, которой сле-
дует руководствоваться при подготовке к лабораторно-практическим занятиям,
их проведении и оформлении отчета. Кроме того, в последующих разделах при-
водится краткое описание техники проведения химического эксперимента, а
также перечень основных правил безопасности при работе в лаборатории.
По каждой теме лабораторных занятий сформулированы задания, которые студенты должны выполнить. При этом использована методика, которая пред-
полагает постепенное уменьшение числа задаваемых ориентиров и их конкрет-
ности. Так, в работах по атомно-молекулярному учению (работы 1-3) после формулировки каждого задания в пункте «Теоретическое исследование зада-
ния» поставлены направляющие вопросы в соответствии с общей схемой дея-
тельности, на которые необходимо ответить на этапе предварительной подго-
товки, используя учебную литературу, лекции, дополнительные источники. В
последующих работах (работы 4-10) конкретные вопросы к заданиям не сфор-
мулированы, краткий перечень теоретических аспектов, которые необходимо освоить студентам для выполнения заданий, вынесен в общий пункт «Теорети-
ческие основы: законы, понятия, определения».
После описания лабораторных работ приведены задачи по соответствующим темам, составленные таким образом, чтобы их решение способствовало осмыс-
ленности выполнения эксперимента в лаборатории. Кроме того, в пособие
3
включены примеры тестовых заданий, которые аналогичны тем, что предлага-
ются студентам на занятии для оценки степени их готовности к работе.
В приложениях к настоящему пособию содержится справочная информация,
которая необходима студентам для выполнения ряда работ: таблицы со значе-
ниями плотностей и концентраций растворов кислот и даграммы Латимера.
Раздел «Этапы проведения эксперимента» и тестовые задания ко всем лабо-
раторным работам подготовлены доцентом Балдиной Л.И. Раздел «Химические реактивы, посуда. Техника лабораторных работ» подготовлен старшим препо-
давателем Атманских И.Н. Лабораторные работы 1–3 подготовлены доцентом Гусевой А.Ф. Лабораторные работы 4, 5 , разделы «Техника безопасности и правила выполнения лабораторных работ» и «Приложения» подготовлены до-
центом Нохриным С.С. Лабораторные работы 6–8 подготовлены доцентом Ко-
четовой Н.А. Лабораторные работы 9, 10 подготовлены доцентом Анимицей И.Е.
4
ЭТАПЫ ПРОВЕДЕНИЯ ЭКСПЕРИМЕНТА
1. Теоретический этап
1.1.Сформулировать цель работы.
1.2.Продумать, какие понятия, законы, правила, гипотезы необходимо ис-
пользовать для достижения поставленной цели. В учебной литературе, лекциях найти ответы на эти вопросы.
1.3. На основании проведенного теоретического анализа (п. 1.1, 1.2) сплани-
ровать выполнение эксперимента. Определить:
а) какие реакции нужно осуществить;
б) какие физические величины при этом нужно измерить;
в) какие реактивы, посуду, оборудование необходимо использовать, какую установку (прибор) следует собрать (зарисовать схему);
г) в какой последовательности будут выполнены все необходимые действия;
какие меры предосторожности следует соблюдать;
д) в какой форме производить запись наблюдений, измерений (предпочти-
тельно это делать в виде таблицы).
Теоретический этап необходимо оформить письменно.
2. Экспериментальный этап
2.1.Отобрать необходимые для выполнения работы реактивы, оборудование
ипосуду.
2.2.Собрать прибор или установку.
2.3.Провести опыт, тщательно наблюдая за всеми происходящими явления-
ми и измеряя необходимые физические величины. Сделать записи в лаборатор-
ном журнале в соответствии с продуманной ранее формой.
3. Обработка экспериментальных данных
5
3.1. Логически объяснить наблюдаемые явления, составить уравнения хими-
ческих реакций в разных формах (молекулярной, ионной, термохимической) в
соответствии с целью работы.
3.2. Если эксперимент количественный, необходимо выполнить соответст-
вующие вычисления с той же точностью, которая достигается в измерениях. 3.3. Обосновать с помощью математических расчетов (вычисление измене-
ния изобарно-изотермического потенциала; константы равновесия реакции;
ЭДС, генерируемой реакцией) направление протекания изученных реакций,
учитывая условия проведения опыта.
3.4. Построить графики полученных экспериментальных зависимостей. На координатных осях указываются переменные величины и единицы, в которых они измеряются. По оси абсцисс (ось x) откладывают независимую перемен-
ную, т.е. величину, задаваемую самим экспериментатором, а по оси ординат
(ось y) − определяемую величину. Масштабы на координатных осях следует выбирать так, чтобы экспериментальные точки не сливались друг с другом и по возможности располагались по диагонали графика, а координаты любой точки на графике определялись легко и быстро без ненужных расчетов.
6
ХИМИЧЕСКИЕ РЕАКТИВЫ, ПОСУДА ТЕХНИКА ЛАБОРАТОРНЫХ РАБОТ
Химическая посуда
Вся посуда по назначению делится на несколько групп:
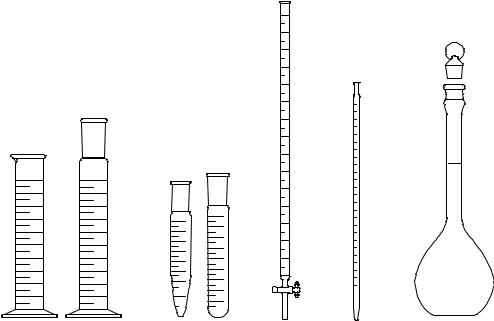
−мерная посуда, рис. 1;
−посуда общего пользования (используется для выполнения нескольких химических операций), рис. 2;
−посуда из фарфора и других материалов, рис. 3.
−посуда специального назначения (например, для получения и очистки га-
зов, см. лабораторную работу №2, рис.4);
1 |
2 |
3 |
4 |
5 |
Рис. 1. Мерная посуда: 1 – мерные цилиндры; 2 – мерные пробирки; 3 – бюретка; 4 – градуированная пипетка; 5 – мерная колба.
7
1 |
2 |
3 |
4 |
|
|
|
|
4 |
5 |
6 |
7 |
8 |
9 |
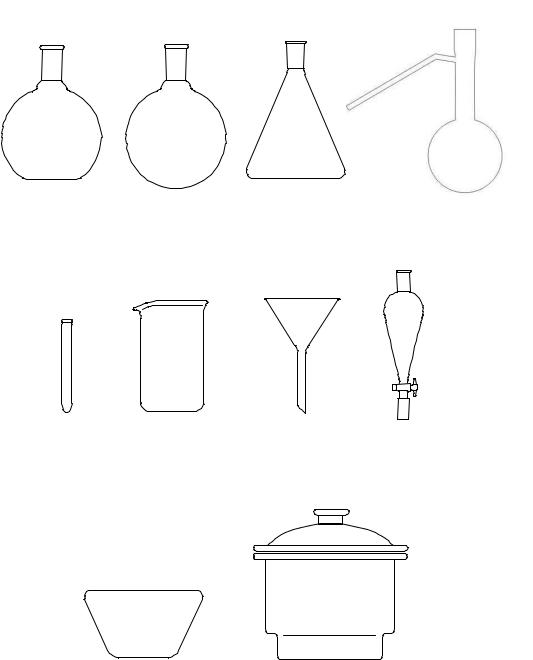
Рис. 2. Посуда общего назначения: 1 – плоскодонная колба; 2 – круглодонная колба; 3 – коническая колба (колба Эйренмейера); 4 – колба Вюрца; 4 – пробирка; 5 – стакан; 6 – воронка; 7 – капельная воронка; 8 – кристаллизатор; 9 – эксикатор.
8
1 |
2 |
3 |
4 |
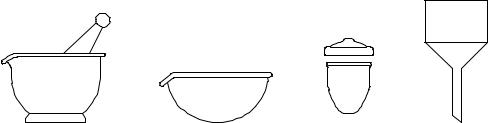
Рис. 3. Фарфоровая посуда: 1 – |
ступка; 2 – |
чашка выпарительная; 3 – тигель; 4 – |
|
воронка Бюхнера. |
|
|
|
Химические реактивы, их хранение
Реактивы – это индивидуальные вещества, их растворы или смеси строго регламентированного состава, предназначенные для лабораторных работ, науч-
ных исследований и химического анализа.
Химические реактивы могут использоваться в твердом, жидком и газообраз-
ном состояниях (в виде паров). Их принято разделять по степени чистоты на не-
сколько квалификаций, характеристики которых приведены в таблице.
|
|
|
Таблица 1 |
|
Классификация химических реактивов |
||||
|
|
|
|
|
Квалификация |
Символ |
Содержание основ- |
Содержание отдель- |
|
реактива |
|
ного вещества, |
ных примесей, масс.% |
|
|
|
масс.% |
|
|
|
|
|
|
|
Чистый |
ч |
не менее 98 |
0,01 – 0,5 |
|
|
|
|
|
|
Чистый для анализа |
чда |
не менее 99 |
до 0,1 |
|
|
|
|
|
|
Химически чистый |
хч |
выше 99 |
10-3 – 10 -5 |
|
|
|
|
|
|
Особо чистый |
осч |
близко к 100 |
10-5 – 10 -10 |
|
|
|
|
|
|
Твердые реактивы хранят в стеклянных и полиэтиленовых банках, а жидкие
– в склянках.
9
В зависимости от свойств веществ банки и склянки закрывают стеклянными,
полиэтиленовыми, резиновыми и корковыми пробками.
Гигроскопичные вещества хранят в бюксах, эксикаторах, запаянных ампу-
лах, склянках с хлоркальциевыми трубками и банках с притертыми пробками.
Пробки банок можно заливать парафином. Реактивы, изменяющиеся под дейст-
вием света, хранят только в темных склянках.
Газы в больших количествах хранят в баллонах, в небольших количествах – в газовых бюретках и газометрах.
Правила работы с реактивами
1.Оберегать реактивы от загрязнения. Не сливать излишки растворов и не ссыпать твердые вещества обратно в сосуд, из которого они взяты. Не путать пробки разных склянок! После употребления реактива склянку тотчас закрыть пробкой и поставить на место.
2.На всех склянках с реактивами всегда должны быть этикетки с названием вещества или химической формулой и указанием его качества. Для растворов должна быть указана концентрация.
3.Реактивы брать в возможно малых количествах.
4.Твердые вещества брать при помощи стеклянных, фарфоровых, пластмас-
совых шпателей, лопаточек, а жидкие – с помощью пипетки.
5. При отборе реактива склянку брать этикеткой в ладонь и последнюю кап-
лю снимать о край сосуда, в который отливают.
Весы и взвешивание
Обычно в химических лабораториях применяют технохимические, аптеч-
ные, электронные технические и аналитические весы.
Технохимические, аптечные и электронные технические весы позволяют определить массу с точностью до 0,01 г, а аналитические − до 0,0001 г. К весам прилагается комплект гирь, называемый разновесом. Гири из разновеса берут пинцетом.
10
