
- •Оформление лабораторных работ по дисциплине «химия»
- •Часть 1
- •Содержание
- •Введение
- •Список литературы для проведения лабораторных работ по дисциплине «химия»
- •Бально-рейтинговая система оценки знаний студентов по дисциплине «химия»
- •Инструкция по технике безопасности при работе студентов в лаборатории химии
- •На тему: «Важнейшие классы неорганических соединений (оксиды, гидроксиды, соли)»
- •Теоретическая часть Сложные неорганические соединения делятся на следующие классы: __________________
- •Экспериментальная часть
- •На тему: «Определение молекулярной массы эквивалента карбоната кальция»
- •Теоретическая часть
- •Экспериментальная часть
- •На тему: «Химическая кинетика. Катализ»
- •Теоретическая часть
- •Экспериментальная часть
- •На тему: «Химическое равновесие»
- •Теоретическая часть
- •Экспериментальная часть
- •На тему: «Электролитическая диссоциация»
- •Теоретическая часть
- •Экспериментальная часть
- •На тему: «Приготовление водных растворов»
- •Теоретическая часть
- •Экспериментальная часть
- •На тему: «Ионообменные реакции»
- •Теоретическая часть
- •Экспериментальная часть
- •На тему: «Ионное произведение воды. Водородный показатель. Гидролиз солей»
- •Теоретическая часть
- •Экспериментальная часть
- •На тему: «Дисперсные системы»
- •Теоретическая часть
- •Экспериментальная часть
- •На тему: «Окислительно-восстановительные реакции»
- •Теоретическая часть
- •Экспериментальная часть Реакции межмолекулярного окисления-восстановления
- •Реакции диспропорционирования
- •Реакции внутримолекулярного окисления-восстановления
- •Двойственное поведение пероксида водорода в овр
- •На тему: «Ряд напряжений металлов. Гальванические элементы. Электролиз»
- •Теоретическая часть
- •Экспериментальная часть
- •На тему: «Коррозия металлов и методы защиты»
- •Теоретическая часть
- •Экспериментальная часть
- •На тему: «Комплексные соединения»
- •Теоретическая часть
- •Экспериментальная часть
Экспериментальная часть
Опыт 1. Зависимость скорости гомогенной реакции от концентрации исходных реагентов
Напишите уравнение реакции:
_____________________________________________________________________________________
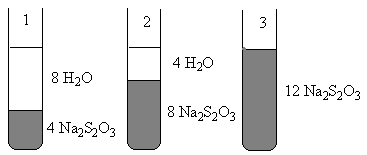
Условная молярная концентрация тиосульфата натрия в пробирке № 1 – «с», № 2 – «2с», № 3 – «3с».
Напишите выражение скорости для данной реакции по закону действующих масс:
V = __________________________
Занесите полученные результаты в таблицу:
|
№ пробирки |
Объем, мл |
Относи-тельная концен-трация |
Время появления помутнения t, с |
Относительная скорость реакции | |||
|
|
|
|
общий объем раствора |
| |||
|
1 |
1 |
4 |
8 |
|
1с |
|
|
|
2 |
1 |
8 |
4 |
|
2с |
|
|
|
3 |
1 |
12 |
0 |
|
3с |
|
|
Начертите график зависимости скорости химической реакции от концентрации реагирующих веществ.
Рисунок – Зависимость скорости химической реакции
от концентрации реагирующих веществ
Вывод (какой линией выражается найденная зависимость скорости реакции от концентрации реагирующих веществ, должна ли проходить линия через начало координат, почему?): ________________________________
___________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________.
Опыт 2. Влияние поверхности реагирующих веществ на скорость реакции в гетерогенной системе
Напишите уравнение реакции:
__________________________________________________________________________________
Запишите математическое выражение закона действующих масс:
_________________________________________________________________________________
Запишите время протекания реакции:
1. (порошок)_________________________________________________________________________
2. (кусок) ____________________________________________________________________________
Рассчитайте
относительную скорость в обоих случаях(![]() )
)
1. __________________________________________________________________________________
2. _________________________________________________________________________________
Вывод: (как влияет поверхность реагирующих веществ на скорость реакции) _____________________ ________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________.
Опыт 3. Качественное определение активности различных катализаторов на примере разложения пероксида водорода
Запишите наблюдения в обоих случаях:
1. ___________________________________________________________________________________ 2. __________________________________________________________________________________.
Запишите уравнения реакций с различными катализаторами:
1. __________________________________________________________________________________
2. __________________________________________________________________________________.
Вывод: (как определили скорость разложения пероксида водорода; какой из катализаторов эффективнее; как доказали, что в обеих пробирках выделяется кислород): __________________________________________________
___________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________.
Опыт 4. Автокатализ
Запишите наблюдения реакции с катализатором и без участия катализатора и отметьте время протекания реакции в каждом случае:
1. ___________________________________________________________________________________
2. ___________________________________________________________________________________
Запишите уравнения реакций:
1. ___________________________________________________________________________________
2. ___________________________________________________________________________________
Рассчитайте
относительную скорость в обоих случаях
(![]() )
)
1. ___________________________________________________________________________________
2. ___________________________________________________________________________________
Вывод: (в каком случае реакция протекает быстрее и почему) ______________________________________
___________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________.
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РФ
ФГБОУ ВПО «Уфимский государственный нефтяной технический университет»
Кафедра «Прикладная химия и физика»
Дисциплина «Химия»
ОТЧЕТ
по лабораторной работе № ___
