
2. Растворимость
Растворимостью называется способность вещества растворяться в том или ином растворителе. Мерой растворимости вещества при данных условиях служит содержание в насыщенном растворе. Потому численно растворимость может быть выражена теми же способами, что и состав, например, процентным отношением массы растворенного вещества к массе насыщенного раствора или количеством растворенного вещества, содержащимся в 1 литре насыщенного раствора. Часто растворимость выражают также числом единиц массы безводного вещества, насыщающего при данных условиях 100 единиц массы раствора. Иногда выраженную этим способом растворимость называют коэффициентом растворимости. Если в 100 г воды растворяется более 100 г вещества, то такое вещество принято называть хорошо растворимым. А если растворяется менее 1 г вещества – малорастворимым. И, наконец, практически нерастворимым, если в раствор переходит менее 0,01 г вещества.
Принципы, позволяющие предсказать растворимость веществ, пока неизвестны. Однако обычно вещества, состоящие из полярных молекул, и вещества с ионным типом связи лучше растворяются в полярных растворителях (вода, спирты, жидкий аммиак). И наоборот.
Растворение большинства твёрдых тел сопровождается поглощением теплоты. Это объясняется затратой значительного количества энергии на разрушение кристаллической решётки твёрдого тела, что обычно не полностью компенсируется энергией, выделяющейся при образовании гидратов (сольватов). Прилагая принцип Ле Шателье к равновесию между веществом в кристаллическом состоянии и его насыщенным раствором
К
 ристалл
+ Растворитель Насыщенный
раствор
ристалл
+ Растворитель Насыщенный
раствор![]() Q,
Q,
приходим к выводу, что в тех случаях, когда вещество растворяется с поглощением энергии, повышение температуры должно приводить к увеличению его растворимости. Если же, однако, энергия гидратации (сольватации) достаточно велика, чтобы образование раствора сопровождалось выделением энергии, растворимость с ростом температуры понижается. Это происходит, например, при растворении в воде щелочей, многих солей лития, магния, алюминия.
Зависимость между растворимостью и температурой очень удобно изображать графически – в виде кривых растворимости. При построении кривой растворимости откладывают на горизонтальной оси температуру, а на вертикальной – растворимость вещества при соответствующей температуре. На рис. 1 приведено несколько характерных кривых растворимости.
К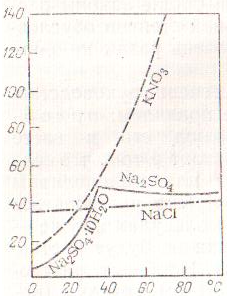 ак
видно из рис. 1, растворимость
ак
видно из рис. 1, растворимость![]() увеличивается при повышении температуры
очень медленно, а
увеличивается при повышении температуры
очень медленно, а![]() -
очень быстро.
-
очень быстро.
Более
сложный вид имеет кривая растворимости
сульфата натрия. При 32,4
![]() С
кристаллогидрат его распадается и
переходит в безводную соль. Этому и
соответствует излом кривой растворимости,
которая, в сущности говоря, состоит из
двух отдельных кривых: до 32,4
С
кристаллогидрат его распадается и
переходит в безводную соль. Этому и
соответствует излом кривой растворимости,
которая, в сущности говоря, состоит из
двух отдельных кривых: до 32,4![]() С
насыщенный раствор находится в равновесии
с осадком, состоящим из
С
насыщенный раствор находится в равновесии
с осадком, состоящим из![]() ,
выше этой температуры -
,
выше этой температуры -
Рис.1.
Кривые растворимости (г/100г
![]() )
)
с
безводным
![]() .
Резкое изменение хода кривой показывает,
что растворимость обоих веществ
существенно различна. То же наблюдается
и для кристаллогидратов с различным
содержанием воды: каждый из них имеет
свою характерную для него растворимость.
.
Резкое изменение хода кривой показывает,
что растворимость обоих веществ
существенно различна. То же наблюдается
и для кристаллогидратов с различным
содержанием воды: каждый из них имеет
свою характерную для него растворимость.
При растворении твердых тел в воде объем системы обычно изменяется незначительно. Поэтому растворимость веществ, находящихся в твердом состоянии, практически не зависит от деления.
Жидкости также могут растворяться в жидкостях. Некоторые из них неограниченно растворимы одна в другой, т.е. смешиваются друг с другом в любых пропорциях, как, например, спирт и вода, другие – взаимно растворяются лишь до известного предела. Т.е. если взболтать диэтиловый эфир с водой, то образуются 2 слоя: верхний представляет собой насыщенный раствор воды в эфире, а нижний – насыщенный раствор эфира в воде. В большинстве подобных случаев с повышением температуры взаимная растворимость жидкостей увеличивается до тех пор, пока не будет достигнута температура, при которой обе жидкости смешиваются в любых пропорциях.
Растворение газов в воде представляет собой экзотермический процесс. Поэтому растворимость газов с повышением температуры уменьшается. Если оставить в теплом помещении стакан с холодной водой, то внутренние стенки его покрываются пузырьками. Это воздух, который был растворен в воде. Он выделяется из нее вследствие нагревания. Кипячением можно удалить из воды весь растворенный в ней воздух.
Однако растворение газов в органических жидкостях нередко сопровождается поглощением теплоты; в подобных случаях с ростом температуры растворимость газа увеличивается.
При растворении газа в жидкости устанавливается равновесие:
Г
 аз
+ Жидкость Насыщенный раствор
газа в жидкости
аз
+ Жидкость Насыщенный раствор
газа в жидкости
При этом объем системы существенно уменьшается. Следовательно, повышение давления должно приводить к смещению равновесия вправо, т.е. к увеличению растворимости газа.
