
3. Способы выражения содержания растворенного вещества в растворе
Содержание растворенного вещества в растворе может быть выражено либо безразмерными единицами – долями или процентами, либо величинами размерными – концентрациями. Ниже приведены наиболее часто употребляемые в химии способы выражения содержания растворенного вещества в растворе:
|
Способ выражения содержания растворенного вещества в растворе |
Определение |
|
Массовая доля (С)
Мольная
доля (
Молярная концентрация или молярность
(
Моляльная концентрация или моляльность (m)
Эквивалентная
концентрация или нормальность ( |
Процентное отношение массы растворенного вещества к общей массе раствора; например, С=9,25% (масс)
Отношение
количества растворенного вещества
(или растворителя) к сумме количеств
всех веществ, находящихся в растворе.
Например, в системе, состоящей из
растворителя и единственного
растворенного вещества, мольная доля
последнего (
а мольная доля растворителя
(
где
Отношение количества растворенного вещества к объему раствора; например,
1,5
М раствор или
Отношение количества растворенного вещества к массе растворителя: например,
m=1,5
моль/кг (
Отношение
числа эквивалентов растворенного
вещества к объему раствора; например,
0,75 н. раствор или
Эквивалентные массы сложных веществ вычисляются по формулам: Эоксида=Моксида/Число атомов элемента∙валентность эл-та Экислоты=Мкислоты/ Основность кислоты Эоснования=Моснования/ Кислотность основания Эсоли=Мсоли/Число атомов металла∙валентность металла
|
4. Индивидуальные задания
Вариант 1
Найти массовую долю глюкозы в растворе, содержащем 280 г воды и 40 г глюкозы.
В каком объеме 1 М раствора и в каком объеме 1 н. раствора содержится 114 г
 ?
?В 1 кг воды растворено 666 г
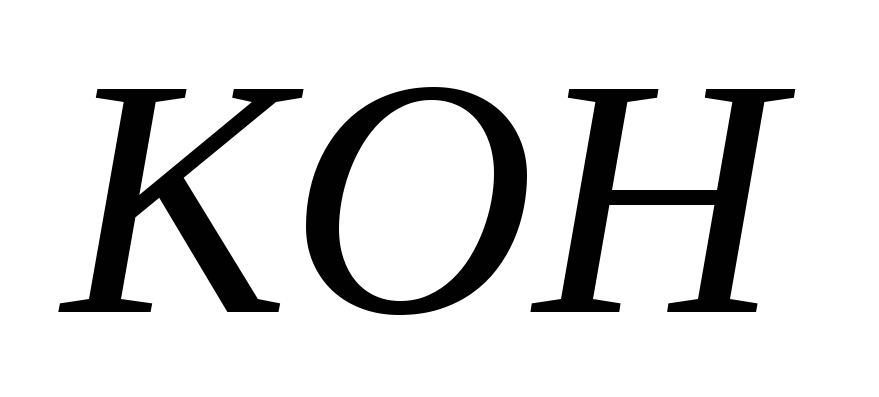 ;
плотность раствора равна
;
плотность раствора равна
1,395
г/мл. Найти: а) массовую долю
![]() ;
б) молярность;
;
б) молярность;
в) моляльность; г) мольные доли щелочи и воды.
Вариант 2
Сколько граммов
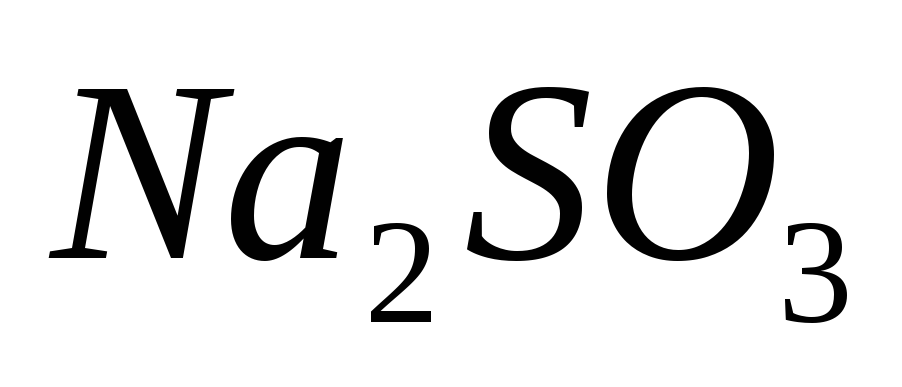 потребуется
для приготовления 5 л 8%-ного (по массе)
раствора (
потребуется
для приготовления 5 л 8%-ного (по массе)
раствора (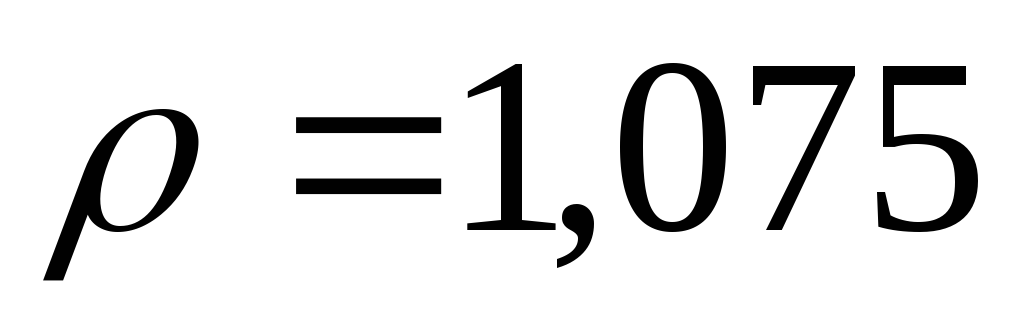 г/мл)?
г/мл)?Из 400 г 50%-ного (по массе) раствора
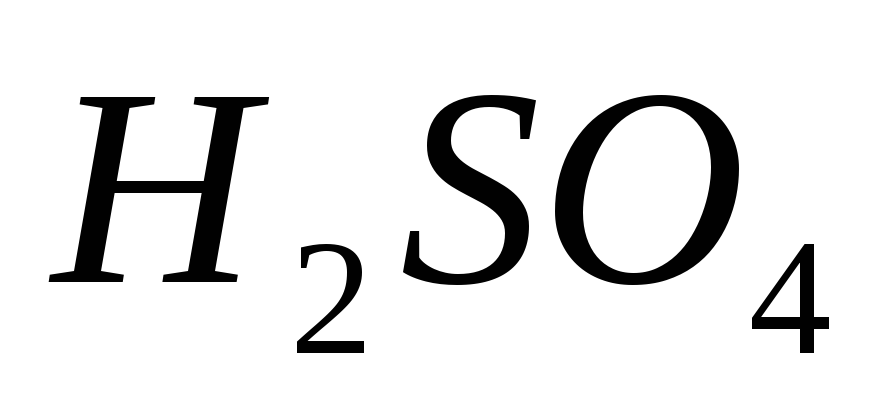 выпариванием удалили 100 г воды. Чему
равна массовая доля
выпариванием удалили 100 г воды. Чему
равна массовая доля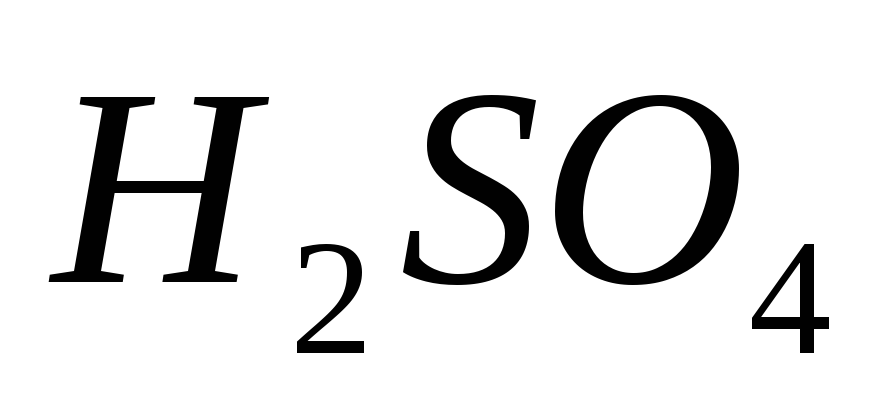 в оставшемся растворе
?
в оставшемся растворе
?В 1 кг воды растворено 250 г NaCl; плотность раствора равна 1,152 г/мл. Найти: а) массовую долю NaCl; б) молярность;
в) моляльность; г) мольные доли соли и воды.
Вариант 3
При 25
 С растворимость
С растворимость равна 36,0 г в 100 г воды. Найти массовую
долю
равна 36,0 г в 100 г воды. Найти массовую
долю в насыщенном растворе.
в насыщенном растворе.В какой массе воды надо растворить 67,2 л
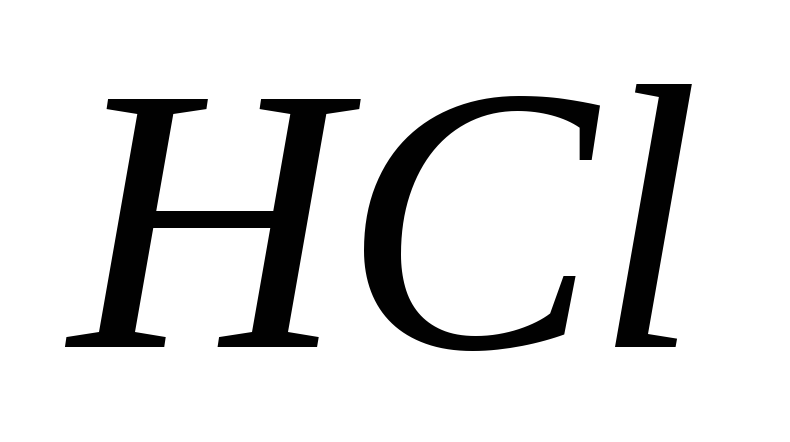 (объем измерен при нормальных условиях),
чтобы получить 9%-ный (по массе) раствор
(объем измерен при нормальных условиях),
чтобы получить 9%-ный (по массе) раствор ?
?В 1 кг воды растворено 176,5 г H2SO4; плотность раствора равна 1,105 г/мл. Найти: а) массовую долю H2SO4; б) молярность;
в) моляльность; г) мольные доли кислоты и воды.
Вариант 4
1.
Найти массу
![]() ,
необходимую для приготовления 300 мл 0,2
М раствора.
,
необходимую для приготовления 300 мл 0,2
М раствора.
2.
Найти молярность 36,2%-ного (по массе)
раствора
![]() ,
плотность которого 1,18 г/мл.
,
плотность которого 1,18 г/мл.
3. В 1 кг воды растворено 87 г Na2SO3; плотность раствора равна 1,075 г/мл. Найти: а) массовую долю Na2SO3; б) молярность;
в) моляльность; г) мольные доли соли и воды.
Вариант 5
1.
В каком объеме 2 М раствора и в каком
объеме 2 н. раствора содержится 114 г
![]() ?
?
2.
Какую массу 20%-ного (по массе ) раствора
![]() надо
добавить к 1 кг 50%-ного (по массе) раствора,
чтобы получить 25%-ный раствор?
надо
добавить к 1 кг 50%-ного (по массе) раствора,
чтобы получить 25%-ный раствор?
3. В 1 кг воды растворено 250 г H2SO4; плотность раствора равна 1,14 г/мл. Найти: а) массовую долю H2SO4; б) молярность;
в) моляльность; г) мольные доли кислоты и воды.
Вариант 6
В каком объеме 1 М раствора и в каком объеме 1 н. раствора содержится 228 г
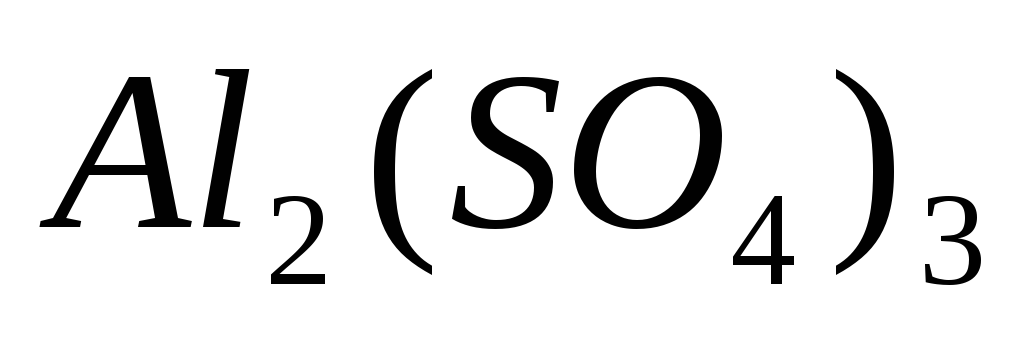 ?
?Плотность 40%-ного (по массе) раствора
 равна 1,25 г/мл. Рассчитать молярность и
моляльность этого раствора.
равна 1,25 г/мл. Рассчитать молярность и
моляльность этого раствора.В 1 кг воды растворено 666 г
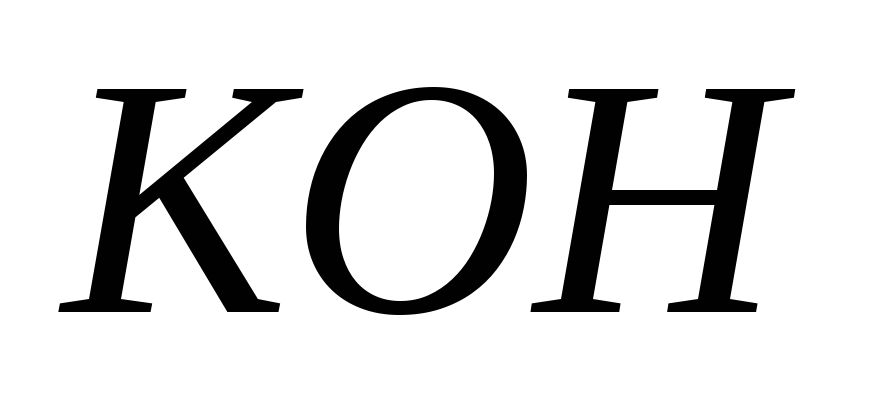 ;
плотность раствора равна 1,395 г/мл. Найти:
а) массовую долю
;
плотность раствора равна 1,395 г/мл. Найти:
а) массовую долю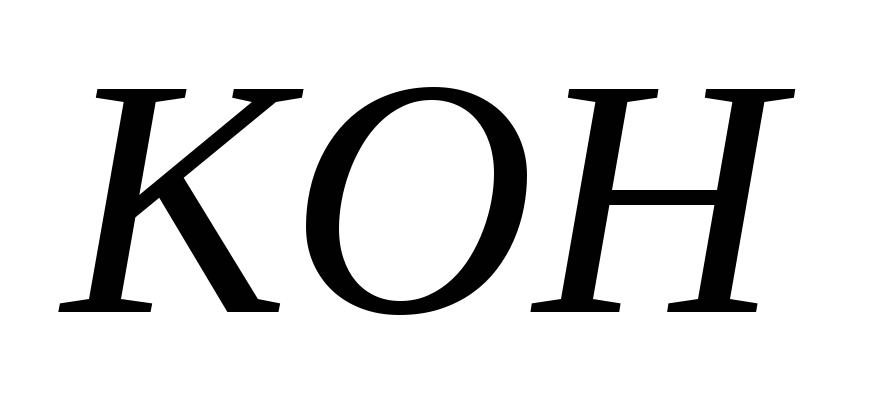 ;
б) молярность;
;
б) молярность;
в) моляльность; г) мольные доли щелочи и воды.
Вариант 7
1.
Сколько мл 0,5 М раствора
![]() можно приготовить из 15 мл
можно приготовить из 15 мл
2,5 М раствора?
2.
Сколько мл 96%-ного по массе раствора
![]() (
(![]() г/мл)
нужно взять для приготовления 1л 0,25 н.
раствора?
г/мл)
нужно взять для приготовления 1л 0,25 н.
раствора?
3. В 1 кг воды растворено 87 г Na2SO3; плотность раствора равна 1,075 г/мл. Найти: а) массовую долю Na2SO3; б) молярность;
в) моляльность; г) мольные доли соли и воды.
ЛИТЕРАТУРА
Химия: Справ. изд./ В.Шретер, К.-Х.Лаутеншлегер, Х.Бибрак и др.: Пер. с нем. – М.:Химия, 1989, 648 с.
Глинка Н.Л. Общая химия:Учебное пособие для вузов./ Под ред. В.А.Рабиновича. Л.: Химия, 1984, 704 с.
ОГЛАВЛЕНИЕ
1. Растворы……………………….……………………………….….3
2. Растворимость……………… …………………………………….5
3. Способы выражения содержания растворенного вещества
в растворе ………………………………………………………….8
4. Индивидуальные задания.……………………………………….. 9
Литература………………………………………………………….11
Светлана Борисовна Белова
Нина Дмитриевна Гришина
Таисия Константиновна Горлачева
РАСТВОРЫ
Методические указания к практической работе по курсу «Химия»
Редактор Соколова М.А.
Подп. в печ.30.06.08. Уч.-изд.л. –0,65. Тираж 50 экз. Зак.78
Издательский центр МАТИ, 109240, Москва, Берниковская наб., 14.
