
11 Лаболаторная работа по химии
.doc
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ОБРАЗОВАНИЮ
ГОСУДАРСТВЕННОЕ ОБРАЗОВАТЕЛЬНОЕ УЧЕРЕЖДЕНИЕ
ВОЛОГОДСКИЙ ГОСУДАРСТВЕННЫЙ ТЕХНИЧЕСКИЙ
УНИВЕРСИТЕТ
Кафедра химии
Электролиз.
(Лабораторная работа №11)
Выполнил: Лебедев Е.А.
Группа СА-12
Проверил: Мальцева С.Б.
Вологда
2006
Цель работы: Ознакомление с электролизом водных растворов некоторых электролитов.
Приборы и материалы: Электроды, раствор электролита, источник питания, необходимые вещества.
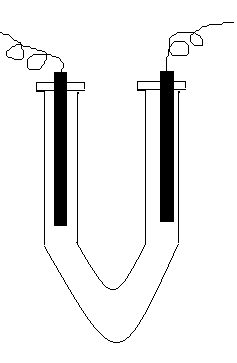
-
U – образная трубка.
-
Электроды.
2
1
Опыт №1. Электролиз водного раствора хлорида кобальта.
На катоде выделился кобальт, йод – крахмальная бумага в колене с анодом потемнела, это объясняется наличием в этом колене хлора, выделившимся в ходе электролиза на аноде.
CoCl2 → Co2+ + 2Cl-
К: Co2+ + 2ē → Co0
А: 2Cl- - 2ē →2Cl0
Опыт №2. Электролиз раствора йодистого калия.
На катоде выделяется калий, соответственно на аноде выделяется йод. Именно поэтому при взятии нескольких капель из анодного пространства, их разбавления, и добавления к ним крахмала раствор посинел. Это объясняется взаимодействием крахмала и йода, так как продукт данной реакции имеет синюю окраску.
KJ → K+ + J-
К: K++ 1ē → K0
А: J-- 1ē →J0
2J→J
Опыт №3. Электролиз раствора сульфата натрия.
Наблюдается бурное выделение газа, а также изменение окраски раствора.
Вывод: Я ознакомился с электролизом водных растворов некоторых электролитов, пронаблюдал происходящие процессы.
