
- •Общая и неоганическая химИя
- •Введение
- •Правила работы в лаборатории
- •Лабораторная работа № 1. Исследование комплексных соединений
- •Общие сведения
- •Выполнение работы Образование комплексных соединений
- •Протокол лабораторной работы
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 2. Исследование окислительно-восстановительных реакций
- •Общие сведения
- •Выполнение работы
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 3. Определение эквивалентной массы металла
- •Общие сведения
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 4. Определение энтальпии реакции нейтрализации
- •Общие сведения
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 5. Исследование скорости химических реакций и химического равновесия
- •Общие сведения
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка экспериментальных данных
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 6. Приготовление раствора и определение его концентрации
- •Общие сведения
- •Выполнение работы
- •Определение концентрации приготовленного раствора титрованием
- •Протокол лабораторной работы
- •Выполнение работы
- •Протокол лабораторной работы
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 8. Исследование гидролиза солей
- •Общие сведения
- •Выполнение работы
- •Протокол лабораторной работы
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 7. Приготовление буферного раствора
- •Общие сведения
- •Выполнение работы
- •I. Выбрать реактивы для приготовления буферного раствора.
- •II. Рассчитать объемы реактивов для приготовления буферного раствора.
- •III. Приготовить буферный раствор и определить его рН
- •IV. Определить буферную емкость
- •Протокол лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Литература
- •Содержание
Выполнение работы
I. Выбрать реактивы для приготовления буферного раствора.
Определение состава буфера с заданным рН начинают с подбора слабой кислоты или слабого основания таким образом, чтобы показатель их константы диссоциации отличался от заданного значения рН или рОН не более, чем на единицу в соответствии с формулой рKd = рН 1. При этом пользуются справочными данными.
II. Рассчитать объемы реактивов для приготовления буферного раствора.
Т.к. концентрации компонентов буферного раствора одинаковы, при расчете объемов компонентов можно пользовать в формуле расчета рН буферного раствора соотношение объемов компонентов.
Для ацетатного буферного раствора объемы кислоты и соли можно вычислить исходя из системы уравнений:
 ,
pKd(CH3COOH)
= 4,756.
,
pKd(CH3COOH)
= 4,756.
Для аммиачно-хлоридного буферного раствора следует рассчитать объемы гидроксида натрия и хлорида аммония. Необходимый для формирования буферного раствора гидроксид аммония получится по реакции:
NH4Cl + NaOH = NH4OH + NaCl.
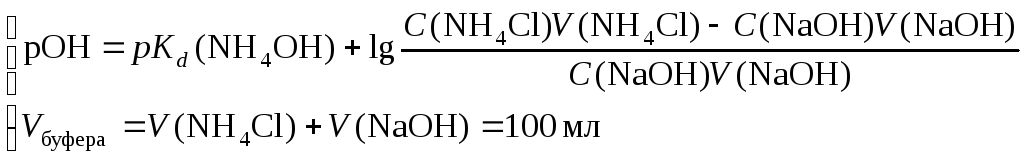 ,
pKd(NH4OH)
= 4,752.
,
pKd(NH4OH)
= 4,752.
III. Приготовить буферный раствор и определить его рН
1. Рассчитанные в п. 2 объемы выбранных растворов отбирают с помощью бюретки на 100 мл и смешивают в колбе на 100 мл.
2. Пробу буферного раствора отобрать в химический стакан объемом 50 мл
3. Включить рН-метр.
4. Вынуть электрод рН-метра из раствора хранения и протереть его кусочком фильтровальной бумаги.
5. Опустить электрод рН-метра в химический стакан с пробой буферного раствора.
6. После того как показания прибора установятся, считать значение рН на экране рН-метра.
IV. Определить буферную емкость
Для ацетатного буфера определяютемкость по щелочи
1. В две конические колбы объемом 50 мл отбирают пипеткой по 5 мл буферного раствора.
2. К каждой пробе добавляют по 3−4 капли фенолфталеина
3. Титруют 0,05 М раствором NaOH до перехода окраски индикатора от бесцветной к розовой.
4. Записать объем титранта VТдля каждой пробы.
Для аммиачногобуфера определяютемкость по кислоте
1. В две конические колбы объемом 50 мл отбирают пипеткой по 5 мл буферного раствора.
2. К каждой пробе добавляют по 3−4 капли метилового оранжевого
3. Титруют 0,05 М раствором HCl до перехода окраски индикатора от желтой к красной.
4. Записать объем титранта VТдля каждой пробы.
Протокол лабораторной работы
1. Значение рН буферного раствора, заданное преподавателем рНтеор.= ……..
2. Реактивы для приготовления буферного раствора и их концентрации.
Для ацетатного буфера – С(СН3СООН) = …………, моль/л
С(CH3COONa) = ……….., моль/л
Для аммиачно-хлоридного буфера – C(NaOH) = …….., моль/л
C(NH4Cl) = ………, моль/л
3. Расчет объемов выбранных растворов
Для ацетатного буфера: V(CH3COOH) = …………, мл
V(CH3COONa) = ………….., мл
Для аммиачно-хлоридного буфера – V(NaOH) = ……., мл
V(NH4Cl) = ………, мл
4. Результат измерения рН приготовленного буферного раствора рНпракт.= ……
5. Объем пробы буфера, взятый для определения буферной емкости Va= …мл
6. Концентрация титранта
Для ацетатного буфера – С(NaOH) = …………, моль/л
Для аммиачно-хлоридного буфера – C(HCl) = …….., моль/л
7. Результаты титрования
Для ацетатного буфера – V(NaOH)1= …………, мл
V(NaOH)2= …………, мл
V(NaOH)ср.= …………, мл
Для аммиачно-хлоридного буфера – V(HCl)1= …….., мл
V(HCl)2= …….., мл
V(HCl)ср. = …….., мл
