
Fizika_sbornik_laboratornykh / Fizika_05M
.docГОУ ВПО
ДВГУПС
Кафедра “Физика”
Лабораторная работа На тему: “Изучение изотермического процесса”
21040165 05М 915
Шифр Номер работы Группа
Выполнил
Навныко А.В.
Проверил: Старший преподаватель кафедры “Оптические системы связи”
Цюй
Хабаровск 2009г.
Цель работы:
Изучить зависимость давления воздуха от объема при постоянной температуре. Измерить изотермический модуль встроенного сжатия. Определить массу воздуха, накачанного в баллон.
Приборы и оборудование:
Воздушные баллоны, микрокомпрессор, краны, клапаны, соединительные трубки.
Краткая теория:
Существуют основные термодинамические параметры: объем, давление, температура. Все они независимы, если система находится в равновесии.
Объем газа всегда совпадает с объемом сосуда, в котором находится.
Давление есть физическая величина, численно равная силе, действующей на единицу площади по нормали к ней. Т.к. обычно рассматривается смесь газов, то вводится понятие парциального давления – давления одного газа из смеси, если бы он занимал весь объем смеси.
Уравнение, которое связывает любой термодинамический параметр с параметрами, принятыми в качестве независимых переменных, называется уравнением состояния.
Простейший объект в термодинамике – идеальный газ – газ, молекулы которого: имеют пренебрежительно малый собственный объем; не взаимодействуют друг с другом; при столкновении ведут себя как абсолютно упругие шарики.
Термодинамическое
уравнение состояния идеального газа,
связывающее параметры идеального газа,
называется уравнением Клапейрона:
![]() .
.
После проведения
некоторых преобразований и идеализировав
это уравнение можно получить наиболее
часто применяемый закон Клапейрона
–Менделеева:
![]() .
.
Термодинамические процессы, в которых изменение состояния газа происходит, когда один из параметров сохраняется постоянным, а два оставшихся изменяются называют изопроцессами.
Различают изотермический, изохорный и изобарный процесс.
При изотермическом
процессе изменение состояния газа
происходит при постоянной температуре
и массе газа. Описывается уравнением
Бойля – Мариотта
![]() .
.
При изобарном
процессе изменение состояния газа
происходит при постоянном давлении.
Описывается уравнениями Гей–Люссака:
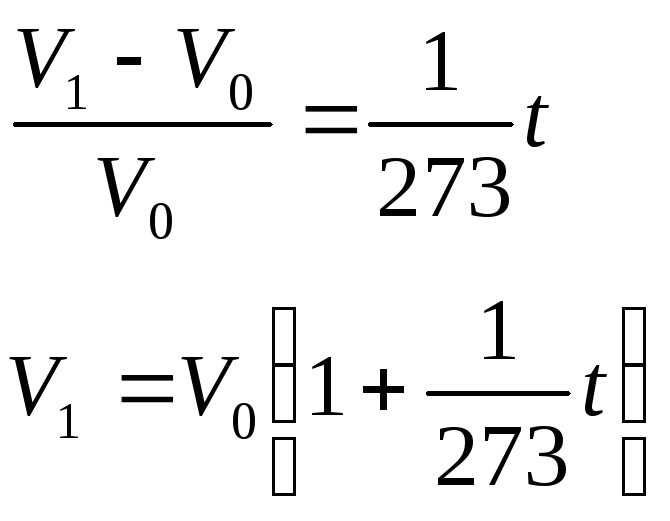
При изохорном процессе изменение состояния газа происходит при постоянном объеме. Описывается уравнениями Шарля:
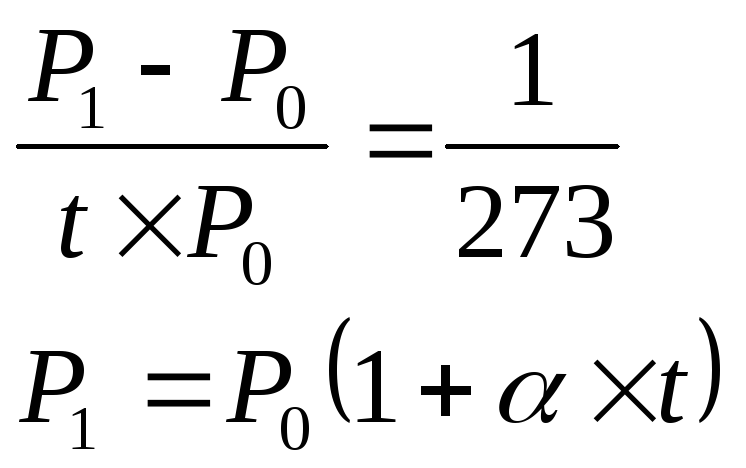
Отметим, что если объем газа в сосуде увеличивается, то газ совершает работу. Это вызвано, прежде всего, передачей импульса молекулами друг другу при движении. Если объем газа уменьшается, то работа газа отрицательна, иначе говоря, работа совершается над ним.
В понятие внутренней
энергии
включается
кинетическая энергия хаотического
движения молекул и потенциальная энергия
взаимодействий молекул. Внутренняя
энергия является функцией состояния
системы. Изменение внутренней энергии
системы при переходе из одного состояния
в другое равно разности значений
внутренней энергии системы в этих
состояниях:
![]() .
.
Внутренняя энергия
может изменяться при осуществлении
различных процессов: в результате
совершения над телом работы; при сообщении
системе количества тепла:
![]() .
.
Отсюда получаем
первое начало термодинамики:
![]() .
.
Заметим, что при изотермическом процессе внутренняя энергия не изменяется. В этом случае количество теплоты, переданное системе, идет на совершение системой работы.
Также существует
процесс, называемый адиабатическим. Он
протекает без теплообмена с внешней
средой. В этом процессе работа совершается
за счет изменения внутренней энергии.
Соотношение параметров идеального газа
(давления и объема) называют уравнением
Пуассона:
![]() .
.
Близкими к адиабатическому могут быть только быстропротекающие процессы.
Проведем соответствующие расчеты и измерения:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
Систематизируем результаты в виде таблиц:
|
№ |
Разность уровней в манометре
|
Объем воздуха в баллонах
|
Обратный объем
|
|
1 |
2499 |
0,7 |
1428,5714 |
|
2 |
1274 |
1,4 |
714,2857 |
|
3 |
686 |
2,1 |
476,1905 |
Вывод:
Выполняя данную работу, я ставил себе цели изучить зависимость давления воздуха от объема при постоянной температуре, измерить изотермический модуль встроенного сжатия, определить массу воздуха, накачанного в баллон.
В ходе работы я использовал установку, состоящую из герметично соединенных между собой микрокомпрессора, барометра и трех баллонов. Изолировав первый баллон от остальных, я накачивал в него воздух, производил измерения давления с помощью барометра. Затем я открывал кран между первым и вторым баллонами, т.о. объем увеличился вдвое, вновь были проведены измерения барометром. И, наконец, мною был открыт кран, соединяющий первые два баллона с третьим. Объем увеличился втрое по сравнению с первоначальным. Показания барометра были зафиксированы в таблицу.
Далее я заполнил
таблицу и используя формулы
![]() - изотермический модуль и
- изотермический модуль и
![]() - масса идеального газа, рассчитал
необходимые величины.ъем
увеличился втрое по сравнению с
первоначальным.два баллона с третьим.
- масса идеального газа, рассчитал
необходимые величины.ъем
увеличился втрое по сравнению с
первоначальным.два баллона с третьим.
