Часть 2.
Для
записи ответов на задания 36 - 40 используйте
бланк ответов № 2. Запишите сначала
номер задания (С1 и т.д.), а затем полное
решение. Ответы записывайте четко и
разборчиво.
36
Используя метод электронного баланса,
составьте уравнение реакции:
NH3
+ KMnO4
+ ... →...
+ K2MnO4
+ H2O.
Определите
окислитель и восстановитель.
37
Навеску
алюминия растворили в разбавленной
азотной кислоте, при этом выделялось
газообразное простое вещество. К
полученному раствору добавили карбонат
натрия. Выпавший осадок
отфильтровали
и прокалили,
фильтрат упарили,
полученный твёрдый остаток
сплавили
с хлоридом аммония.
Напишите
уравнения четырёх описанных реакций.
38
Напишите уравнения реакций, с помощью
которых можно осуществить следующие
превращения:
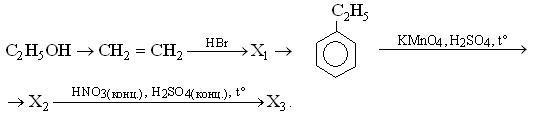
При
написании уравнений реакций используйте
структурные формулы органических
веществ.
39
Газ, полученный при сжигании 19,2 г серы,
без остатка прореагировал с 682,5 мл
5%-ного
раствора едкого натра (плотность 1,055
г/мл). Определите состав полученного
раствора и рассчитайте массовые доли
веществ в этом растворе.
40
При
сжигании 29,7 г органического вещества
выделилось 13,44 л (н.у.) углекислого газа,
5,4 г воды и 21.9 г хлороводорода.
Плотность паров
вещества по азоту 3,536. Вещество реагирует
с водным раствором гидроксида натрия,
продукт последней реакции растворяет
свежеполученный гидроксид меди(II).
На
основании данных условия задания:
1)произведите
необходимые вычисления для установления
молекулярной формулы органического
вещества;
2)установите
молекулярную формулу исходного
органического вещества;
3)составьте
структурную формулу исходного вещества,
которая однозначно отражает порядок
связи атомов в его молекуле;
4)напишите
уравнение реакции этого вещества с
водным раствором гидроксида натрия.