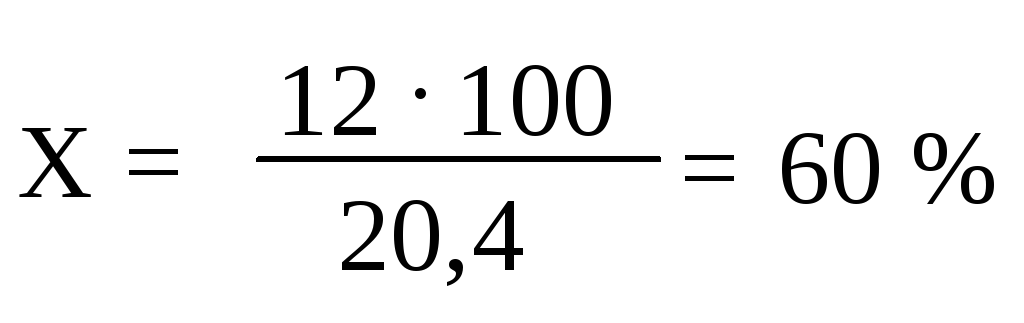- •Методы очистки органических соединений
- •5. Аллонж
- •Схемы приборов
- •Схемы приборов
- •I - круглодонная колба; 2- обратный водяной холодильник
- •I- воронка для горячего фильтрования; 2 - химическая воронка;
- •Диазотирование синтез иодбезнзола из анилина /5/
- •Схемы основных приборов
- •Определение показателя преломления
Схемы основных приборов

1 – предохранительная трубка; 2 - парообразователъ; 3 – тройник; 4 – винтовой зажим; 5 – трубка по которой поступает пар; 6 – перегоняемое вещество и вода; 7 - перегонная колба; 8 – пароотводная трубка; 9 - холодильник; 10 – аллонж; 11 - приемник.
Рисунок 1- Прибор для перегонки с водяным паром

1 - плитка; 2 - перегонная колба; 3 - химический термометр; 4 - прямой воздушный холодильник; 5 - аллонж; 6 - приемник
Рисунок 2 - Прибор для перегонки иодбензола
Таблица 3 - Описание хода синтеза
|
Ход синтеза |
Наблюдения, объяснения |
|
1 |
2 |
|
I этап: реакция диазотирования В фарфоровом стакане вме-стимостью 250 мл смешиваю 25 мл конц. соляной кислоты с 25 мл воды и к раствору прибавляю 7,6 мл анилина. Раствор охлаждаю до 1-2 °С добавляю из капельной воронки при непрерывном перемешивании раствор 8 г нитрита натрия в 20 мл воды. Добавление нитрита натрия следует вести с такой скоростью, чтобы температура не поднималась выше 8 °С. Через 10 мин после окончания добавления раствора азотистокислого натрия делаю пробу на присутствие свободной азотистой кислоты.
II этап: превращение соли диазония в иодбензол. Раствор соли диазония смешиваю в круглодонной колбе вместимостью 500 мл с раствором 20 г йодистого калия в 30 мл воды и оставляю в ледяной бане. Ш этап: отгонка иодбензола с водяным паром. Раствор подщелачиваю конц. раствором гидроксида натрия до сильно-щелочной реакции (рН=10). Иодбензол отгоняю с водяным паром. IV этап: экстракция и осушка Иодбенол отделяю, водный раствор дважды экстрагирую эфиром порциями по 20 мл. Иодбензол соединяю с эфирными вытяжками, сушу хлористым кальцием. V этап: перегонка иодбензола Фильтрую под тягой осушенный эфирный раствор в перегонную колбу. Отгоняю на водяной бане с холодильником эфир, меняю холодильник на воздушный и на плитке отгоняю иодбензол (рис. 2).
|
Происходит реакция диазотирования 1. Никаких видимых изменений в реакционной смеси не наблюдаю.
Иодкрахмальная бумажка не синеет, значит свободной азотистой кислоты в смеси нет. Диазотирование закончено. Раствор азотистокислого натрия прикапывал в течение 40 мин. Происходят реакции 2 и 3. Образуются темно-вишневые маслянистые капли. Смесь стояла в ледяной бане 1,5 часа. После этого работу прекращаю на неделю.
Происходит реакция 4, фенолят (ионное соединение) с водяным паром не перегоняется. Тяжелые маслянистые капли собираются на дне приемника.
Растворений в воде иодбензол переходит в эфир, эфирный слой окрашивается в желтый цвет. Раствор становится прозрачным.
Иодбензол отгонялся в интервале 184-189 °С, продукт представляет собой темно-красную жидкость с резким неприятным запахом. |
Выход иодбензола – 12 г
Расчет выхода в процентах от теоретического:
|
20,4г - 100% 12 г - X |
|
Расчет выхода от указанного в методике:
|
16г - 100% 12 г - У |
|
Таблица 4 - Константы иодбензола
|
Название и структурная формула |
Молекулярная масса |
Константы |
Плотность, г/см3 |
Тпл., оС |
Ткип., оС |
Показатель преломления |
Растворимость |
Примечание (токсичность) |
Ссылка на литературные источники |
|
Иодбензол
|
204,5 |
Литературные |
1,83815 |
31,4 |
138,7 |
1,621318 |
в воде, сп., э., хл. |
Наркотик оказывает влияние на кроветворение, может вызвать экзему |
2, с. 433 |
|
Полученные |
- |
- |
184-189 |
1,622920 |
ОПРЕДЕЛЕНИЕ ТЕМПЕРАТУРЫ ПЛАВЛЕНИЯ ТВЕРДОГО ВЕЩЕСТВА
Температура, выше которой кристаллическое органическое вещество превращается в жидкость, называется температурой плавления. Температура плавления является физической константой и используется в качестве критерия чистоты твердых веществ. Чистое вещество плавится резко при определенной температуре. Наличие в веществе примесей или влаги приводит к понижению температуры
|
|
плавления, Прибор для определения температуры плавления изображен на рисунке. Для веществ с температурой плавления выше 250 °С используется прибор, не содержащий жидкого теплоносителя. Вещество, температуру плавления которого надо определить, помещают в капилляр, запаянный с нижнего конца. Кусочки капилляров нужного диаметра запаивают с одного конца, осторожно внося их сбоку в пламя горелки. Капилляр наполняют веществом так, чтобы плотный слой его занимал около 0,5 см. Для этого небольшое количество вещества мелко измельчают на часовом стекле, собирают |
его в кучку и погружают в нее открытый конец капилляра. Сместить это вещество вниз к запаянному концу и утрамбовать его можно, бросая капилляр с веществом запаянным концом вниз в стеклянную трубку длиной 50-60 см. Заполненный капилляр прикрепляют посредством резинового кольца к термометру на уровне ртутного шарика так, чтобы было видно одновременно и шкалу термометра и содержимое капилляра на просвет. Прибор нагревают на спиртовке сначала быстро, а когда показания термометра достигнут величины на 10-15 °С ниже предполагаемой температуры плавления, нагрев уменьшают. За начало плавления принимают начало уменьшения высоты столбика вещества в капилляре, за конец плавления - момент полного расплавления вещества с превращением его в прозрачную жидкость. Интервал температур между началом плавления и его окончанием тем, меньше, чем чище вещество. Считается допустимым интервал плавления 1-2 °С.