
- •Глава 9. Физико-химические
- •9.1. Анализ состава газовой фазы в зоне столба дуги
- •9.1.2. Образование соединений между компонентами газовой смеси
- •9.1.3. Насыщение расплавленного металла газами в капле и сварной ванне
- •9.2. Влияние атмосферных газов на свойства стали и сплавов при сварке
- •9.2.1. Влияние кислорода на свойства стали
- •9.2.3. Влияние водорода на свойства стали
- •9.2.4 Влияние со2, со и паров н2о на свойства стали
- •9.2.5. Влияние атмосферных газов на свойства цветных металлов
- •9.3. Взаимодействие металла с защитными флюсами при сварке
- •9.3.1. Строение и свойства сварочных флюсов
- •9.3.2. Характеристика важнейших простых оксидов, входящих в состав шлаковой фазы
- •9.3.3. Основные системы сварочных шлаков
- •9.4. Массообмен между расплавленным металлом, газовой средой и шлаком
- •9.5. Расплавление электрода и перенос капель в ванну
- •9.6. Источники водорода при сварке под флюсом
- •9.7. Окисление металла шва флюсом
- •9.8. Переход вредных примесей из флюса в металл шва
- •9.9. Раскисление металла при сварке
- •9.9.1. Виды раскисли тельных процессов
- •9.9.2. Легирование наплавленного металла
- •9.10. Рафинирование сварочной ванны и модифицирование металла шва
- •9.10.1. Влияние серы на структуру и свойства шва
- •9.10.2. Десульфурация сварочной ванны
- •9.10.3. Снижение содержания фосфора в металле шва
- •9.11. Дефекты металлургического происхождения в сварных швах
- •9.11.2. Шлаковые включения в металле шва
- •9.11.3. Ликвационная неоднородность в металле шва
9.1.2. Образование соединений между компонентами газовой смеси
Наряду с диссоциацией простых и сложных молекулярных газов для высоких температур сварки плавлением характерно образование молекул газа в эндотермических реакциях при взаимодействии кислорода и водорода с другими газами: азотом, водородом и фтором. Например, азот N2 и кислород О2 при Т= 3500 К взаимодействуют с образованием оксида азота NO по реакции, которая сопровождается поглощением тепла:
![]() (9.14)
(9.14)
Образующийся оксид азота может существовать в нераспавшемся виде при пониженных температурах (Г< 3500 К). В контакте с металлом ванны при температурах 1800... 1900 К он распадается и играет существенную роль как окислитель; он передает атомы кислорода и азота на поверхность жидкого металла. По мнению многих исследователей, оксид азота одновременно передает азот и кислород расплавленному металлу. Подтверждением этому служит тот факт (рис 9.5), что с увеличением кислорода в газовой среде растет и насыщение металла азотом, хотя степень его диссоциации невелика (см. рис. 8.9).

В низкотемпературной зоне также происходят реакции образования соединений ОН и фтористого водорода HF, не растворимых в металле. Эти реакции используют для снижения парциального давления водорода над сварочной ванной.
9.1.3. Насыщение расплавленного металла газами в капле и сварной ванне
В жидком металле капель и сварочной ванны происходят процессы растворения газов столба дуги. В сварочной ванне эти процессы протекают менее интенсивно, чем в каплях, по следующим причинам:
температура жидкого металла в сварочной ванне ниже, чем в каплях, где она приближается к температуре кипения металла;
для сварочной ванны отношение поверхности реакции к объему значительно меньше, чем для капель.
Растворимость газа в жидком металле также зависит от его парциального давления и состояния. Если газ находится в атомарном состоянии, то его растворимость в металле [Г] при Т = const согласно закону Генри прямо пропорциональна его давлению ([Г] = К1 рг), а растворимость двухатомных газов, находящихся в молекулярном состоянии, подчиняется закону Сивертса ([Г2] = К2√рг2), т.е. прямо пропорциональна корню квадратному из давления газа.
Количество растворяющегося в металле газа [С]г для большинства металлов увеличивается с ростом температуры по следующей зависимости:
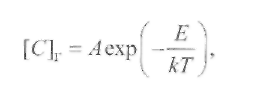 (9.15)
(9.15)
где А и к - константы; Е - теплота растворения газа в металле.
Из уравнения (9.15) следует, что с увеличением температуры металла повышается и содержание растворенного в нем газа, причем в каплях оно может быть значительным. Однако нельзя забывать, что при температурах, близких к температуре кипения металла, имеет место и обратный процесс: содержание газа в металле заметно падает и в момент кипения становится равным нулю, поскольку образуется много паров металла, а парциальное давление газа при этом снижается.
Процесс растворения газов в жидком металле состоит из отдельных, протекающих последовательно стадий (подробно рассмотренных в гл. 8):
адсорбции атомов газа поверхностью металла капли и сварочной ванны;
взаимодействия адсорбированного газа в поверхностном слое с металлом, т. е. образования растворов и химических соединений (этот процесс называется хемосорбцией);
отвода продуктов хемосорбции в глубь жидкого металла.
Адсорбция и хемосорбция протекают с очень большими скоростями - практически мгновенно. Отвод продуктов хемосорбции в глубь жидкого металла происходит с меньшей скоростью. На этой стадии процесса растворения газов в жидком металла большую роль играет механическое перемешивание. При сварке оно проявляется довольно значительно вследствие интенсивного турбулентного движения расплава (из головной части сварочной ванны в хвостовую, см. рис. 9.2), обусловленного давлением дуги на жидкий металл. Наибольшее насыщение металла газом происходит в каплях. Оно зависит от длительности пребывания капли на торце электрода и времени ее пролета через столб дуги, а также от температуры капли. Температура, максимальная при коротком замыкании столба дуги каплей, зависит от состава газовой среды. По данным А.Я. Ищенко, в условиях сварки в аргоне при Iсв = 400 А алюминиевого сплава АМг6, плавящегося при ~ 970 К, температура капель достигает 2100 К, а при сварке в гелии - значительно меньшего значения: 1900 К.
Рассмотренная схема растворения атомарных газов в металле, в основе которой лежит закон Генри, получила название химического поглощения газов металлом.
М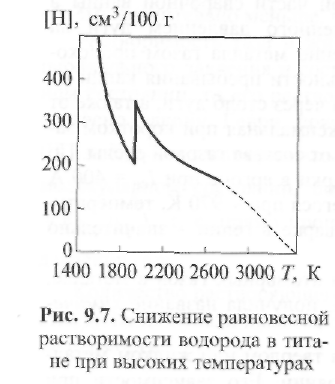 аксимальное
насыщение газов в твердом или жидком
металле достигается в равновесном
состоянии. Его зависимости при нормальном
давлении от температуры и фазового
состояния дляFe,
A1,
Сu,
Ni
и Ti
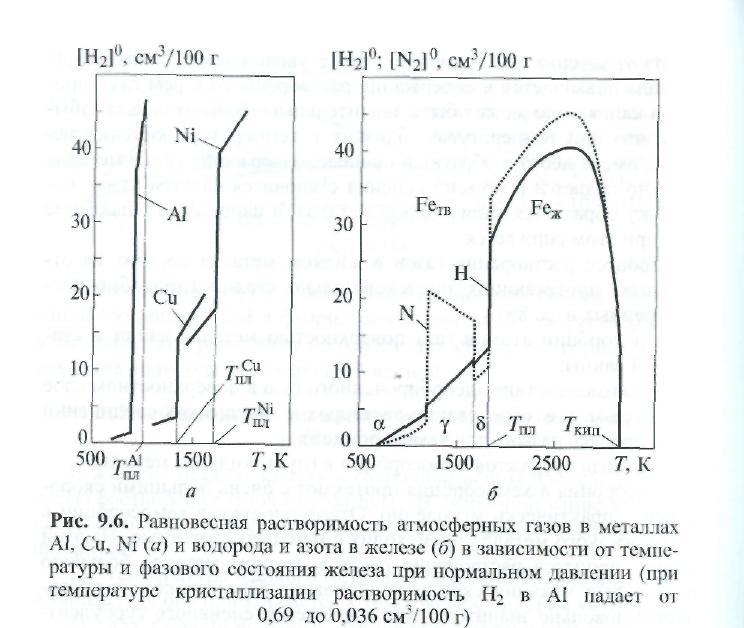
представлены на рис. 9.6 и 9.7. Из рис. 9.6
следует, что равновесная
растворимость атмосферных газов при
нормальном давлении в алюминии А1, меди
Сu,
никеле Ni
существенно зависит от температуры
и агрегатного состояния металла (при
температуре кристаллизации растворимость
Н2
в А1 падает от 0,69 до 0,036 см3
/100 г), а их растворимость в железе - и
от фазовой модификации: Feα
, Feγ,
Feδ.
аксимальное
насыщение газов в твердом или жидком
металле достигается в равновесном
состоянии. Его зависимости при нормальном
давлении от температуры и фазового
состояния дляFe,
A1,
Сu,
Ni
и Ti
представлены на рис. 9.6 и 9.7. Из рис. 9.6
следует, что равновесная
растворимость атмосферных газов при
нормальном давлении в алюминии А1, меди
Сu,
никеле Ni
существенно зависит от температуры
и агрегатного состояния металла (при
температуре кристаллизации растворимость
Н2
в А1 падает от 0,69 до 0,036 см3
/100 г), а их растворимость в железе - и
от фазовой модификации: Feα
, Feγ,
Feδ.
При электродуговой сварке наличие электрического поля создаст возможность электрического поглощения газов металлом. Оно наблюдается только у поверхности катода а области активного пятна, куда внедряются положительные ионы газов, переносящие заряды столба дуги. Наличие у поверхности катода слоя положительных ионов повышенной концентрации приводит к их перемещению в объем металла диффузионным путем вследствие выравнивания разности концентраций (по механизму концентрационной диффузии). Поэтому при сварке на обратной полярности («+» на электроде) в капле растворяется меньше водорода. Это снизит концентрацию Н2 и в ванне. Степень развития электрического поглощения газов металлом зависит также от значения катодного падения потенциала, состава газовой среды, силы тока и других факторов.
