
- •ЧАСТЬ I. ОБЩИЕ ВОПРОСЫ
- •Введение. Основные задачи и значение инженерной геологии
- •Глава 1. Основные сведения о Земле
- •§ 1. Происхождение Земли
- •§ 2. Форма, масса и плотность Земли
- •§ 3. Строение Земли
- •ЧАСТЬ II. МИНЕРАЛЫ И ГОРНЫЕ ПОРОДЫ
- •§ 1.3. Метаморфические процессы минералообразования
- •§ 2. Строение минералов
- •§ 3. Химический состав минералов
- •§ 5. Классификация и распространенность минералов
- •§ 1. Структура и текстура горной породы
- •§ 2. Магматические горные породы
- •§ 3. Осадочные горные породы
- •§4. Метаморфические горные породы
- •ЧАСТЬ III. ОСНОВНЫЕ СВЕДЕНИЯ О ТЕКТОНИКЕ
- •§ 1. Колебательные движения земной коры
- •§ 2. Складчатые и разрывные движения
- •§ 3. Ненарушенное и нарушенное залегание горных пород
- •§ 1. Трещиноватость горных пород
- •§ 2. Геометрические элементы тектонических разрывов
- •ЧАСТЬ IV. ГЕОЛОГИЧЕСКАЯ ИСТОРИЯ ЗЕМЛИ
- •ЧАСТЬ V. ГРУНТОВЕДЕНИЕ
- •ЧАСТЬ VI. ПОДЗЕМНЫЕ ВОДЫ
- •Глава 1. Виды подземных вод
- •Глава 2. Химический состав подземных вод
- •Глава 3. Законы движения подземных вод
- •§ 1. Связь расхода и напора подземного потока
- •§ 2. Общие условия движения подземных вод
- •§ 3. Методы определения коэффициента фильтрации
- •Глава 4. Воздействие подземных вод на горные породы и грунты
- •§ 1. Гидростатическое и гидродинамическое давление в нескальных грунтах
- •§ 2. Явление плывунности
- •ЧАСТЬ VII. ИНЖЕНЕРНО-ГЕОЛОГИЧЕСКИЕ ПРОЦЕССЫ
- •Глава 1. Выветривание и связанные с ним явления
- •§ 1. Виды выветривания
- •§ 2. Меры борьбы с процессами выветривания
- •§ 3. Геологическая деятельность ветра
- •Глава 2. Геологическая деятельность атмосферных и поверхностных вод
- •§ 1. Виды речных долин и русловых отложений
- •§ 2. Методы борьбы с негативными последствиями геологической деятельности атмосферных и поверхностных вод
- •§ 1. Ледники, моря и озера. Защита берегов
- •§ 2. Неблагоприятные процессы и явления, возникающие на искусственных водохранилищах и меры борьбы с ними
- •Глава 4. Суффозия механическая и химическая. Плывуны. Методы борьбы с суффозией и плывунами
- •§ 1. Суффозия механическая и химическая
- •§ 2. Методы борьбы с суффозией и плывунами
- •Глава 5. Движение грунтов на склонах и откосах. Меры предупреждения и борьбы с оползнями
- •§ 1. Движение грунтов на склонах и откосах
- •§ 2. Меры предупреждения и борьба с оползнями
- •Глава 6. Процессы и явления, связанные с промерзанием и оттаиванием грунтов
- •Глава 7. Просадочные явления
- •Глава 8. Процессы и явления, возникающие в грунтах под сооружениями
- •ЧАСТЬ VIII. ИНЖЕНЕРНО-ГЕОЛОГИЧЕСКИЕ ИЗЫСКАНИЯ ДЛЯ СТРОИТЕЛЬСТВА
- •Глава 1. Стадии проектирования
- •Глава 2. Методы инженерно-геологических исследований
- •Глава 3. Инженерно-геологические исследования для гидротехнического строительства
- •БИБЛИОГРАФИЧЕСКИЙ СПИСОК
- •СОДЕРЖАНИЕ
91
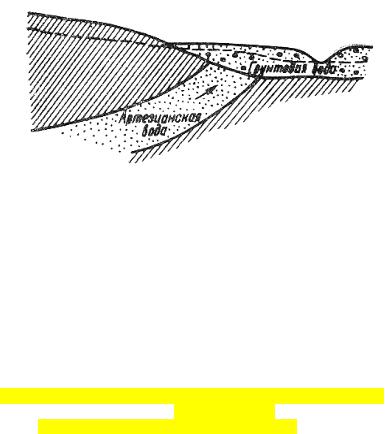
Рис. 6.9. Схема питания грунтовых вод артезианскими.
Глава 2. Химический состав подземных вод
Химическийсоставподземныхводобычноменяетсявзависимости от времени года (за исключением глубоких артезианских бассейнов).
Подземныеводы обычно используютсядля целей питьевого, техническоговодоснабженияиирригации. Встроительствезнаниехимизма подземныхводнеобходимодляопределениястепениихагрессивностипо отношениюктемилиинымстроительнымматериалам(например, кбетону), а в гидротехническом строительстве, также и к горным породам и минералам.
Реакцияводыоцениваетсяпопоказателюконцентрациивводеводородного иона. Любая природная вода содержит какое-то количество
диссоциированных водородных ионов Н+ и гидроксил-ионов ОН- :
Н2О ↔ Н+ + ОН–
ВнейтральнойводеколичествоионовН=ОН. Накаждые10 миллионов молекул Н2О приходится один ион Н+.
Такимобразом, концентрацияионовН+ дляабсолютночистойнейтральной воды составляет 10-7. Эта величина обозначается рН: рН=7 – нейтральная вода; рН<7 – кислая вода; рН>7 – щелочная вода (рН=0 – кислота в нормальном растворе; следовательно, чем меньше рН, тем более кислая и агрессивная вода).
Жесткость воды обусловлена присутствием солей Ca и Mg. Жесткость измеряется в градусах или в миллиграмм-эквивалентах на литр. За единицу жесткости принимают 1 мг-экв Са, то есть 20,04 мг Са на 1л воды.
Содержание свободной углекислоты (СО-) в воде должно соот-
ветствоватьравновесиюсодержащихсявводесоединенийHCO3 иCaCO3. Если в воде избыток ионов СО-, то при соприкосновении такой воды с
