
Азот (n2)
Входит в состав белков, нуклеиновых кислот, фосфолипидов мембран, порфиринов (основа хлорофилла и цитохромов), многочисленных ферментов (в т.ч. NAD и NADP) многих витаминов.
При недостатке азота в среде тормозится рост растений, ослабляется образование боковых побегов, наблюдается мелколистность и бледно-зелёная окраска листьев вследствие разрушения хлорофилла.
Несмотря на наличие в атмосферном
воздухе 78 % N2(4![]() 105т), такой молекулярный азот не усваивается
высшими растениями (молекула азота
(N
105т), такой молекулярный азот не усваивается
высшими растениями (молекула азота
(N![]() N)
химически инертна; для разрыва трех ее
ковалентных связей в химическом процессе
синтеза аммиака требуются катализаторы,
высокие температура и давление) и может
переходить в доступную для них форму
только благодаря деятельности
микроорганизмов-азотфиксаторов. Из
литосферных запасов азота (18
N)
химически инертна; для разрыва трех ее
ковалентных связей в химическом процессе
синтеза аммиака требуются катализаторы,
высокие температура и давление) и может
переходить в доступную для них форму
только благодаря деятельности
микроорганизмов-азотфиксаторов. Из
литосферных запасов азота (18![]() 1015т) в почве сосредоточена лишь его
минимальная часть, из которой лишь 0,5 –
2 % прямо доступно растениям: - этоNH4+иNO3--ионы,
образующиеся в результате минерализации
бактериями органического азота
растительных и животных остатков и
гумуса. А именно, процессов:
1015т) в почве сосредоточена лишь его
минимальная часть, из которой лишь 0,5 –
2 % прямо доступно растениям: - этоNH4+иNO3--ионы,
образующиеся в результате минерализации
бактериями органического азота
растительных и животных остатков и
гумуса. А именно, процессов:
Аммонификации (превращение органического азота вNH4+);
Нитрификации (окислениеNH4+доNO3-);
![]()
![]()
Денитрификации (анаэробное восстановлениеNO3-доN2)
Фиксация молекулярного азота (N2)
Химическое связывание молекулярного азота в форме NH4+илиNO3-осуществляется либо в результате электрических разрядов в атмосфере, либо в присутствии катализатора при температуре более 5000С и атмосферном давлении около 35 МПа.
Биологическое связывание молекулярного азота атмосферы осуществляется азотфиксирующими микроорганизмами. Они бывают:
Свободноживущие(р.Azotobacter,Beijrinckia– аэробные и р.Clostridium– анаэробные);
*Симбиотические(р.Rhizobium, образующий клубеньки на корнях бобовых растений, и некоторые актиномицеты).
*Инфицирование растения хозяина симбиотическими бактериями начинается с проникновения бактерии в клетку корневого волоска, миграции в клетки коры и интенсивного деления инфицированных клеток, что приводит к образованию клубеньков на корнях. При этом сами бактерии превращаются в бактероиды, которые в 40 раз больше по размеру, чем исходная бактерия. Основная роль в процессе азотфиксации принадлежит ферментунитрогеназе.Фермент состоит из двух компонентов: более высокомолекулярногоFe-Moбелка (Мr= 200-250 000, 2 молекулыMo, 30 молекулFeи 22 молекулыS) иFe-белка (Мr= 50-70 000, 4 молекулыFeи 4 молекулыS).Fe-Moбелок служит для связывания и восстановления молекулярного азота, аFe-белок служит источником электронов для восстановленияFe-Moбелка, которые он получает от ферредоксина. Весь комплекс работает только в присутствии гидролиза АТР и защитного действия белка легоглобина (синтезируется клетками хозяина и защищает нитрогеназу от кислорода).

Образующийся NH4+, связывается с кетокислотами, образуя аминокислоты, транспортируемые в клетки растения-хозяина.
Редукция нитрата и пути ассимиляции аммиака
Так как в органические соединения включается только аммонийный азот, нитрат-ионы NO3-, поглощаемые корнем, должны восстанавливаться в клетках до аммиака. Осуществляется это в два этапа:
Восстановление нитрата до нитрита, катализируемое нитратредуктазой (в цитоплазме); NO3- ---2 e---- NO2-
Восстановление нитрита до аммиака, катализируемое нитритредуктазой (в хлоропластах). NO2- ---- 6e--- NH4+
Аммиак, образующийся при восстановлении нитратов или в процессе фиксации молекулярного азота,далее усваивается растениями с образованием различных аминокислот. В первую очередь акцептором NH4+является α-кетоглутаровая кислота, которая под действиемглутаматдегидрогеназыпревращается в глутамат.
+
+
NH3
NADPH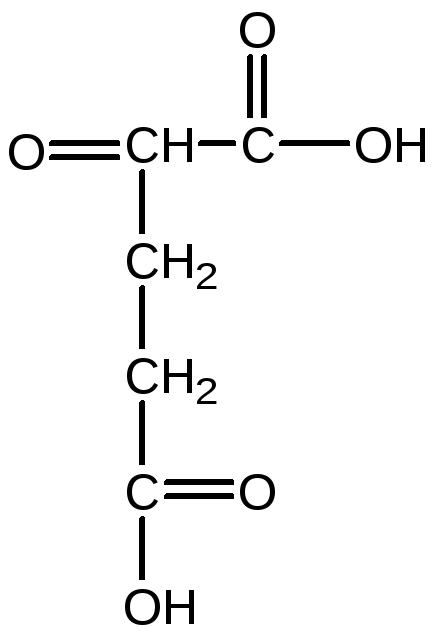
![]() H+
H+

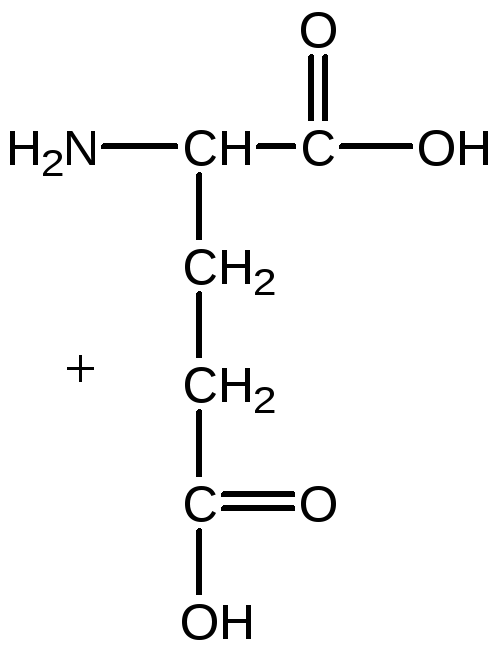
α-кетоглутаровая кислота глутамат
Этот фермент активен в корнях и листьях растений, преимущественно в митохондриях.
Аминная группа глутамата может переноситься на другие кетокислоты в результате трансаминирования (ферменты – аминотрансферазы).
Таким образом, возможен синтез различных
аминокислот:
-аланиниз пировиноградной кислоты;
-аспарагиновая кислота– из
щавелевоуксусной кислоты;
- глицин– из глиоксиловой;
-фенилаланин– из фенилпировиноградной
кислоты

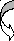 глутаминовая пировиноградная
глутаминовая пировиноградная
кислота ГЛУ кислота ПВК
α-кетоглутаровая аланин АЛА
кислота
Кроме того, ассимиляция аммиака может также осуществляться при участии фермента глутаминсинтетазы, который активен в хлоропластах и цитоплазме. Он принимает участие в аминировании глутамата до глутамина, который является одной из форм транспорта азота по растению.Этот процесс является энергозависимым.
+
NH4+
АТР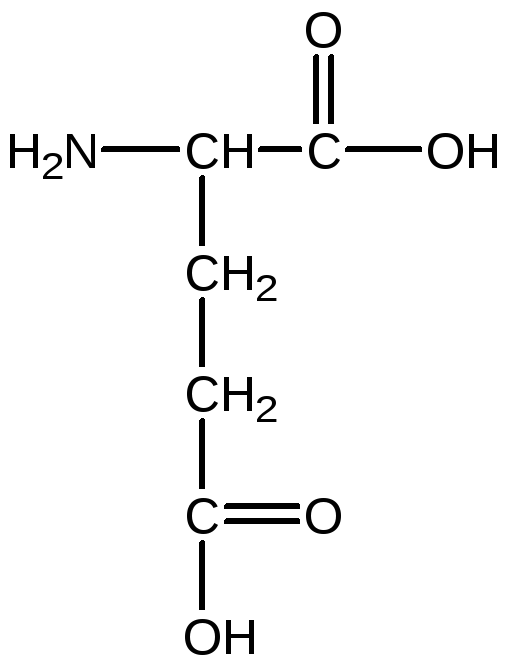

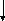
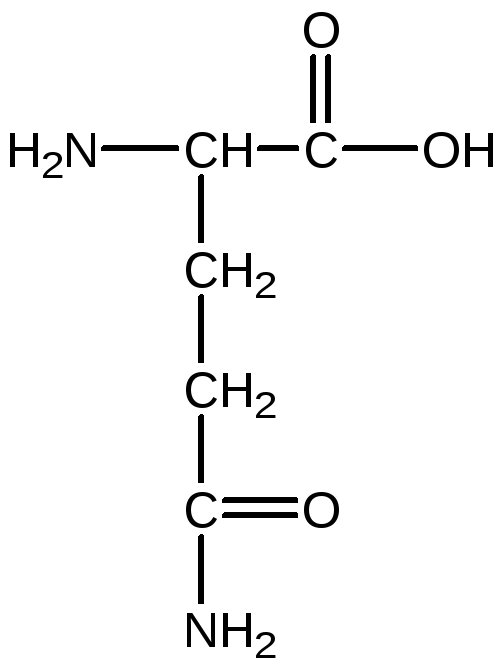
глутамат глутамин
Принято считать, что образование аспарагина преобладает в том случае, когда происходит распад белков в семенах. В клетках корня и листьев растущего растения идет, главным образом, образование глютамина. Таким образом, образование аспарагина - это путь обезвреживания аммиака, появляющегося при распаде белка - так называемая регрессивная ветвь азотного обмена, тогда как синтез глютамина - это путь обезвреживания аммиака при синтезе белка - прогрессивная ветвь азотного обмена.
Роль амидов в растении разнообразна. Это не только форма обезвреживания аммиака, это и транспортная форма азотных соединений, обеспечивающая отток их из одного органа в другие. Кроме того, амиды и их предшественники аминокислоты являются материалом для создания многих других аминокислот в реакциях переаминирования, когда аминогруппа аминокислоты обменивается с кетогруппой кетокислоты с образованием аминокислоты.
