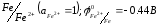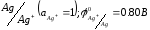- •Фізична та колоїдна хімія
- •Фізична хімія
- •Тема 1. Хімічна термодінамика
- •Тема 2. Хімічна кінетика та рівновага. Каталіз
- •Тема 3. Розчини
- •Тема 4. Електрохімія
- •Колоїдна хімія
- •Тема 5. Фізико-хімія поверхневих та сорбційних явищ
- •Тема 6. Дисперсні системи. Класифікація, методи одержання та очищення.
- •Тема 7. Молекулярно-кінетичні, оптичні та електричні властивості дисперсних систем
- •Тема 8. Стійкість та коагуляція дисперсних систем.
- •Тема 9. Фізико-хімія вмр.
- •Тема 1 «Хімічна термодінамика».
- •Тема 2 «Хімічна кінетика та рівновага. Каталіз»
- •Тема 3 «Розчини»
- •Тема 4 «Електрохімія»
- •Колоїдна хімія
- •Тема 5 «Фізико-хімія поверхневих та сорбційних явищ».
- •Тема 6 «Загальна характеристика дисперсних систем. Класифікація, отримання та очищення дисперсних систем».
- •Тема 7 – 8 «Молекулярно-кінетичні, оптичні та електричні властивості дисперсних систем», «Стійкість та коагуляція дисперсних систем»
- •Тема 9 «Фізико-хімія вмр».
Тема 4. Електрохімія
Конкретні цілі
1.Електропровідність розчинів електролітів. Питома електрична провідність. Молярна електрична провідність, її залежність від розбавлення розчину електроліту. Молярна електрична провідність.Закон Кольрауша.
2.Механізм виникнення електродного потенціалу. Рівняння Нернста. Класифікація електродів: електроди першого та другого родів, газові, окисно-відновні, йонселективні (ПСЕ).
3.Оборотні та необоротні гальванічні елементи. Кола без переносу і з переносом. Концентраційні кола. Дифузійний потенціал.
4.Термодинамічні характеристики реакцій, що відбуваються в гальванічних елементах. Електроди порівняння та індикаторні електроди, що застосовують у різних видах потенціометричного титрування.
Джерела інформації:
1. Физическая и коллоидная химия / Под ред. В.И.Кабачного, - Харьков: Изд-во НФаУ, 2005, с. 110-139.
2. Физическая и коллоидная химия: Учебн. Для фарм. Вузов и факультетов / Под ред. К.И.Евстратовой.- М.: Высш. шк. , 1990, с. 139-143, с. 160-175.
Тестові завдання до теми 4 «Електрохімія»:
1. Використовуючи значення стандартних окислювально-відновних потенціалів напівреакцій відновлення, визначте найсильніший окисник
Cl2+2e=2Cl- φ0=1,36B
HClO+H++2e=Cl-+H2O φ0=1,49B
ClO-+H2O+2e=Cl-+2OH- φ0=0,94B
ClO3- +H++6e=Cl- +3H2O φ0=1,45B
ClO4+8H++8e=Cl- +4H2O φ0=1,38B
2. Метод потенціометричного визначення рН, як найбільш універсальний, занесено в державну фармакопею. За допомогою якої з пар електродів визначають рН?
A. Цинковий - хлорсрібний
B. Мідний - каломельний
C. Мідний - водневий
D. Скляний - нас. каломельний
E. Кисневий - хінгідронний
3. Каломельний електрод внесено в ДФ України, як допоміжний електрод для виміру рН. До якого типу електроду відноситься каломельний електрод?
A. Газовий
B. Першого роду
C. Другого роду
D. Окислювально-відновний
E. Ионселективный
4. Стандатний водневий електрод - це платинова пластина, занурена в розчин кислоти при температурі 298 К і р = 1.013(105 Па з активністю іонів Н3О+) :
1 моль/л
0,5 моль/л
0,1 моль/л
0,2 моль/л
2,0 моль/л
5. Мембранний потенціал, що виникає між внутрішньою і зовнішньою сторонами клітинної мембрани, знаходиться в незбудженому стані, називається
Відновний потенціал
Потенціал спокою
Потенціал дії
Потенціал ушкодження
Стандартний потенціал
6. Амплітуда коливання(деполяризація і реполяризація) мембранного потенціалу, що виникає при збудженні клітини носить назву
Стандартний потенціал
Водневий потенціал
Окислювально-відновний потенціал
Потенціал Донану
Потенціал дії
7. Рівновага, що встановлюється в системі розчинів, розділених мембраною, непроникною хоч би для одного виду іонів, присутніх в системі(у клітинах роль таких непроникаючих іонів виконують іони білків), називається
А. Мембранна рівновага Донану
В. Дифузійна рівновага
С. Седиментаційна рівновага
Д. Седиментаційно-дифузійна рівновага
Е. Динамічна рівновага
8. Потенціал, що виникає на межі розділу двох розчинів, що містять один і той же електроліт різної концентрації, або двох розчинів різних електролітів внаслідок відмінності рухливості їх катіонів і аніонів, називається
Контактний потенціал
Редокс-потенціал
Стандартний відновний потенціал
Дифузійний потенціал
Стандартний окислювальний потенціал
9. Вкажіть редокс-пару, до якої І2/2І- є відновником . Е0 (І2/2І-) = 0, 54 В.
Cl2 → 2 Cl- (E0=1,36B)
SO42- →S0 (E0=0,45B)
Sn2+ → Sn4+ (E0=0,15B)
2S2O32- → S4O62- (E0=0,09B)
2H+ → H2 (E0=0,00B)
Ситуаційні завдання до теми 4 «Електрохімія»:
Завдання1.
Виходячи зі значень стандартних електродних потенціалів напівелементів
а)
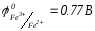

б)
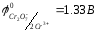
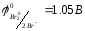
в)
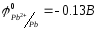
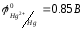
складіть повне іонне рівняння ОВР і розрахуйте зміну вільної енергії Гиббса в реакції та вкажіть, чи можливо здійснити її в гальванічному елементі.
Завдання2.
Запищіть схему, розрахуйте стандартну ЕРС та максимальну роботу гальванічних елементів, складених із напівелементів
а)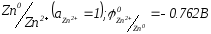

б)
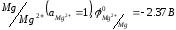
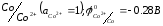
в)