
- •Е.В. Рудковская, г.В. Диденко
- •Предисловие
- •Содержание учебного материала Введение
- •Раздел 1. Физико-химические процессы в гидросфере
- •Раздел 2. Физико-химические процессы в атмосфере
- •Раздел 3. Физико-химические процессы в литосфере
- •Заключение
- •Правила поведения в химической лаборатории
- •Первая медицинская помощь Первая медицинская помощь при ожогах и отравлениях
- •Токсичные вещества
- •Классификация токсичных веществ (ядов)
- •Краткие теоретические сведения
- •1. Стеклянная посуда общего назначения
- •3.Работа с мерной посудой
- •4. Мытье посуды
- •Контрольные вопросы:
- •Правила отбора проб воды. Определение органолептических показателей воды
- •Краткие теоретические сведения
- •Техника отбора пробы
- •Определение основных органолептических показателей воды
- •Классификация запахов естественного происхождения
- •Ход работы с предложенных проб воды определите следующие органолептические показатели׃
- •Оценка интенсивность запаха
- •3)Определение цветности воды.
- •Выполнение измерений температуры
- •6)Определение прозрачности
- •Визуальный способ определения мутности Выполнение анализа
- •Лабораторная работа №3 определение общего солесодержания, взвешенных и растворенных веществ
- •Краткие теоретические сведения
- •3) Общее солесодержание
- •Контрольные вопросы׃
- •Краткие теоретические сведения
- •Фотометрический анализ
- •Основной закон светопоглощения (закон Ламберта-Бугера-Бера)
- •Графическое отображение закона Ламберта-Бугера-Бера
- •Ход выполнения работы:
- •2) Количественный фотоколориметрический метод
- •3) Оформление результатов работы
- •Контрольные вопросы:
- •Лабораторная работа №5 определение фосфатов-ионов в природных и сточных водах
- •Краткие теоретические сведения
- •Ход выполнения работы:
- •1)Построение градуировочного графика
- •2)Выполнение определений:
- •Контрольные вопросы:
- •Лабораторная работа №6
- •Краткие теоретические сведения Строение микроскопа
- •Биоиндикация
- •Биотестирование
- •Ход работы:
- •Масляная иммерсия
- •Водная иммерсия
Фотометрический анализ
Фотометрический анализ является общим названием всех методов, которые основаны на светопоглощении. В основе фотометрического анализа лежит реакция образования (или разрушения) соединений, которые поглощают свет. При образовании соединения, которое поглощает свет, количество продукта реакции пропорционально оптической плотности раствора. А разрушение соединения, которое поглощает свет, характеризуется уменьшением оптической плотности раствора, пропорциональной количеству продукта реакции. Таким образом, измерение оптической плотности раствора продукта реакции дает возможность установить количество вещества, которое вступило в реакцию с реактивом.
Фотометрическое определение состоит из двух стадий׃ образование соединения, которое поглощает свет, и измерение оптической плотности (интенсивности окраски) раствора.
Основной закон светопоглощения (закон Ламберта-Бугера-Бера)
![]() ,
,
где
![]() -оптическая
плотность раствора при определенной
длине волны λ;
-оптическая
плотность раствора при определенной
длине волны λ;
![]() -
коэффициент светопоглощения, величина
постоянная для раствора данного
соединения при прохождения света с
длинной волны λ;
-
коэффициент светопоглощения, величина
постоянная для раствора данного
соединения при прохождения света с
длинной волны λ;
![]() -толщина
исследуемого слоя раствора (длина
кюветы), см;
-толщина
исследуемого слоя раствора (длина
кюветы), см;
![]() -
молярная концентрация раствора, моль/л.
-
молярная концентрация раствора, моль/л.
Физический смысл
![]() ׃
при
׃
при
![]() =1см
и
=1см
и![]() =1моль/л,
тогда
=1моль/л,
тогда![]() =
=![]() .
.
То есть, молярный коэффициент поглощения равен оптической плотности одномолярного раствора при толщине слоя исследуемого раствора (длине кюветы) равной 1см.
![]() характеризирует
внутренние свойства вещества и не
зависит от концентрации, толщины слоя
и интенсивности освещения.
характеризирует
внутренние свойства вещества и не
зависит от концентрации, толщины слоя
и интенсивности освещения.
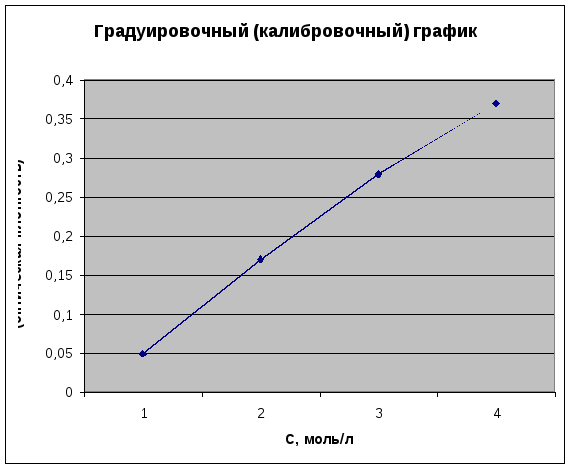
Графическое отображение закона Ламберта-Бугера-Бера
Зависимость оптической плотности (светопоглощения) от концентрации веществ в растворе принято изображать графически. На оси абсцисс откладывают значения концентрации, а на оси ординат – соответственно значения оптической плотности. Соответственно основному закону фотометрии на графике получаем прямую линию, которая проходит через начало координат.
Ход выполнения работы:
1) Визуальный метод определения наличия аммиака в пробе (качественное определение)
В пробирку наливают 10 cм3 воды, которую анализируют. Прибавляют пару капель 50%-ного раствора сегнетовой соли, это предотвращает появление белого осадка гидроксида магния, который мешает анализу (ионы магния всегда содержатся в воде в небольших количествах). Добавляют (пару капель) реактива Несслера. Ставят пробирку в штатив на 10 минут. По данным таблицы определяют содержание аммиака в воде.
Табл. 2 Шкала для определения содержания аммиака в воде
|
Окраска при осмотре |
Массовая концентрация аммиака, мг/дм3 |
Окраска при осмотре |
Массовая концентрация аммиака, мг/дм3 | ||
|
сбоку |
сверху |
сбоку |
сверху | ||
|
Нет |
Нет |
0,05 |
Светло-желтая |
Светло-желтая |
1,0 |
|
Нет |
Еле заметная |
0,1 |
Светло-желтая |
Желтая |
>2,0 |
|
Еле заметная |
Светло-желтая |
0,2 |
Желтая |
Интенсивно желто-бурая |
4,0 |
|
Светло-желтая |
Желтоватая |
0,4 |
- |
- |
- |
