
МДФд_27
.pdf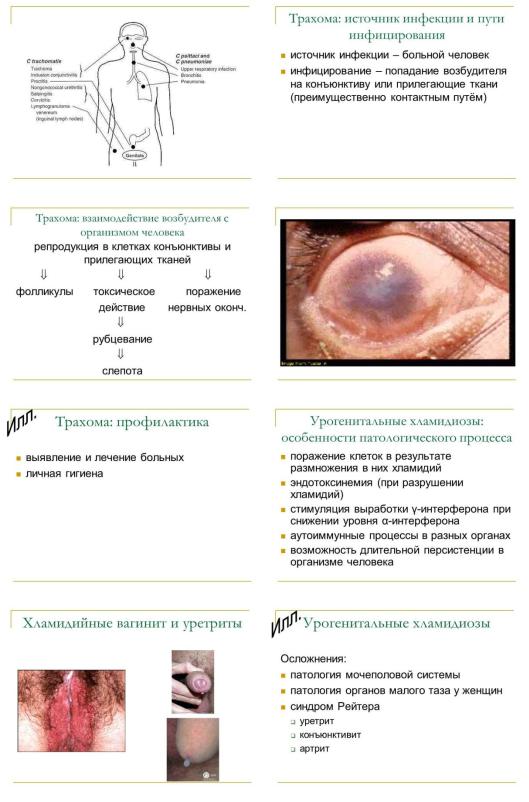
МДФд. Занятие № 27 |
- 11 - |
|
|
|
|
|
|
|
|

МДФд. Занятие № 27 |
- 12 - |
|
|
|
|
|
|
|
|

МДФд. Занятие № 27 |
- 13 - |
|
|
|
|
|
|
|
|

МДФд. Занятие № 27 |
- 14 - |
|
|
|
|
|
|
|
|

МДФд. Занятие № 27 |
- 15 - |
|
|
|
|
|
|
|
|

МДФд. Занятие № 27 |
- 16 - |
|
|
|
|
|
|
|
МДФд-27В. Теоретический материал
БАКТЕРИИ – ОБЛИГАТНЫЕ ВНУТРИКЛЕТОЧНЫЕ ПАРАЗИТЫ
К этой экологической группе относятся представители двух порядков: Rickettsiales и Chlamydiales (риккетсии и хламидии).
Патогенные для человека риккетсии относятся к родам Rickettsia и Orientia, входящих в семейство Rickettsiaceae, и к роду Erlichia, входящему в одноименное семейство Erlichiaceae.
Патогенные для человека хламидии относятся к родам Chlamydia и Clamydophila, входящим в семейство Clamydiaceae.
РИККЕТСИИ И РИККЕТСИОЗЫ
Риккетсии, как патогенные для человека бактерии, были открыты американским микробиологом Риккетсом в 1909 году, когда он открыл возбудителя пятнистой лихорадки Скалистых гор. Именно в честь Риккетса эти бактерии и получили свое название.
Представляют собой грамотрицательные полиморфные палочки, окрашивающиеся по Ро- мановскому-Гимзе в синий, а по Здрадовскому – в красный цвет (в обеих случаях на фоне голубой цитоплазмы или синего ядра клетки-хозяина).
Риккетсии предаются членистоногими (вшами, блохами, клещами) и поражают эндотелий сосудов, клетки крови, гладкомышечные клетки.
Выделяют четыре морфологических типа риккетсий: тип а, трип b, трип c и трип d. Типа а – коккобактерии – является основным морфологическим типом риккетсий.
Тип b представляет собой палочковидные двузернистые формы размером от 1,0 до 1,5 мкм. Тип с – переходные к типу d формы: удлиненные, могут быть изогнутыми, двузернистые,
размером 3-4 мкм.
К типу d относятся нитевидные многозернистые формы, представляющие собой мицелий, состоящий из а- и b-клеток.
Основной причиной исключительно внутриклеточного размножения риккетсий является их неспособность синтезировать НАД. Поэтому, риккетсии вынуждены «брать» НАД непосредственно у клетки-хозяина, для чего им необходимо находиться внутри этой клетки. Осуществлять окис- лительно-восстановительные реакции своего метаболизма вне клетки-хозяина для риккетсий совершенно невозможно.
Для риккетсий характерна низкая устойчивость во внешней среде. Из химиотерапевтических веществ они наиболее чувствительны к тетрациклинам.
МДФд. Занятие № 27 |
- 17 - |
Риккетсии обладают особым токсическим веществом, которое неотделимо от бактериальной клетки и проявляет свое действие лишь при жизни микроорганизма. Это токсическое вещество представляет собой термолабильный белок, который при внутривенном введении белой мыши вызывает у нее острую интоксикацию и гибель в течение 2-24 часов. У людей этот белок индуцирует появление специфических антител, которые можно выявить в реакции нейтрализации на белых мышах.
Кдругим факторам патогенности риккетсий относятся гемолизины, эндотоксин и неидентифицированные факторы адгезии и инвазии.
Патогенные для человека виды рода Rickettsia классифицируются на две группы: сыпного тифа и клещевых пятнистых лихорадок. Все виды одной группы имеют общий антиген.
Кгруппе сыпного тифа относятся R. prowazekii и R. typhi. Эти риккетсии располагаются только в цитоплазме клетки-хозяина, не поражая ее ядро.
R. prowazekii вызывает эпидемический сыпной тиф – антропоноз, переносчиком которого служит вошь.
R. typhi – этиологический фактор эндемического (крысиного) сыпного тифа. Источник этого заболевания – крысы и мыши, переносчики – крысиные блохи и крысиная вошь.
Кгруппе клещевых пятнистых лихорадок относятся R. rickettsii, R. conorii, R. australis, R. sibirica и R.akari. Эти риккетсии располагаются и в цитоплазме и в ядре клетки-хозяина.
R. rickettsii является возбудителем лихорадки Скалистых гор. Источник этого заболевания – грызуны, переносчики – иксодовые клещи.
R. conorii является возбудителем марсельской (средиземноморской) лихорадки. Источник этого заболевания – собаки, переносчик – собачий клещ.
R. australis является возбудителем северо-австралийского клещевого сыпного тифа (североавстралийского клещевого риккетсиоза). Источник этого заболевания – грызуны, переносчики – иксодовые клещи.
R. sibirica является возбудителем североазиатского риккетсиоза. Источник этого заболевания – грызуны, переносчики – иксодовые клещи.
R. akari является возбудителем везикулезного (осповидного) риккетсиоза. Источник этого заболевания – мыши и крысы, переносчики – гамазовые клещи.
ЭПИДЕМИЧЕСКИЙ СЫПНОЙ ТИФ
Эпидемический сыпной тиф не имеет четко очерченного природного ареала распространения и его возникновение возможно в любой местности. Как риск возникновения, так и заболеваемость этой инфекцией тесно связана с педикулезом. В Европе во время первой мировой войны потери действующих армий от риккетсиозов (прежде всего – сыпного тифа) превышали боевые потери. Самая крупная эпидемия сыпного тифа была в России в 1914 – 1922 годах, когда сыпняком переболело 25 миллионов человек, из которых 3 миллиона умерло. Смертность при эпидемическом сыпном тифе в доантибиотиковую эру доходила до 80%.
Возбудитель эпидемического сыпного тифа – R. prowazekii – открыт Провацеком в 1913 г. Сам Провацек погиб от выделенной им культуры в результате внутрилабораторного заражения.
Вклетке-хозяине R. prowazekii образует капсулу. Других морфологических отличий от остальных риккетсий у нее нет.
R. prowazekii, как и все представители рода Rickettsia имеет два антигена. Группоспецифический (у R. prowazekii – общий с R. typhi) антиген отделяется от бактери-
альной клетки при обработке эфиром, поэтому определяется как растворимый антиген. Представляет собой термостабильный липидо-полисахаридо-протеиновый комплекс. Является протективным антигеном.
Видоспецифический антиген не отделяется от бактериальной клетки, поэтому определяется как корпускулярный антиген. В отличие от растворимого антигена, термолабилен.
Заражение эпидемическим сыпным тифом происходит при втирании фекалий инфицированной вши. R. prowazekii проникает в кровь и адгезируется на холинсодержащих рецепторах эндотелия прекапилляров и макрофагов.Развивающаясятоксинемия обуславливает интоксикацию организма, а размножение возбудителя в эндотелии капилляров – формирование своеобразной «муфточки». В результате развивается характерный для всех риккетсиозов специфический диффузный гранулематоз, приводящий к тромбозу прекапилляров. Клинические это проявляется головной болью и развитием менингоэнцефалита (поражение ЦНС), сыпью (поражение кожи), развитием миокардита (поражение сердечной мышцы) и гломерулонефрита (поражение почек).
Вобычных лабораториях для микробиологической диагностики эпидемического сыпного тифа используется серологический метод. С помощью РА, РСК, РНГА, ИФА, РИФ выявляют специфические антитела, при этом реакция агглютинации положительна в срок до 3-5 месяцев после болезни, в то время как реакция связывания комплемента сохраняется положительной многие го-
МДФд. Занятие № 27 |
- 18 - |
ды после перенесенного заболевания.
В специализированных лабораториях из крови больного выделяют культуру возбудителя. Для этого или заражают в желточный мешок куриный эмбрион (идентификацию выросшей культуры осуществляют с помощью ИФА) или внутрибрюшинно заражают морскую свинку, которую впоследствии забивают, готовят гистологические препараты из ткани головного мозга, в которых при положительном результате регистрируют картину специфического гранулематоза. При этом орхит (для заражения используются именно самцы), в отличие от других видов риккетсий, R. prowazekii у морской свинки не вызывает.
Возбудитель эпидемического сыпного тифа после перенесенного заболевания сохраняется в макрофагах и может реактивироваться через 10-20 и более лет. Такой поздний рецидив эпидемического сыпного тифа носит название болезни Брилля-Цинссера.
Со «свежим» эпидемическим сыпном тифом болезнь Брилля-Цинссера дифференцируется серологическим методом. Сравнивают титр специфических антител в нативной сыворотке крови пациента и в ней же, но после обработки 2-меркаптоэтанолом. Если титр одинаковый, то это значит, что специфические антитела представлены IgG, если после обработки 2-меркаптоэтанолом титр антител к R. prowazekii снижается, это значит, что они представлены IgM. В первом случае – у больного болезнь Брилля, во втором – «свежий» случай сыпного тифа. Эту же задачу можно решить, применив ИФА, которая позволяет определить принадлежность выявленных иммуноглобулинов или к классу G или к классу М.
ЭНДЕМИЧЕСКИЙ СЫПНОЙ ТИФ
Эндемический сыпной тиф распространен повсеместно, в основном – в портовых городах Северного, Балтийского, Средиземного, Каспийского и Черного морей. Наиболее часто он встречается в портах «южных» морей Америки, Африки, Дальнего Востока и Северной Австралии.
Возбудитель эндемического сыпного тифа – R. typhi – морфологически схожа с R. prowazekii. Имея с ней общий растворимый, термостабильный, антиген, R. typhi отличается от возбудителя эпидемического сыпного тифа своим корпускулярным, термолабильным, антигеном (как и у других риккетсий, этот антиген у R. typhiвидоспецифический).
R. typhi обладает токсином, который тесно связан с бактериальной клеткой и по своей антигенной структуре отличается от токсина риккетсий Провацека.
Условия инфицирования при сыпных тифах схожи, но в очагах эндемического сыпного тифа возможно участие в передаче инфекции человеческих блох и вшей, алиментарный путь инфицирования (через пищевые продукты, загрязненные мочой грызунов), аэрогенный путь инфицирования (при попадании фекалий блох на слизистую оболочку верхних дыхательных путей), а также инфицирование при укусе крысиного клеща.
Дифференциальный диагноз между эпидемическим и эндемическим сыпным тифом проводят микробиологическими методами: или серологическим или биологическим.
В первом случае ставят параллельные реакции с корпускулярными антигенами обеих возбудителей. Если титр реакции с корпускулярным антигеном R. prowazekii выше, чем реакции с корпускулярным антигеном R. typhi, то у пациента эпидемический сыпной тиф, если наоборот, то
– эндемический.
При биологическом методе кровью больного внутрибрюшинно заражают самца морской свинки. Наличие у лабораторного животного скротального феномена говорит о том, что в крови пациента содержатся R. typhi (соответственно, у пациента – эндемический сыпной тиф). Отсутствие скротального феномена свидетельствует в пользу эпидемического сыпного тифа.
ОРИЕНЦИИ
Патогенный для человека вид – Orientiatsutsugamushi. Это мелкие грамотрицательные бактерии, присутствующие только в цитоплазме (но не в ядре) зараженной клетки. Вызывают лихорадку цуцугамуши, передающуюся человеку от грызунов краснотелковыми клещами.
ЭРЛИХИИ
Эрлихии (Erlichia) – мелкие грамотрицательные кокковидные бактерии. Размножаются в цитоплазматических вакуолях лейкоцитов, формируя микроколонии (цитоплазматические включения), называемые «морулами»; внешне они похожи на ягоды малины.
У человека эрлихии вызывают эрлихиозы – заболевания, сопровождающиеся лихорадкой, сыпью, миалгией, лейко- и тромбоцитопенией.
МДФд. Занятие № 27 |
- 19 - |
ХЛАМИДИИ
Морфологически и функционально хламидии представлены двумя основными формами: элементарными и ретикулярными тельцами.
Элементарные тельца хламидий – очень мелкие клетки (0,15 – 0,2 мкм), полиморфны, хотя преимущественно представлены кокковым формами. Геном хламидий составляет всего лишь ¼ генома кишечной палочки. Метаболическималоактивны, так как адаптированы к внеклеточному существованию. При проникновении в эукариотическую клетку подавляют в ней фагосомолизосомальное слияние.
Ретикулярные тельца – более крупные (до 1 мкм). Развиваются из элементарных телец в течение 5 – 6 часов. Содержат большое количество рибосом и генофора.
Ретикулярные тельца размножаются бинарным делением, их конденсация в клетке-хозяине сопровождается переходом их в промежуточные тельца (при микроскопии напоминающие бычий глаз), которые, в свою очередь преобразуются в новые элементарные тельца, выходящие из инфицированной клетки посредством ее лизиса (т.е. размножение хламидий приводит к гибели клеткихозяина).
Хламидии проникают в клетку путем инвагинации места адсорбции элементарного тельца. В цитоплазмы клетки появляется эндоцитозный пузырек, внутри которого и размножаются ретикулярные тельца с последующими превращениями в промежуточные и, наконец, в новые элементарные. В результате эндоцитозный пузырек, буквально набитый ретикулярными, промежуточными и элементарными тельцами, окруженными общей оболочкой (производной от клеточной оболочки) при микроскопии выглядит (и, собственно, является) цитоплазматическим включением.
Chlamydia формирует в пораженной клетке одно большое внутриклеточное включение, в котором накапливается гликоген, вследствие чего такое включение можно выявить с помощью раствора Люголя. Chlamydophila образует много мелких включений, располагающихся вокруг ядра клетки-хозяина.
Из рода Chlamydia ведущую роль в патологии человека играет вид C. trachomatis, который по биологическим свойствам классифицируется на два биовара, а по белкам наружной мембраны – на серовары.
Серовары от А до К объединены в биоварtrachoma. При этом серовары А – С вызывают трахому, а серовары D – K являются этиологическим фактором урогенитального хламидиоза (негонококковых уретритов и слизисто-гнойных цервицитов, при которых в пораженных клетках обнаруживаются цитоплазматические включения), а также пневмонии и конъюнктивита у новорожденных (так называемой бленнореи с включениями).
Серовары L1 – L3, объединенные в биовар LGV, вызывают паховый грануломатоз (венерическую лимфогранулему).
Род Chlamydophila включает в себя два патогенных для человека вида: C. psittaci и C. pneumonia. Вид Chlamydophilapsittaci, содержащий 8 сероваров, вызывает орнитоз, серологически однородный вид Chlamydophilapneumonia – бронхомневмонию, а также создает условия для образования на внутренней стенке кровеносного сосуда атеросклеротической бляшки.
ТРАХОМА
Источник инфекции при трахоме – больной человек. Инфицирование происходит при попадании возбудителя на конъюнктиву или прилегающие к ней ткани (преимущественно контактным путем).
Репродукция C. trachomatis в клетках конъюнктивы и прилегающих к ней тканей сопровождается поражением нервных окончаний, а главное –образованием фолликул, которые в результате токсического действия бактерий рубцуются, что приводит к слепоте.
Профилактика трахомы заключается в выявлении и лечении больных и соблюдении правил личной гигиены.
УРОГЕНИТАЛЬНЫЕ ХЛАМИДИОЗЫ
При урогенитальных хламидиозах в организме больного человека не только наблюдается поражение клеток в результате размножения в них хламидий, но и развивается эндотоксинемия (как результат разрушения хламидий), стимулируется выработка гамма-интерферона при снижении уровня альфа-интерферона и формируются аутоиммунные процессы в различных органах и тканях. Кроме перечисленных особенностей патологического процесса при урогенитальных хламидиозах, следует учитывать возможность длительной персистенции хламидий в организме человека, что тоже привносит свои особенности в патогенез данной инфекции.
МДФд. Занятие № 27 |
- 20 - |
В случае отсутствия лечения или его неадекватности, развиваются такие осложнения, как патология мочеполовой системы, патология органов малого таза у женщин, синдром Рейтера (сочетания уретрита, конъюнктивита и артрита).
Для профилактики хламидийных конъюнктивитов осуществляют комплекс мер. Всем новорожденным местно, т.е. в конъюнктиву (девочкам – и в половую щель) вводят раствор нитрата серебра, или, реже, раствор антибиотика (эритромицина или тетрациклина). У беременных целенаправленно проводят выявление и лечение урогенитального хламидиоза, особенно тщательно проводят диагностическое тестирование женщин из групп риска. Матери детей, больных конъюнктивитом с включениями или хламидийной пневмонией, равно как и их сексуальные партнеры, в обязательном порядке подлежат лечению.
ВЕНЕРИЧЕСКАЯ ЛИМФОГРАНУЛЕМА
Инфицирование при этой инфекции происходит половым путем. Местно, т.е. в районе половых органов, формируется очаг первичного поражения: везикула, преходящая в папулу, а позже
– в эрозию. Через несколько дней происходит заживление этого очага, однако, спустя 2 – 6 недель появляется миалгия, чувство слабости и разбитости, возможно развитие лихорадочной реакции. В результате поражения региональных лимфатических узлов формируется струмозный бубон. Позже кожа над ним лопается и выделяется зеленовато-желтый гной. При заживлении формируется рубец. К отдаленным последствиям венерической лимфогранулемы относятся развитие папиллом, асцессов, язв, слоновости в области гениталий.
ОРНИТОЗ
Chlamydophilapsittaci попадает в организм человека через дыхательные пути. Здесь она захватывается макрофагами, которые разносят возбудитель по организму. Возбудитель орнитоза размножается в клетках печени (как следствие у пациента наблюдается увеличение печени, а у каждого третьего – и нарушение ее функции), а также в селезенке. Далее Chlamydophilapsittaci вновь попадает в кровь, а с ней – в легкие (здесь образуются некротические гранулемы и геморрагии), лимфоузлы (персистенция в которых обуславливает рецидивирующий характер заболевания) и другие органы (миокард, перикард, надпочечники, головной мозг), поражение которых может вызвать летальный исход.
МИКРОБИОЛОГИЧЕСКАЯ ДИАГНОСТИКА ХЛАМИДИЙНЫХ ИНФЕКЦИЙ
Методы, применяемые для микробиологической диагностики хламидийных инфекций зависят от конкретного заболевания.
При орнитозе в первые 2 – 3 недели можно выделить возбудителя из крови, путем введения ее в организм белой мыши или желточный мешок куриного эмбриона, в клетках тканей которых возбудитель обнаруживается и идентифицируется с помощью РИФ или ИФА. Более распространены серологический (выявление специфических антител в сыворотке крови с помощью РСК, РТГА, ИФА) и аллергический (выявление ГЗТ кожно-аллергической пробой) методы.
Микробиологическая диагностика пахового лимфогранулематоза заключается в обнаружении инфицированных клеток в содержимом (пунктате) пораженного лимфатического узла. Это можно сделать или микроскопическим путем или путем заражения патологическим материалом культуры клеток для размножения в ней возбудителя. В обоих случаях обнаружение и идентификация возбудителя проводится как при орнитозе – с помощью РИФ или ИФА.
Микробиологическая диагностика других хламидиозов проводится путем микроскопии мазка из патологического материала, в котором обнаруживаются цитоплазматические включения, сформированные Chlamydiatrachomatis, или возбудитель, обнаружение и идентификация которого осуществляется с помощью РИФ или ИФА.
РЕСПИРАТОРНАЯ ПАТОЛОГИЯ ХЛАМИДИЙНОЙ ПРИРОДЫ
Респираторную патологию вызывают все три рассмотренные выше вида хламидий. Chlamydiatrachomatis вызывает пневмонию новорожденных, пневмонию у грудных детей с
иммунодефицитом, а также пневмонию у взрослых (также на фоне иммунодефицита). Chlamydophilapsittaci вызывает орнитоз, который клинически протекает прежде всего имен-
но как пневмония.
