
- •Российский химико-технологический университет
- •I. Введение.
- •II. Схема эхтс.
- •III.3. Баланс энергии. Исследование политропного процесса.
- •III.4. Эксергетический анализ.
- •IV. Горение топлива.
- •IV.1. Материальный баланс.
- •IV.2. Энергетический (энтальпийный) баланс.
- •IV.3. Эксергетический анализ.
- •V. Расчет химического реактора.
- •V.1. Энергетический баланс. Определение расхода топлива.
- •V.2. Эксергетический анализ.
- •VI. Процесс теплообмена
- •VI. 1. Эксергетический анализ.
- •VII. Расчет турбокомпрессора.
- •VII.1. Определение механической мощности турбокомпрессора.
- •VII.2. Определение расхода воды.
- •VII.3. Графическое представление процесса сжатия в турбокомпрессоре.
- •VIII. Паросиловой цикл Ренкина.
- •VIII.1. Аналитический расчет цикла.
- •VIII.2. Определение механической мощности цикла.
- •XI. Список литературы.
IV.3. Эксергетический анализ.
Эксергетический
КПД адиабатного горения:
 ;
;
T1=T0=298,15K ; T2=Tтеор.ад.гор.=2218К (см. IV.2) ; P1=P2=P°=1атм
![]() (см.
V.2)
(см.
V.2)
Для сечения 2-2 эксергии компонентов определяем по формуле:
![]()
(вывод формулы – см. V.2)

Мольные
доли компонентов:
![]()
![]() (x
и y
для T=T2
см. IV.2)
(x
и y
для T=T2
см. IV.2)
Эксергии компонентов:
|
Компонент |
|
|
|
|
|
|
|
CO2 |
20,10 |
32,20 |
0,022 |
0,103 |
97,6 |
1,941 |
|
CO |
275,4 |
28,40 |
0,004 |
0,00310 |
306 |
0,059 |
|
O2 |
3,95 |
31,50 |
0,003 |
0,00896 |
39,4 |
0,169 |
|
H2O |
8,60 |
32,30 |
0,002 |
0,155 |
50,4 |
2,927 |
|
OH |
157 |
29,0 |
0,060 |
0,00386 |
292 |
0,073 |
|
H2 |
235,3 |
27,3 |
0,00335 |
0,00193 |
262 |
0,036 |
|
N2 |
0,70 |
27,90 |
0,004 |
0,724 |
44,2 |
13,69 |
![]()
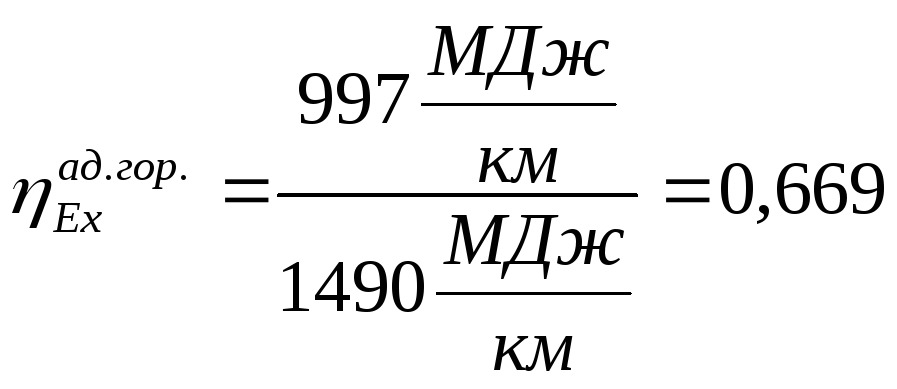
V. Расчет химического реактора.
V.1. Энергетический баланс. Определение расхода топлива.
Допущения:
Вся тепловая мощность, полученная при охлаждении топочных газов от температуры адиабатного горения до температуры T2=1835К, передается смеси метана и воды.
Диссоциацией продуктов сгорания при T2 можно пренебречь.
Энергетический
баланс:
![]()
![]() (см.
IV.2)
(см.
IV.2)
![]() (см.
IV.2)
(см.
IV.2)
![]()
![]() (см.
III.2)
(см.
III.2)
Расход топлива равен

V.2. Эксергетический анализ.
Эксергетический КПД химического реактора определяется из соотношения:

Зависимость эксергии компонента от температуры и парциального давления выражается соотношением:

Сечение 1-1:
T1=Toc=T0=298,15K ; P1= Pº=1 атм
![]()
Эксергии компонентов:
|
Компонент |
|
|
|
|
|
CH4 |
830,0 |
0,5 |
828,3 |
0,5 |
|
С3H8 |
2149,0 |
0,5 |
2147,3 |
0,5 |
|
O2 |
3,95 |
0,21 |
0,08 |
Эксергиями компонентов воздуха пренебрегаем |
|
N2 |
0,70 |
0,79 |
0,12 |
![]()
Сечение 2-2:
T2=1835К ; P2= Pº=1 атм

Эксергии компонентов:
|
Компонент |
|
|
|
|
|
|
|
CO2 |
20,10 |
32,20 |
0,022 |
0,106 |
72,57 |
2 |
|
O2 |
3,95 |
31,50 |
0,003 |
0,00743 |
26,70 |
0,14 |
|
H2O |
8,60 |
32,30 |
0,002 |
0,159 |
38,55 |
3 |
|
N2 |
0,70 |
27,90 |
0,004 |
0,727 |
32,40 |
13,69 |
![]()
Сечение 8-8:
T8=573K ; P8=3,79МПа (III.3)

Эксергии компонентов:
|
Компонент |
|
|
|
|
|
|
|
CH4 |
830,0 |
14,32 |
0,075 |
0,25 |
839,5 |
0,446 |
|
H2O |
8,60 |
32,30 |
0,002 |
0,75 |
19,50 |
1,338 |
![]()
Сечение 9-9:
T9=1123K ; P8=2,9МПа

Эксергии компонентов:
|
Компонент |
|
|
|
|
|
|
|
CH4 |
830,0 |
14,32 |
0,075 |
0,0337 |
861,6 |
0,0847 |
|
H2O |
8,60 |
32,30 |
0,002 |
0,362 |
28,95 |
0,910 |
|
H2 |
235,0 |
27,3 |
0,00335 |
0,458 |
254,2 |
1,150 |
|
CO2 |
20,10 |
32,20 |
0,022 |
0,0267 |
40,75 |
0,067 |
|
CO |
275,4 |
28,40 |
0,004 |
0,117 |
292,0 |
0,294 |
![]()
Эксергетический КПД химического реактора:

