
Содержание
[убрать]
1Исторические описания
2Этиология и факторы риска
2.1Основные факторы риска
3Классификация TNM
3.1Т – первичная опухоль:
3.2N – регионарные лимфатические узлы:
3.3М – отдаленные метастазы:
4Гистологические типы РМЖ
5Молекулярная таксономия РМЖ
6Симптомы
7Диагностика
7.1Самостоятельное обследование молочных желёз
7.2Сигналы тревоги
8Дифференциальная диагностика
9Принципы лечения
10Виды оперативных вмешательств
10.1Органосохраняющие операции
10.2Радикальные операции
11Профилактика
12Психологические аспекты заболевания
13См. также
14Примечания
15Литература
16Ссылки
Исторические описания[править | править вики-текст]
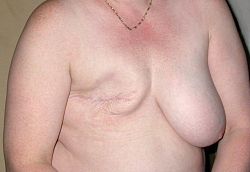
Женская грудь после мастэктомии
Рак молочной железы является одной из самых изученных и изучаемых форм рака. Древнейшее из известных описаний рака молочной железы (хотя сам термин «рак» ещё не был известен и не использовался) было найдено в Египте и датируется примерно 1600 годом до н. э. Так называемый «Папирус Эдвина Смита» описывает 8 случаев опухолей или изъязвлений молочной железы, которые были подвергнуты лечению прижиганием огнём. Текст гласит: «От этой болезни нет лечения; она всегда приводит к смерти».
В течение многих столетий врачи описывали подобные случаи в своей практике с тем же печальным заключением. Никаких сдвигов в лечении рака молочной железы не происходило до тех пор, пока в XVII веке врачи не добились лучшего понимания работы кровеносной и лимфатической систем организма и не смогли понять, что рак молочной железы распространяется (метастазирует) по лимфатическим путям и в первую очередь поражает ближайшие — подмышечные — лимфатические узлы. Французский хирург Жан-Луи Пети(1674—1750) и вскоре после него шотландский хирург Бенджамин Белл[en] (1749—1806) были первыми, кто догадался удалять при раке молочной железы не только саму молочную железу, но и ближайшие лимфатические узлы и подлежащую грудную мышцу. Их успешная работа была подхвачена Уильямом Стюартом Холстедом[en] (1852—1922), который в 1882 году ввёл в широкую медицинскую практику технически усовершенствованный вариант этой операции, которую он назвал «радикальной мастэктомией». Операция стала настолько популярной при раке молочной железы, что даже получила название по имени её изобретателя — «мастэктомия Холстеда» или «мастэктомия по Холстеду».
Этиология и факторы риска[править | править вики-текст]
Вопросы этиологии рака молочной железы в настоящее время исследованы недостаточно. В отличие от рака лёгкого или рака мочевого пузыря, ни один изканцерогенов окружающей среды не удаётся убедительно связать с провокацией рака молочной железы[4].
В ряде случаев рак молочной железы предстаёт как классическое наследственное заболевание. Наиболее выраженными генетическими факторами предрасположенности к раку молочной железы исследователи считают гены BRCA1[en] (№ NM_007294 в базе данных GenBank) и BRCA2[en] (№ NM_007294 в GenBank); вклад наследственных мутаций в этих генах в частоту наследственный заболеваний раком молочной железы — около 20 %. Подобную роль играют и гены ATM, TP53 (ген белка p53), PTEN[6].
В настоящее время исследована экспрессия различных генов в опухолях молочной железы и выделены различные молекулярные типы опухоли. Клинически, они имеют существенно различный риск развития метастазов и требуют различной терапии. Коллекция данных[7] по экспрессии 17 816 генов в опухолях молочной железы доступна онлайн[8] и используется не только для медико-биологических исследований, но и как ставший классическим тестовый пример для визуализации и картографии данных.
Основные факторы риска[править | править вики-текст]
Факторы риска развития рака молочной железы[9]:
отсутствие в анамнезе беременностей и родов;
курение (особенно, если оно начато в юном возрасте);
раннее менархе (до 12 лет);
поздняя менопауза (после 55 лет);
отягощенный семейный анамнез (онкозаболевания у кровных родственников);
больные, леченные по поводу рака женских половых органов;
ожирение[10];
сахарный диабет;
гипертоническая болезнь;
злоупотребление алкоголем;
употребление экзогенных гормонов — при непрерывном употреблении экзогенных гормонов с целью контрацепции или лечения — более 10 лет.
По результатам недавних исследований Калифорнийского университета в Беркли (University of California-Berkeley) 239 женщин, удалось выявить дополнительный фактор риска рака молочной железы, которым оказался вирус лейкоза коров (BLV) (англ.)русск.. Исследователями допускается, что наличие в организме человека этого вируса связано с риском рака молочной железы больше, чем традиционные факторы риска: ожирение, употребление алкоголя и прием гормональных препаратов в постменопаузе. На данный момент доказана лишь связь между раком молочной железы и присутствием BLV в организме. Является ли вирус причиной развития опухоли, неизвестно. [11][12]
В исследованиях института Гарвана в Австралии обнаружено, что развитию метастазов опухоли молочной железы и прогрессированию рака способствует белок ELF5 (англ.)русск..[13]
Симптомы рака молочной железы на ранних стадиях заболевания могут отсутствовать или характеризоваться появлением в молочной железе небольших малочувствительных подвижных масс. Рост опухоли сопровождается нарушением её подвижности, фиксацией, розоватыми или оранжевыми выделениями из соска.
Классификация TNM[править | править вики-текст]
Т – первичная опухоль:[править | править вики-текст]
ТХ – первичная опухоль недоступна оценке;
Т0 – нет признаков первичной опухоли;
Tis – рак in situ:
Тis (DCIS) – протоковая карцинома in situ;
Тis (LCIS) – дольковая карцинома in situ;
Тis (Paget) – болезнь Педжета соска, не связанная с инвазивной карциномой в подлежащей паренхиме молочной.
Т1 – опухоль до 2 см.
Т2 – опухоль от 2 см до 5 см.
Т3 – опухоль более 5 см;
Т4 – опухоль любого размера с распространением на грудную стенку, кожу (изъязвление или узелки на коже)
N – регионарные лимфатические узлы:[править | править вики-текст]
NХ – регионарные лимфатические узлы не могут быть оценены.
N0 – нет метастазов в регионарных лимфатических узлах;
N1 – метастазы в подмышечных лимфатических узлах I, II уровня не спаянные между собой
N2 –а) метастазы в подмышечных лимфатических узлах I, II уровня спаянные между собой; b) клинически определяемый внутренний маммарный лимфатический узел при отсутствии клинических признаков метастазов в подмышечных лимфатических узлах;
N3 – а) метастазы в подключичных лимфатических узлах III уровня; b) метастазы во внутренних маммарных и подмышечных лимфатических узлах; метастазы в надключичных лимфатических узлах.
М – отдаленные метастазы:[править | править вики-текст]
М0 – отдаленные метастазы не определяются;
М1 – имеются отдаленные метастазы.
Гистологические типы РМЖ[править | править вики-текст]
В гистологическом плане среди раковых опухолей молочной железы выделяют следующие типы[14]:
Внутрипротоковый рак in situ
Дольковый рак in situ
Инвазивный протоковый рак
Инвазивный дольковый рак
Рак молочной железы с признаками воспаления
Тубулярная карцинома
Медуллярный рак
Коллоидный рак (слизистый рак, перстневидно-клеточный рак)
Папиллярный рак
Метапластический рак (плоскоклеточный рак)
Рак с остеокластоподобными клетками
Аденоид-кистозный рак
Секреторная карцинома (ювенильный рак)
Кистозная гипертсекреторная карцинома
Апокринный рак
Рак с признаками эндокринного новообразования (первичная карциноидная опухоль, апудома)
Криброзный рак
Молекулярная таксономия РМЖ[править | править вики-текст]
В последние годы развивается молекулярная таксономия рака молочной железы, позволившая выделить в рамках данного заболевания четыре основных молекулярных подтипа. Эти подтипы отличаются друг от друга характерными наборами молекулярных маркеров и фактически представляют собой разные болезни — с различной этиологией, молекулярным патогенезом и прогнозом, требующие специфических терапевтических подходов. Указанные подтипы опухолей различаются, во-первых, тем, какие цитокератины в них экспрессируются (базальные или люминальные), а во-вторых — наличием или отсутствием амплификации гена HER2. Приведём перечень этих подтипов (указывая в скобках частоту, с которой они встречаются)[15]:
Люминальный подтип A (30—45 %): эстроген-зависимые малоагрессивные опухоли, избытка экспрессии рецепторов белка HER2 нет, наилучший прогноз;
Люминальный подтип B (14—18 %): эстроген-зависимые агрессивные опухоли, выражена амплификация онкогена HER2, значительно худший прогноз;
HER2-позитивный подтип (8—15 %): эстроген-независимые агрессивные опухоли, выражена амплификация онкогена HER2, повышенная вероятность негативного исхода заболевания;
Базальный подтип (27—39 %): эстроген-независимые агрессивные опухоли, избытка экспрессии рецепторов белка HER2 нет, наихудшие показатели выживаемости.
Симптомы[править | править вики-текст]
Рак молочной железы на ранних стадиях (1-й и 2-й) протекает бессимптомно и не причиняет боли. Могут иметь место очень болезненные месячные, боли в молочных железах при мастопатии. Обычно рак молочной железы обнаруживают до явного появления непосредственных симптомов опухоли — либо на маммографии, либо женщина чувствует появление уплотнения в груди. Любое новообразование необходимо пунктировать для выявления раковых клеток. Наиболее точная диагностика происходит по результатам трепан-биопсии под контролем УЗИ. Много случаев диагностики болезни лишь на 3-й и 4-й стадиях, когда опухоль уже видна невооружённым глазом, имеет вид язвы или большой шишки. Может появиться не исчезающее в течение менструального цикла уплотнение в подмышечной ямке или над ключицей: эти симптомы свидетельствуют о поражении лимфоузлов, т.е. метастазах в лимфоузлы, явно выражающихся уже на поздних стадиях.
Прочие симптомы поздних (III-IV) стадий :
Прозрачные или кровянистые выделения из груди
Втяжение соска в связи с прорастанием опухоли в кожу
Изменение цвета или структуры кожи груди в связи с прорастанием опухоли в кожу [источник не указан 1665 дней].
Диагностика[править | править вики-текст]
Регулярное посещение врача-маммолога — специалиста в области заболеваний молочных желез (не реже одного раза в 1—2 года). Всем женщинам старше 20 лет ранее рекомендовалось ежемесячно проводить самостоятельное обследование молочной железы. Женщинам старше 40—50 лет необходимо каждые 1—2 года (даже при отсутствии жалоб) проводить маммографические обследования[16][17].
Женщинам любого возраста с выявленными заболеваниями молочных желёз показана маммография с целью дифференциальной диагностики с использованием ультразвуковых, патоморфологических методик, в том числе интервенционной радиологии.
Самостоятельное обследование молочных желёз[править | править вики-текст]
Основная статья: самостоятельное обследование молочной железы
Согласно мета-анализу, опубликованному в Cochrane Collaboration, два больших исследования, проведённые в России и Китае, не выявили положительного эффекта при самостоятельном обследовании молочных желез с целью ранней диагностики рака молочной железы. Результаты исследований указали на возможность повышенного риска в связи с увеличением количества биопсий молочной железы[18].
Сигналы тревоги[править | править вики-текст]
Сигналы тревоги рака молочной железы:
наличие уплотнений или опухолевидных образований в одной или обеих молочных железах;
выделения из соска любого характера, не связанные с беременностью или лактацией;
эрозии, корочки, чешуйки, изъязвления в области соска, ареолы;
беспричинно возникающая деформация, отек, увеличение или уменьшение размеров молочной железы;
увеличение подмышечных или надключичных лимфоузлов.
Выявление врачом хотя бы одного из указанных «сигналов тревоги» требует срочного (в молодом возрасте от 1-й до 4-й стадии может пройти всего несколько месяцев) направления больной к онкологу-маммологу терапевтом или маммологом в онкологический диспансер, где должны быть проведены УЗИ и пункция. Затем по результатам назначается либо операция с последующей химиотерапией, либо сначала химиотерапия с последующей операцией. Велик процент невнимательного (или задерживающего) отношения медицинскго персонала на районном уровне к новообразованиям, в результате чего злокачественная опухоль диагностируется на поздних (3-4 стадиях). От времени обращения до дня УЗИ может пройти месяц, а это недопустимо. Не стоит полагаться на то, что опухоль может быть доброкачественной. Быстрое обследование в медицинском учреждении поможет сохранить жизнь. Скрининг рака молочной железы проводится при физикальном обследовании молочной железы врачом любой специальности ежегодно, а также ежемесячного самообследования молочных желез. Маммография проводится женщинам от 35 до 50 лет раз в 2 года (при отягощённом личном и семейном анамнезе — 1 раз в год), женщинам после 50 лет — ежегодно. Профилактика рака молочной железы заключается в устранении факторов, способствующих его развитию, а также в оптимальной диспансеризации женщин с гиперпластическими процессами и своевременном адекватном их лечении, включая оперативные методы. Диагностика данного заболевания должна быть комплексная. Методами исследования являются: УЗИ молочных желез, пункция новообразования и трепан-биопсия под контролем УЗИ, МРТ, маммография, [[термомаммография - устаревший метод]. Велика роль анализа крови на онкомаркер. Для установления типа опухоли делают гистологическое исследование тканей.
Дифференциальная диагностика[править | править вики-текст]
1.Дисгормональные заболевания
Мастодиния (основные отличия: выраженный болевой синдром, невроз, связь с предменструальным периодом, чаще поражаются обе молочные железы у нерожавших).
Мастопатия
Гинекомастия
2. Доброкачественные опухоли
Фиброаденома
Липома
Внутрипротоковая папиллома (наблюдаются кровянистые или обильные серозные выделения из одного протока)
3. Острый гнойный мастит
Принципы лечения[править | править вики-текст]
К основным методам лечения рака молочной железы относятся: хирургическое лечение, лучевая терапия, химиотерапия, иммунотерапия, таргетная терапия[19].
Хирургическое лечение остаётся ведущим методом лечения рака молочной железы (остальные методы лечения, как правило, применимы при локализованном процессе). В большинстве случаев выполняется мастэктомия — хирургическое удаление всей молочной железы (весьма часто — наряду с окружающими тканями); профилактическая мастэктомия показана пациенткам, у которых диагностированы мутации в BRCA1 и BRCA2[20]. В последнее время при малом размере опухоли применяют также лампэктомию, когда удаляется только опухоль; однако такая операция остаётся травматичной, ведёт к деформации молочной железы, а её применимость ограничивается рядом жёстких требований. Данных недостатков лишён недавно разработанный метод криомаммотомии, при котором через небольшой надрез кожи к опухоли подводят криозонд с температурой наконечника минус 100—120 °C; при этом опухоль замораживается и превращается в примёрзший к криозонду «ледяной шарик», который удаляется из надреза вместе с криозондом[21][22].
Лучевая терапия обычно применяется как дополнение (адъювантная терапия) к хирургическому лечению и осуществляется после проведения мастэктомии или лампэктомии с целью уничтожения раковых клеток, которые могут остаться на месте удалённой опухоли, и снизить риск рецидива заболевания.
Химиотерапия нацелена на подавление клеток опухоли химическими препаратами, к которым эти клетки особенно чувствительны. Может применяться до, после и вместо хирургического лечения (когда отсутствуют показания к хирургическому вмешательству).
Иммунотерапия заключается в стимулировании собственного иммунитета пациента против клеток опухоли; применяется как дополнение к химиотерапии.
Таргетная терапия применяется по отношению к пациентам, у которых опухоль экспрессирует специфический ген HER2. Для такой терапии применяют трастузумаб[en] — препарат моноклональных антител, способный блокировать активность гена HER2 в клетках опухоли молочной железы, замедляя рост данной опухоли. Обычно применяют либо в комбинации с химиотерапией, либо в виде адъювантной терапии после хирургического лечения рака молочной железы[23][24]. В последние годы для таргетной терапии HER2-позитивного рака молочной железы применяют также препаратылапатиниб, пертузумаб[en], нератиниб[en][25].
Виды оперативных вмешательств[править | править вики-текст]
Органосохраняющие операции[править | править вики-текст]
Органосохраняющие операции – радикальное удаление опухоли в пределах здоровой ткани с удовлетворительным косметическим результатом.
Лампэктомия.
Радикальная секторальная резекция (по Блохину).
Квадрантэктомия с лимфаденэктомией.
Гемимастэктомия с лимфаденэктомией.
Субтотальная резекция с лимфаденэктомией.
Подкожная мастэктомия с лимфаденэктомией.
Радикальные операции[править | править вики-текст]
Радикальная мастэктомия по Маддену.
Радикальная мастэктомия по Пэйти.
Радикальная мастэктомия по Холстеду.
Расширенная радикальная модифицированная мастэктомия.
Расширенная радикальная подмышечно-грудинная мастэктомия.
Мастэктомия по Пирогову.
Простая мастэктомия
Профилактика[править | править вики-текст]
Первичная профилактика рака проводится по следующим направлениям:
Онкогигиеническая профилактика.
Биохимическая профилактика.
Медико-генетическая профилактика.
Иммунобиологическая профилактика.
Эндокринно-возрастная профилактика.
Психологические аспекты заболевания[править | править вики-текст]
Эмоциональное воздействие на человека, связанное с постановкой диагноза, процедурой лечения и проблемами социальной адаптации, подчас чрезвычайно глубоко.
Большинство цивилизованных клиник, занимающихся профилактикой и лечением раковых заболеваний, работает в сотрудничестве с реабилитационными группами, которые специальными психотерапевтическими методами создают поддерживающие условия с целью подготовки к лечению больных с установленным диагнозом и помощи тем, кто продолжает жизнь после предпринятого лечения.
Существуют и он-лайн реабилитационные группы, общение в которых может быть удобно определенной категории больных, в частности тогда, когда они крайне неуверенны в себе, застенчивы и имеют отрицательный образ самих себя, связанный с болезнью. Следует отметить, что часто общение с больными, не профессионалами в медицине, может вызывать неоправданное волнение.
Что такое цитологическое исследование соскобов и отпечатков опухолей? Цитологическое исследование – это лабораторно-инструментальный метод исследования, суть которого заключается в оценке качественных и количественных характеристик клеток в биологическом материале (в соскобе или отпечатке). С помощью цитологического исследования врач получает возможность установить характер изменения ткани – злокачественное перерождение или доброкачественное разрастание. Получить биологический материал для этого исследования можно несколькими способами. Соскоб получают путем соскабливания небольшого количество ткани с поверхности опухоли и последующего нанесения полученного биологического материала на предметное стекло. Отпечатки опухолей получают путем кратковременного прижатия предметного стекла к свежему срезу удаленной опухоли. Цитологическое исследование востребовано во многих сферах медицины: хирургии, акушерстве, онкологии. С его помощью проводят диагностику многих онкологических и предраковых заболеваний. Кто назначает данное исследование, где его можно пройти? Назначить данное исследование могут врач-хирург, акушер-гинеколог, онколог, дерматолог. Взятие биологического материала для приготовления препарата осуществляет врач соответствующей специальности. При поверхностно расположенных опухолях врач может взять материал и приготовить препарат в процедурном кабинете. Иногда мазки-отпечатки делают из ткани опухоли, удаленной во время хирургической операции. В этом случае препарат готовят непосредственно в операционной. Показания для исследования отпечатков опухолей и соскобов с опухолей В гинекологической практике при диагностике заболеваний женских половых органов готовят мазки из соскобов с шейки матки и цервикального канала. В гастроэнтерологии отпечатки кусочков биопсийного материала, полученного с помощью фиброгастродуоденоскопии, используют для диагностики рака желудка или пищевода. С помощью ФГДС получают и соскобы со слизистой оболочки пищевода, желудка и 12-перстной кишки. В онкологии с помощью этого метода исследования выполняют первичную диагностику опухолей кожи и слизистых (рака кожи, базалиомы и пр.). Весьма востребовано цитологическое экспресс-исследование. В этом случае прямо во время операции по удалению опухоли производят изготовление препарата, и врач-цитолог изучает его под микроскопом. От результата исследования зависит объем операции. Если злокачественных клеток не обнаружено, удаляют только опухоль. Если же они имеются, то иссекают и близлежащие ткани, и регионарные лимфоузлы. Как готовят соскобы и отпечатки опухолей Изготовление соскоба – достаточно легкая манипуляция. Шпателем или ложкой Фолькмана врач соскребает с поверхности новообразования немного ткани и наносит материал тонким слоем на предметное стекло. Далее препарат подсушивают и, при необходимости, красят специальными красителями. Для получения отпечатков врач тесно прижимает срез опухоли к предметному стеклу, после чего препарат подсушивают и красят. Интерпретация результатов Специалист изучает препараты под микроскопом и дает заключение, которое заносит в специальный бланк. В заключении врач указывает, доброкачественный или злокачественный процесс имеет место. При доброкачественном процессе описывает дисплазию или предраковую пролиферацию (размножение клеток), если она имеет место. При злокачественной опухоли указывает ее гистологическую форму и степень дифференцировки. Недостатки метода Недостаток метода заключается в большой зависимости точности результата от правильности сбора материала. Иногда в материал попросту не попадают раковые клетки. Рекомендуется дополнять этот метод гистологическим исследованием.
риготовить:
Установить с пациентом доверительное отношение, разъяснить механизм забора материала и получить согласие на его проведение;перчатки; маску;ватные шарики; марлевые салфетки; скарификатор; 70% спирт; обезжиренное
предметное стекло;контейнер для отходов; бланки направлений; ручку; стеклограф; стерильный физиологический раствор; емкость с питательной средой:
Действие:
Вымыть (гигиенический уровень) руки и надеть перчатки; обработать ватным шариком, со спиртом кожу над розеолой; с помощью ватного тампона промыть кожу стерильным физиологическим раствором и просушить стерильной салфеткой; собрать тампоны и салфетку в контейнер; скарифицировать кожу над розеткой; с помощью пипетки нанести на рану 1-2 капли питательной среды; через 1-2 минуты собрать материал пипеткой или кусочком ваты; сделать отпечаток на предметном стекле и обвести стеклографом; провести дезинфекцию помещения и инструментов; снять перчатки и поместить их в контейнер; вымыть руки (гигиенический уровень) и осушить руки; оформить направление и отправить материал в лабораторию; заполнить медицинскую документацию.
Большинство болезней кожи имеют сходную клиническую картину, однако можно выделить девять основных групп характерных дерматологических нарушений:
– зуд
– алопеция
– образование чешуек/корок/себорея
– макулы/папулы/вскрывающиеся пустулы
– узлы/опухоли
– свищи
– язвы
– изменения пигментации
– отиты
Как только врач-клиницист начнет относить каждого пациента к какой-либо из перечисленных выше категорий, ему станет намного проще формировать список дифференциальных диагнозов и разрабатывать диагностический план. Необходимо помнить, что у пациента могут быть сопутствующие болезни в настоящий момент времени, которые затрудняют постановку основного диагноза.
Быстрая постановка диагноза часто представляет значительные трудности для практикующего врача, поэтому далее речь пойдёт о доступных методах лабораторного исследования, требующих минимальных затрат времени и средств. Наиболее простые и быстрые диагностические тесты, используемые на практике:
– Соскобы кожи
– Трихоскопия
– Вычёсывание гребнем или щёткой
– Скотч-тест
– Исследование на дерматофиты
– Цитология кожи
