
- •Значения длины связи
- •Интервал перехода кислотно-основных индикаторов
- •Относительная электроотрицательность некоторых элементов
- •Ионные радиусы
- •Строение и ожидаемая полярность молекул
- •Виды гибридизаций ао и геометрические параметры частиц
- •Константы неустойчивости некоторых комплексных ионов
- •Окраска вещества при поглощении определенной части спектра
- •Криоскопические (k) и эбулиоскопические (е) константы некоторых растворителей
- •Давление насыщенного водяного пара при различных температурах
- •Произведения растворимости малорастворимых электролитов при 25 с
- •Растворимость, осаждение и гидролиз солей при комнатной температуре
- •Стандартные электродные потенциалы в водных растворах
- •Стандартные окислительно-восстановительные потенциалы
- •Стандартные термодинамические свойства веществ
- •Теплоты сгорания органических веществ
Стандартные электродные потенциалы в водных растворах
|
Электрод |
Е0, В |
Электрод |
Е0, В |
|
Li+/Li |
– 3,045 |
Tl +/Tl |
– 0,336 |
|
Rb+/Rb |
– 2,925 |
Co2+/Co |
– 0,277 |
|
K+/K |
– 2,924 |
Ni2+/Ni |
– 0,257 |
|
Cs+/Cs |
– 2,923 |
Mo3+/Mo |
– 0,200 |
|
Ba2+/Ba |
– 2,912 |
Sn2+/Sn |
– 0,136 |
|
Fr+/Fr |
– 2,900 |
Pb2+/Pb |
– 0,126 |
|
Sr2+/Sr |
– 2,868 |
Fe3+/Fe |
– 0,036 |
|
Ra2+/Ra |
– 2,800 |
2H+/H2 |
0,000 |
|
Ca2+/Ca |
– 2,866 |
Ge4+/Ge |
+0,124 |
|
La3+/La |
– 2,379 |
Ge2+/Ge |
+0,240 |
|
Y3+/Y |
– 2,372 |
Re3+/Re |
+0,300 |
|
Na+/Na |
– 2,714 |
Bi3+/Bi |
+ 0,308 |
|
Mg2+/Mg |
– 2,363 |
Cu2+/Cu |
+ 0,342 |
|
Be2+/Be |
– 1,847 |
Tc2+/Tc |
+0,400 |
|
Al3+/Al |
– 1,662 |
Ru2+/Ru |
+0,455 |
|
Ti 2+/Ti |
– 1,628 |
Cu+/Cu |
+ 0,521 |
|
Zr4+/Zr |
– 1,580 |
Rh2+/Rh |
+0,600 |
|
Hf4+/Hf |
– 1,550 |
Tl 3+/Tl |
+ 0,741 |
|
Ti 3+/Ti |
– 1,370 |
Rh3+/Rh |
+0,758 |
|
V2+/ V |
– 1,186 |
Po4+/Po |
+0,760 |
|
Mn 2+/ Mn |
– 1,180 |
Hg |
+0,797 |
|
Cr 2+/Cr |
– 0,913 |
Ag+/Ag |
+ 0,799 |
|
Zn2+/Zn |
– 0,763 |
Hg 2+/Hg |
+ 0,851 |
|
Cr3+/Cr |
– 0,744 |
Pd2+/Pd |
+0,951 |
|
Ta 3+/Ta |
– 0,600 |
Ir3+/Ir |
+1,156 |
|
Ga3+/Ga |
– 0,549 |
Pt2+/Pt |
+ 1,190 |
|
Fe2+/Fe |
– 0,440 |
Au3+/Au |
+ 1,498 |
|
Cd2+/Cd |
– 0,403 |
Au+/Au |
+ 1,691 |
|
In3+/In |
– 0,338 |
|
|
Стандартные окислительно-восстановительные потенциалы
-
Элемент
Полуреакция
Е0, В
Ag
Ag+ + 1ē = Ag
+0,80
AgCl + 1ē = Ag+ Cl-
+ 0,22
Ag2+ + 1ē = Ag+
+ 1,98
Ag2О + Н2О + 2ē= 2Ag+ 2ОН-
+ 0,34
2AgО + Н2О + 2ē=Ag2О + 2ОН-
+ 0,607
Ag2S + 2ē= 2Ag+ S2-
– 0,691
Ag2S + 2Н++ 2ē= 2Ag + Н2S
– 0,0366
AgI + 1ē = Ag+ I-
– 0,15
Al
AlO
 + 2H2O
+ 3 ē
= Al + 4OH-
+ 2H2O
+ 3 ē
= Al + 4OH-– 2,35
Al(OH)3 + 3ē = Al + 4OH-
– 2,328
As
H3AsO4 + 2H+ + 2ē = HAsO2 + 2H2O
+ 0,56
AsO
 + 2H2O
+ 2ē
= AsO
+ 2H2O
+ 2ē
= AsO +
4OH-
+
4OH-– 0,71
Be
Be2O
 +
3H2O
+ 4ē
= 2Be + 6OH-
+
3H2O
+ 4ē
= 2Be + 6OH-– 2,63
Bi
NaBiO3 + 6H+ + 2ē = Bi3+ + 3H2O + Na+
+1,81
Br
BrO3- + 3H2O + 6ē = Br-+ 6OH-
+0,61
Br2 + 2ē = 2Br-
+1,09
HBrO + H+ + 2ē = Br- + H2O
+1,34
Cl
Cl2 + 2ē = 2Cl-
+1,36
ClO3- + 6H+ + 6ē = Cl- + 3H2O
+1,46
ClO- + H2O + 2ē = Cl- + 2OH-
+0,92
2ClO- + 2H2O + 2ē = Cl2 + 4OH-
+1,56
ClO
 + 2H2O
+ 4ē
= Cl-
+ 4OH-
+ 2H2O
+ 4ē
= Cl-
+ 4OH-+0,76
ClO
 + H2O
+ 2ē
= ClO-
+ 2OH-
+ H2O
+ 2ē
= ClO-
+ 2OH-+0,66
ClO
 + 8H+
+ 8ē
= Cl-
+ 4H2O
+ 8H+
+ 8ē
= Cl-
+ 4H2O+1,389
ClO
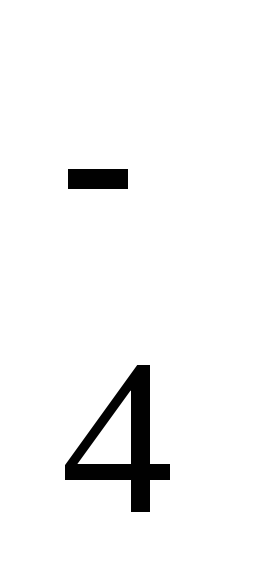 + H2O
+ 2ē
= ClO
+ H2O
+ 2ē
= ClO + 2OH-
+ 2OH-+0,36
HClO2 + 2H+ + 2ē = HClO + H2O
+ 1,645
Cr
Cr2O72- + 14H+ + 6ē = 2Cr3+ + 7H2O
+1,33
CrO
 +2H2O
+ 3ē
= CrO2-
+ 4OH-
+2H2O
+ 3ē
= CrO2-
+ 4OH-- 0,21
CrO
 + 4H2O
+ 3ē
= Cr3+
+ 8OH-
+ 4H2O
+ 3ē
= Cr3+
+ 8OH-+1,45
CrO
 + 8H+
+ 3ē
= Cr3+
+ 4H2O
+ 8H+
+ 3ē
= Cr3+
+ 4H2O
+1,47
Cr(OH)3 + 3ē = Cr + 3OH-
– 1,48
CrO3 + 6H+ + 3ē = Cr3+ + 3H2O
– 0,11
CrO
 + 4H2O
+ 3ē
= Cr(OH)3
+ 5OH-
+ 4H2O
+ 3ē
= Cr(OH)3
+ 5OH-– 0,13
H
2H2O + 2ē = H2 + 2OH-
– 0,83
H2O2 + 2H+ + 2ē = 2H2O
+1,776
I
2IO3- + 12H+ + 10ē = I2 + 6H2O
+1,195
2IO- + 4H+ + 2ē = I2 + 2H2O
+1,10
HIO + H+ + 2ē = I- + H2O
+0,987
IO- + H2O + 2ē = I- + 2OH-
+0,485
IO
 + 6H+
+ 6ē
= I-
+ 3H2O
+ 6H+
+ 6ē
= I-
+ 3H2O
+1,085
IO
 + 2H2O+
4ē =
IO-
+ 4OH-
+ 2H2O+
4ē =
IO-
+ 4OH-
+0,15
IO
 + 3H2O+
6ē =
IO-
+ 6OH-
+ 3H2O+
6ē =
IO-
+ 6OH-
+0,26
I2 + 2ē = 2I-
+0,54
2HIO + 2H+ + 2ē = I2 + 2H2O
+1,439
Fe
Fe(OH)3 + 1ē = Fe(OH)2 + OH-
– 0,56
Fe2O3 + 4H+ + 2ē = 2FeOH+ + H2O
+0,16
Mn
MnO2 + 4H+ + 2ē = Mn2+ + 2H2O
+1,24
MnO
 + 8H+
+ 5ē
= Mn2+
+ 4H2O
+ 8H+
+ 5ē
= Mn2+
+ 4H2O+1,53
MnO
 + 1ē
= MnO42-
+ 1ē
= MnO42-+0,56
MnO2 + 4OH- + 2ē = Mn2+ + 2H2O
+1,15
MnO
 + 2H2O
+ 2ē
= MnO2
+ 4OH-
+ 2H2O
+ 2ē
= MnO2
+ 4OH-+0,60
MnO
 + 4H+ +
3ē =
MnO2
+ 2H2O
+ 4H+ +
3ē =
MnO2
+ 2H2O+1,679
MnO
 +
2H2O
+ 3 ē
= MnO2
+ 4OH-
+
2H2O
+ 3 ē
= MnO2
+ 4OH-+0,595
Mn(OH)2 + 2ē = Mn + 2OH-
– 1,56
Mn(OH)3 + 1ē = Mn(OH)2 + OH-
+0,15
Mn2O3 + 6H+ + 2ē = 2Mn2+ + 3H2O
+1,485
N
NO
 + 2H+
+ 1ē
= NO2
+ H2O
+ 2H+
+ 1ē
= NO2
+ H2O+0,77
N2 + 2H2O + 6H+ + 6ē = 2NH4OH
0,092
3N2 + 2H+ + 2ē = 2HN3
– 3,09
N2H
 +
3H+
+ 2ē
= 2NH
+
3H+
+ 2ē
= 2NH
+1,275
N2O + 2H+ + 2ē = N2 + H2O
+1,766
N2O4 + 2ē = 2NO

+0,867
N2O4 + 2H+ + 2ē = 2HNO2
+1,065
N2O4 + 4H+ + 4ē = 2NO + 2H2O
+1,035
2NO + 2H+ + 2ē = N2O + H2O
+1,591
2NO + H2O + 2ē = N2O + 2OH-
+0,76
HNO2 + H+ + 1ē = NO + H2O
+0,983
NO
 +
3H+
+ 2ē
= HNO2
+ H2O
+
3H+
+ 2ē
= HNO2
+ H2O
+0,94
NO
 + 2H+
+ 2ē
= NO2-
+ H2O
+ 2H+
+ 2ē
= NO2-
+ H2O+0,84
NO
 + H2O
+ ē
= NO + 2OH-
+ H2O
+ ē
= NO + 2OH-– 0,46
NO
 + 4H+
+ 3ē
= NO + 2H2O
+ 4H+
+ 3ē
= NO + 2H2O+0,96
2NO
 + 2H2O
+ 4ē
= N2O
+ 2H2O
+ 4ē
= N2O + 4OH-
+ 4OH-– 0,18
2NO
 + 3H2O
+ 4ē
= N2O
+ 6OH-
+ 3H2O
+ 4ē
= N2O
+ 6OH-+0,15
2NO
 + 2H2O
+ 2ē
= N2O4
+ 4OH-
+ 2H2O
+ 2ē
= N2O4
+ 4OH-– 0,85
2NO
 + 4H+
+ 2ē
= N2O4
+ 2H2O
+ 4H+
+ 2ē
= N2O4
+ 2H2O+0,803
NO
 + H2O
+ 2ē
= NO
+ H2O
+ 2ē
= NO + 2OH-
+ 2OH-+0,01
О
O2+ 2H++ 4ē= 4OH-
+0,40
O2+ 2H++ 2ē=H2O2
+0,69
O2+4H++4ē=2H2O
+1,229
O2+ 2H2O+2ē=H2O2 + 2OH-
– 0,146
O3+ 2H++ 2ē=H2O + O2
+2,076
O2+ 2H2O+ 4ē= 4OH-
+0,40
O3 + 2H2O + 2ē = O2 + 2OH-
+1,24
P
H3PO4 + 5H+ + 5ē = P + 4H2O
-0,41
H3PO4 + 2H+ + 2ē = H3PO3 + H2O
-0,28
Pb
[Pb(OH)4]2- + 2ē = Pb + 4OH-
-0,52
PbO2 + 4H+ + 2ē = Pb2+ + 2H2O
+1,46
PbO2 + 2ē = PbO22-
+1,70
S
S + 2ē = S2-
-0,48
S + H2О + 2ē = HS-+ ОН-
- 0,478
SO42- + 10H+ + 8ē = H2S + 4H2O
+0,30
S + 2H+ + 2ē = H2S
+0,142
SO2 + 4H+ + 4ē = S + 2H2O
+0,45
SO42-+ 4H+ + 2ē = SO2 + 2H2O
+0,16
SO42- + 8H+ + 6ē = S + 4H2O
+0,35
SO42- + 8H+ + Cu2+ + 8ē = CuS + 4H2O
+0,42
SO42- + 2H+ + 2ē = SO32- + H2O
-0,10
Se
SeO42- + 2H+ + 2ē = SeO32- + H2O
+1,15
