
Вьюник. Лекция № 10
.pdf
Молекула |
Молекулярнi орбiталi |
Енергетичнi дiаграми |
Енергетичнi дiаграми
Трьохатомнi молекули
Трьохатомнi лiнiйнi молекули. Стан e¯ в трьохатомних молекулах описується з допомогою трьохцентрових МО, зокрема застосовується у варiантi МО – ЛКАО.
Застосування розглянемо на прикладi BeH2. Електронна формула: (σsзв)2(σxзв)2. У атома H немає орбiталей, здатних утворювати π- зв‘язок. У зв‘язку з цим 2px- та 2py- орбiталi атома Be в утворенi хiмiчного зв‘язку не приймають участi. Вони переходять в незмiнному станi, як -МО з енергiєю рiвною середнiй енергiї вихiдних АО атома Be (це так званi незв‘язуючi МО).
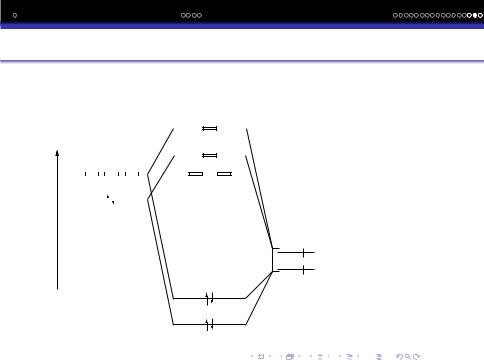
Комбiнацiя 1s− орбiталi 2-х атомiв H та 2s− орбiталi ато-
ма Be приводить до утворення трьохцентрових МО: σsзв i
σsр.
21/23
Молекула |
Молекулярнi орбiталi |
Енергетичнi дiаграми |
Енергетичнi дiаграми
Трьохатомнi молекули
|
Орбіталі Be |
|
Орбіталі BeH2 |
Орбіталі H |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
σ р |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
z |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
σ р |
|
E |
|
|
|
|
|
|
|
|
|
|
|
|
|
s |
|
|
|
2p |
|
|
πx πy |
|
|||||||||
|
|
|
2s |
|
|
|
|
|
|
|
|
|
|
||
1sA 
1sB 
σzзв
σsзв
22/23
Молекула |
Молекулярнi орбiталi |
Енергетичнi дiаграми |
Енергетичнi дiаграми
Трьохатомнi молекули
Комбiнацiя 1sорбiталей 2-х атомiв H та 2pz -орбiталi атома Be приводить до утворення 2-х трьохцентрових орбiталей σzзв та σzр.
ЕН атома гiдрогену бiльша ЕН атома Be. Отже АО гiдрогену розмiщенi на енергетичнiй дiаграмi нижче нiж АО атома Be.
4-и валентних e¯ розмiщуються на σsзв− та σzзв− орбiталях. При цьому кожна iз 2-х ЕП в рiвнiй мiрi належить обом атомам H.
Хiмiчний зв‘язок утворюється за рахунок 2-х трьохцентрових орбiталей, на яких рухається по два e¯.
BeF2: У атома F валентними є: 2s,2px,2py,2pz–орбiталi. Електронна формула:
(2sa)2(2sb)2(σsзв)2(σxзв)2(πyзвπzзв)4(πyнзвπzнзв)4
23/23
