
- •2 Кислотно-основные методы
- •2.1 Краткие теоретические основы метода
- •2.1.1 Кислотно-основное взаимодействие
- •Классификация кислот и оснований в зависимости от величины их рКа
- •Величины рКа оснований в различных растворителях
- •2.1.2 Титрованные растворы
- •Титранты кислотно-основного метода
- •2.1.3 Установление конца титрования с помощью визуальных индикаторов
- •Интервал перехода окраски и показателя титрования кислотно-основных индикаторов
- •Данные для эмпирического выбора индикатора при кислотно-основном титровании
- •Интервалы рН и изменение цвета индикаторов (гф XI, вып.2, стр. 102)
- •2.1.4 Определение ингредиентов многокомпонентных лекарственных форм
- •2.1.5 Варианты и способы кислотно-основного титрования
- •2.2 Ацидиметрия
- •2.2.1 Вариант нейтрализации
- •2.2.2 Вариант вытеснения
- •2.2.3 Вариант гидролитического разложения
- •2.3.2 Вариант вытеснения
- •2.3.3 Вариант гидролитического разложения
- •2.3.4 Косвенное титрование
- •Соле- и комплексообразование
- •Конденсация
- •2.4 Титрование в неводных растворителях
- •Примеры дифференцирующего действия растворителя
- •Пример нивелирующего действия растворителя
- •2.4.1 Титрование в среде протогенных растворителей. Ацидиметрия
- •Определение кофеина
- •Определение изониазида
- •Определение дибазола
- •Определение атропина сульфата
- •2.4.2 Титрование в среде протофильных растворителей. Алкалиметрия
- •Определение теобромина
- •Определение фталазола
2.3.4 Косвенное титрование
Способ алкалиметрического титрования применяется в анализе соединений, взаимодействия которых со вспомогательными реактивами сопровождается выделением эквивалентного количества кислоты. При этом могут использоваться различные типы реакций, наибольшее распространение получили реакции соле- и комплексообразования и конденсации.
Соле- и комплексообразование
В этом случае определение основано на свойстве соединений, содержащих подвижный атом водорода вступать в реакцию соле- и комплексообразования с ионами некоторых металлов (Ag+,Co2+,Cd2+), что сопровождается выделением эквивалентного количества кислоты, которую определяют алкалиметрически (вариант нейтрализации). По этому способу определяют теобромин, теофиллин в индивидуальном виде и в составе эуфиллина, рибофлавин.
При проведении анализа к навеске препарата прибавляют растворы серебра нитрата, образуется соль и эквивалентное количество кислоты, которую оттитровывают щелочью (индикатор – феноловый красный). Например, определение теофиллина:
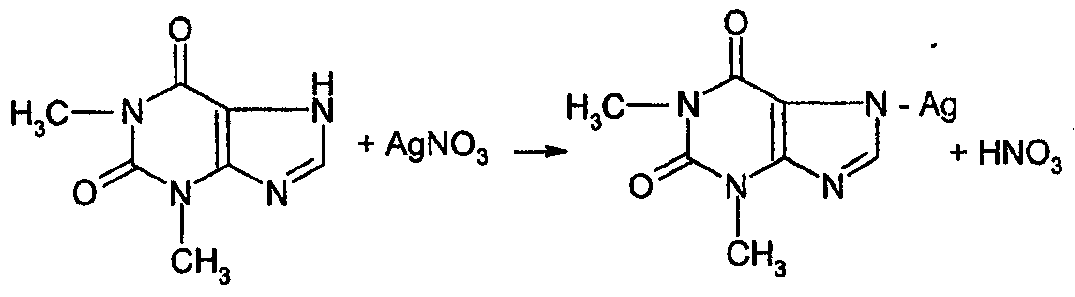
HNO3+NaOH→NaNO3+H2O
Э = М.м.
Вариант нашел применение в анализе индивидуальных веществ и их лекарственных форм заводского и экстемпорального изготовления.
Конденсация
Образование оксима.В этом случае определение основано на свойстве соединений, содержащих кетонный или альдегидный карбонилы реагировать с гидроксиламина гидрохлоридом с образованием оксима, что сопровождается выделением эквивалентного количества кислоты, которую определяют алкалиметрически.
Так можно провести количественное определение камфоры и её производных, кортикостероидов, цитраля и др.
Реакция конденсации кетона с гидроксиламином протекает в спиртоводном растворе при нагревании.

Способ может использоваться в анализе индивидуальных веществ и лекарственных форм промышленного изготовления.
Реакция конденсации цитраля протекает при нагревании до 70-75°С в водном растворе.
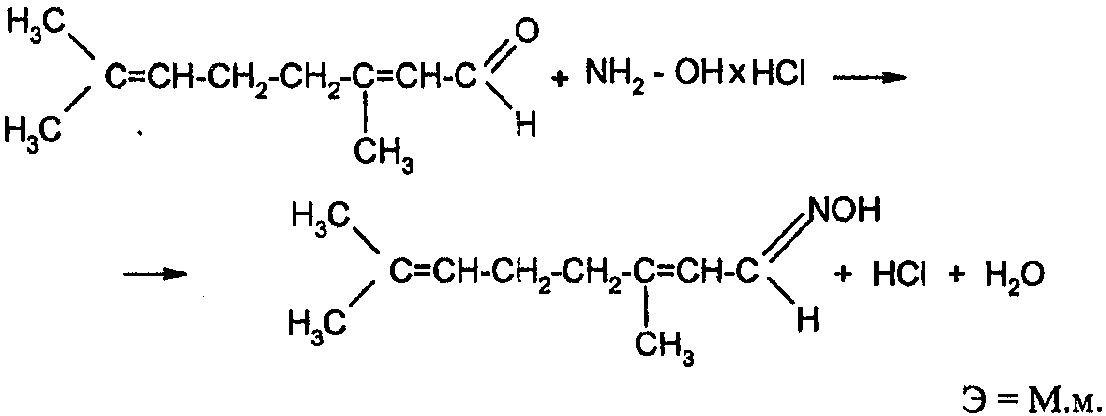
Выделившуюся кислоту титруют щелочью с бромфеноловым синим.
Ацетилирование.В этом случае определение основано на свойстве соединений, содержащих спиртовой или фенольный гидроксил, вступать во взаимодействие с уксусным ангидридом с образованием сложных эфиров и выделением эквивалентного количества уксусной кислоты. В учебных руководствах такое определение носит название метода ацетилирования.
Этим способом проводят количественное определение ментола, синэстрола, диэтилстильбестрола.
Реакция ацетилирования протекает в безводной среде (например, в пиридине) при нагревании. После завершения реакции ацетилирования в реакционную среду добавляют воду для разложения избытка уксусного ангидрида. Уксусную кислоту, выделившуюся в процессе ацетилирования и образовавшуюся из избытка уксусного ангидрида, титруют щелочью (индикатор фенолфталеин).
Параллельно проводят контрольный опыт, в котором тот же объем уксусного ангидрида, что взят для реакций с определяемым веществом, разлагают водой и образовавшуюся уксусную кислоту оттитровывают щелочью. Расчет проводят по разности объемов щелочи, пошедшей на титрование контрольного опыта и испытуемого раствора.
Молярная масса эквивалента препарата зависит от количества спиртовых или фенольных гидроксилов в структуре определяемого вещества.
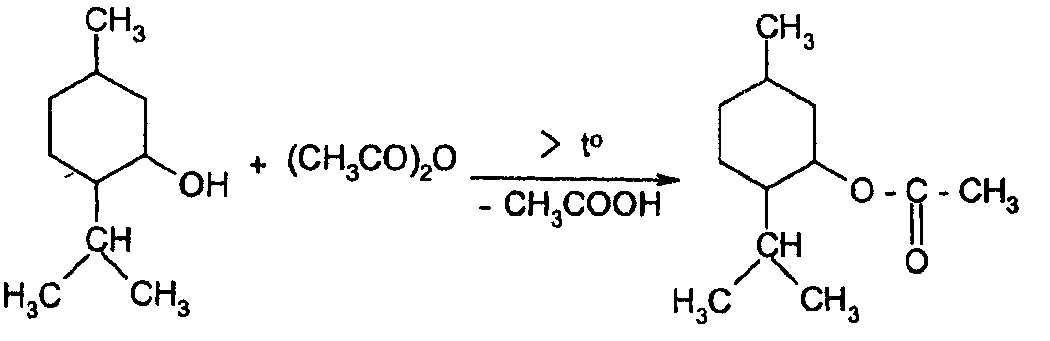
Э = М.м.
(CH3CO)2O + H2O → 2CH3COOH
CH3COOH+NaOH→CH3COONa+H2O
Способ используется в анализе индивидуальных веществ, является фармакопейным для субстанций ранее перечисленных соединений. Во внутриаптечном анализе не используется.
Образование гексаметилентетрамина.Метод является специфичным при анализе галогеноводородных солей аммония в смесях, содержащих хлористо- или бромистоводородные соли других катионов (натрия, кальция, калия). В основе метода лежит способность солей аммония вступать во взаимодействие с формальдегидом, в результате чего образуется гексаметилентетрамин и эквивалентное количество кислоты, которую титруют раствором щелочи (индикатор фенолфталеин).

Метод может быть использован в количественном определении солевых растворов.
