
- •1.Термодинамическая система и окружающая среда.
- •3.Внутренняя энергия и энтальпия
- •10.Условия химического равновесия.
- •11.Закон действия масс.
- •12.Константа равновесия в гомогенной системе. Способы выражения константы равновесия.
- •14.Уравнение изобары Вант-Гоффа.
- •22.Давление насыщенного пара. Закон Рауля.
- •28.Простая и фракционная перегородка
- •29.Экстракция,экстрагент,коэффициент распределения
10.Условия химического равновесия.
Состояние хим. равновесия - это состояние при котором хим.потенциал продуктов и исходных в-в равны между собой, с учётом стехиометрии процесса.
О химическом равновесии можно говорить при выполнении двух условий:
Скорости прямой и обратной реакции равны между собой.
Равновесие существует если при оказании внешнего воздействия, а затем при его снятии система возвращается в исходное состояние.
11.Закон действия масс.
При постоянной температуре скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ, взятых в степенях, равных стехиометрическим коэффициентам в уравнении реакции.
Например, для реакции синтеза аммиака:
N2 + 3H2 = 2NH3
закон действующих масс имеет вид:
Кс = [NH3]2 / [N2][H2]3
12.Константа равновесия в гомогенной системе. Способы выражения константы равновесия.
константа равновесия – это постоянная величина, равная отношению произведений равновесных концентраций конечных и исходных участников реакции, взятых в степенях, соответствующих стехиометрическим коэффициентам
Гомогенными называются реакции, протекающие в одной фазе: в смеси газов, в жидком или иногда в твёрдом растворе.
Способы выражения константы равновесия
Если
концентрации веществ, участвующих в
реакции, выражены в молярных единицах
молярности , т.е. в моль/л, то она обычно
обозначается Кс
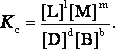
Для гомогенной газовой реакции константу равновесия удобнее выразить через парциальные давления веществ:

Иногда
константу равновесия удобно выразить
не через парциальные давления и
концентрации, а через количества веществ:
![]() или через соответствующие мольные доли:
или через соответствующие мольные доли:
В общем случае константы равновесия Кс, Кр, Кn и КN различны.
13.Принцип Ле-Шателье-Брауна.
если на систему, находящуюся в равновесии, оказывается внешнее воздействие, то равновесие смещается в том направлении, которое ослабляет внешнее воздействие.
14.Уравнение изобары Вант-Гоффа.

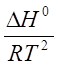 данное
выражение позволяет качественно оценить
влияние Т на равновесие и константу
равновесия.
данное
выражение позволяет качественно оценить
влияние Т на равновесие и константу
равновесия.
15.Фаза.
Фазой называется– гомогенная часть гетерогенной системы, имеющая реальную границу раздела, внутри которой все свойства могут меняться непрерывно, а при переходе через которую скачком.
16.Составляющие вещества и компоненты.
Компонентом называется– минимальное количество составляющих в-в, достаточное для описания состояния систем.
Составляющими веществаминазываются – вещества, входящие в состав системы, которую можно выделить обычными препаратными методами и которые могут существовать вне системы сколько угодно.
17.Правило фаз Гиббса.
Число степеней свободы равновесной термодинамической системы, на которую из внешних факторов влияют только температура и давление, равно числу независимых компонентов С=К-Ф+n(число внешних параметров)
Правило фаз показывает, что число степеней свободы возрастает с увеличением числа компонентов и уменьшается с увеличением числа фаз системы.
18.Условия фазового равновесия в системе.
В гетерогенной системе имеется фазовое равновесие, если между фазами существуют следующие виды равновесий:
Термическое(равенство температур)
Механическое(равенство давлений)
Химическое в отношении каждого компонента
19.уравнение Клайперона-Клаузиуса
![]() где,
–ΔV-
изменение объёма вещества при переходе
его из первой фазы во вторую, Т –
температура перехода,
ΔH –
изменение энтропии и энтальпии вещества
при переходе 1 моля вещества из одной
фазы в другую
где,
–ΔV-
изменение объёма вещества при переходе
его из первой фазы во вторую, Т –
температура перехода,
ΔH –
изменение энтропии и энтальпии вещества
при переходе 1 моля вещества из одной
фазы в другую
Оно позволяет оценить как меняется температура или давление при фазовом переходе при изменении 2 параметра.
20. диаграмма состояния воды
Зависимость между величинами, характеризующими состояние системы, и фазовыми превращениями в системе переход из твердого состояния в жидкое ,из жидкого в газообразное
21.Истинные
растворы. Способы выражения концентрации
раствора. Расчёт молярной и массовой
доли вещества и молярной концентрации
вещества в растворе. 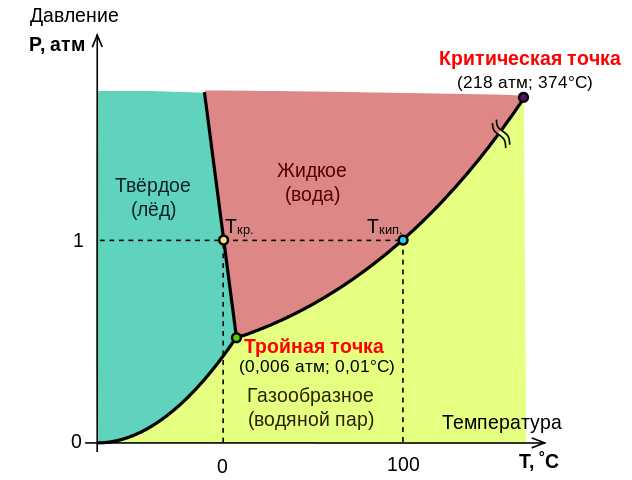
Истинный раствор - это разновидность раствора, в котором размеры частиц растворенного вещества предельно малы и сопоставимы с размером частиц растворителя.
Растворы бывают газообразные(газовые смеси),жидкие итвердые. Газообразным раствором является воздух. Морская вода – смесь солей в воде – жидкий раствор. Твердые растворы – металлические сплавы. Растворы состоят из растворителя и растворенного вещества (веществ).
Раствором называется твердая или жидкая гомогенная система, состоящая из двух или более составных частей.
Растворителем считается – в-во, определяющее агрегатное состояние раствора или в-во, которого больше по объёму или массе.
Способы выражения концентрации растворов.
Концентрация раствора – это масса или количество растворенного вещества в определенном количестве, массе или объеме раствора или растворителя.
1) Массовая доля (wi) – это масса растворенного вещества, содержащаяся в 100 граммах раствора.
2) Молярная доля(мольная) – Xi – кол-во моль компонента, содержащиеся в 1 моль р-ра.
3) Моляльная концентрация(моляльность) mi – количество молей растворенного вещества, содержащихся в 1 кг растворителя [моль/кг].
4) Молярная концентрация Сi – количество молей растворенного вещества, содержащаяся в 1 литре или в 1дм3 раствора [моль/л].
