
- •1.Термодинамическая система и окружающая среда.
- •3.Внутренняя энергия и энтальпия
- •10.Условия химического равновесия.
- •11.Закон действия масс.
- •12.Константа равновесия в гомогенной системе. Способы выражения константы равновесия.
- •14.Уравнение изобары Вант-Гоффа.
- •22.Давление насыщенного пара. Закон Рауля.
- •28.Простая и фракционная перегородка
- •29.Экстракция,экстрагент,коэффициент распределения
22.Давление насыщенного пара. Закон Рауля.
Давление насыщенного пара растворителя над раствором прямо пропорционально его молярной доле в растворе. Pi=Pi0*Xi
23.закон Генри
При постоянной температуре парциальное давление pi растворенного вещества над его предельно разбавленным раствором пропорционально мольной доле этого веществаXi, то естьpi = Ki*Xi,где Ki - постоянная Генри для вещества i.
24.криоскопия
Криоскопия - явление понижения температуры замерзания раствора по сравнению с чистым растворителем. При условии, что в растворе содержится нелетучее растворённое вещество.
25.эбулиоскопия
Метод исследования жидких растворов нелетучих веществ, основанный на повышении температуры кипения раствора по отношению к температуре кипения чистого растворителя.
26.осмос. осмотическое давление
Явление переноса растворителя через полупроницаемую мембрану из области с большим его содержанием в область с меньшим содержанием- осмос.
Давление, которое надо приложить чтобы переход остановить-осмотическое давление.
27.законы коновалова
Первый закон Коновалова описывает процесс фракционной перегонки: насыщенный пар по сравнению с равновесным раствором обогащён компонентом, добавление которого к системе повышает общее давление пара
Рассмотрим фазовую диаграмму при постоянном давлении для бинарной системы в координатах состав — температура:
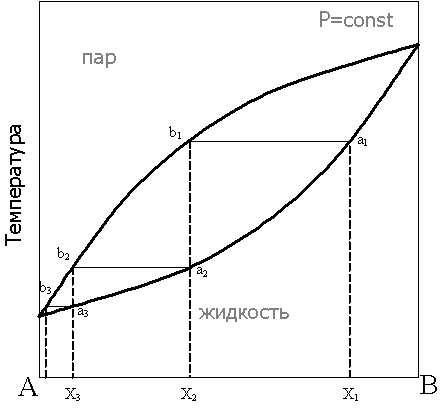
Второй закон Коновалова (1881 г.) описывает растворы с отклонениями от свойств идеальных растворов и объясняет существование азеотропных растворов, состав которых при перегонке не изменяется: Экстремумы на кривых полного давления пара отвечают такому равновесию раствора и насыщенного пара, при котором состав обеих фаз одинаков
28.Простая и фракционная перегородка
Перегонкойназывается способ очистки жидкой смести от примесей или способ разделения жидкостей на 2 чистых вещества путём кипячения с последующим отведением пара.
Если цикл кипячения отведения пара проводится однократно,то перегонка -простая, а если таких циклов несколько и они следуют последовательно друг за другом, то перегонка-фракционная.
29.Экстракция,экстрагент,коэффициент распределения
Экстракция– процесс перехода из одной фазы в другую.
Коэффициент распределенияпоказывает во сколько раз концентрация вещества в фазе экстрагента больше чем в фазе экстрактива.
Экстрагент–жидкость, которая не смешивается с фазой экстрактива. Экстрагент должен характеризоваться максимальным коэффициентом распределения по извлекаемому веществу.
Экстракт- органическая фаза, отделенная от водной фазы и содержащая экстрагированные соединения.(однократная,многократная,непрерывная,противоточная).
